Clear Sky Science · es
La traducción local específica de ARNm está modelada por condensados para el crecimiento de células multinucleadas
Cómo las células grandes mantienen sincronizadas tareas distantes
Las células de nuestros cuerpos suelen ser unidades diminutas y autónomas con un solo núcleo. Pero algunos organismos, incluidos ciertos hongos y las células musculares, son compartimentos enormes llenos de muchos núcleos que comparten el mismo citoplasma. En estos gigantes, las señales y moléculas pueden tardar mucho en difundirse de un lugar a otro, lo que plantea una pregunta: ¿cómo coordinan el crecimiento y la división a través de distancias tan grandes sin perder el control? Este estudio aborda esa cuestión en un hongo multinucleado al descubrir cómo diminutas gotas dentro de la célula ajustan localmente la producción de proteínas justo donde se necesitan.
Diminutas gotas que organizan una célula gigante
En el hongo filamentosos Ashbya gossypii, células largas en forma de tubo llamadas hifas contienen muchos núcleos que se dividen de forma asincrónica mientras el crecimiento ocurre principalmente en las puntas. Trabajos anteriores demostraron que una proteína llamada Whi3 forma gotas microscópicas, o condensados, con ARNm específicos que codifican reguladores clave del ciclo celular y del crecimiento de la punta. Aquí, los autores buscaron entender qué hacen realmente estos condensados. Usando imágenes tridimensionales rápidas, hallaron que los condensados de Whi3 cambian de tamaño y número según la posición en la célula y el estado local de crecimiento y división nuclear. Los condensados grandes se agrupan cerca de puntas hifales con crecimiento lento, mientras que condensados más pequeños y variables rodean núcleos en etapas concretas del ciclo celular. Hongos mutantes que no pueden formar condensados normales crecen más rápido en las puntas y muestran divisiones nucleares más sincronizadas, lo que sugiere que las propiedades de los condensados ayudan a coordinar estos procesos.
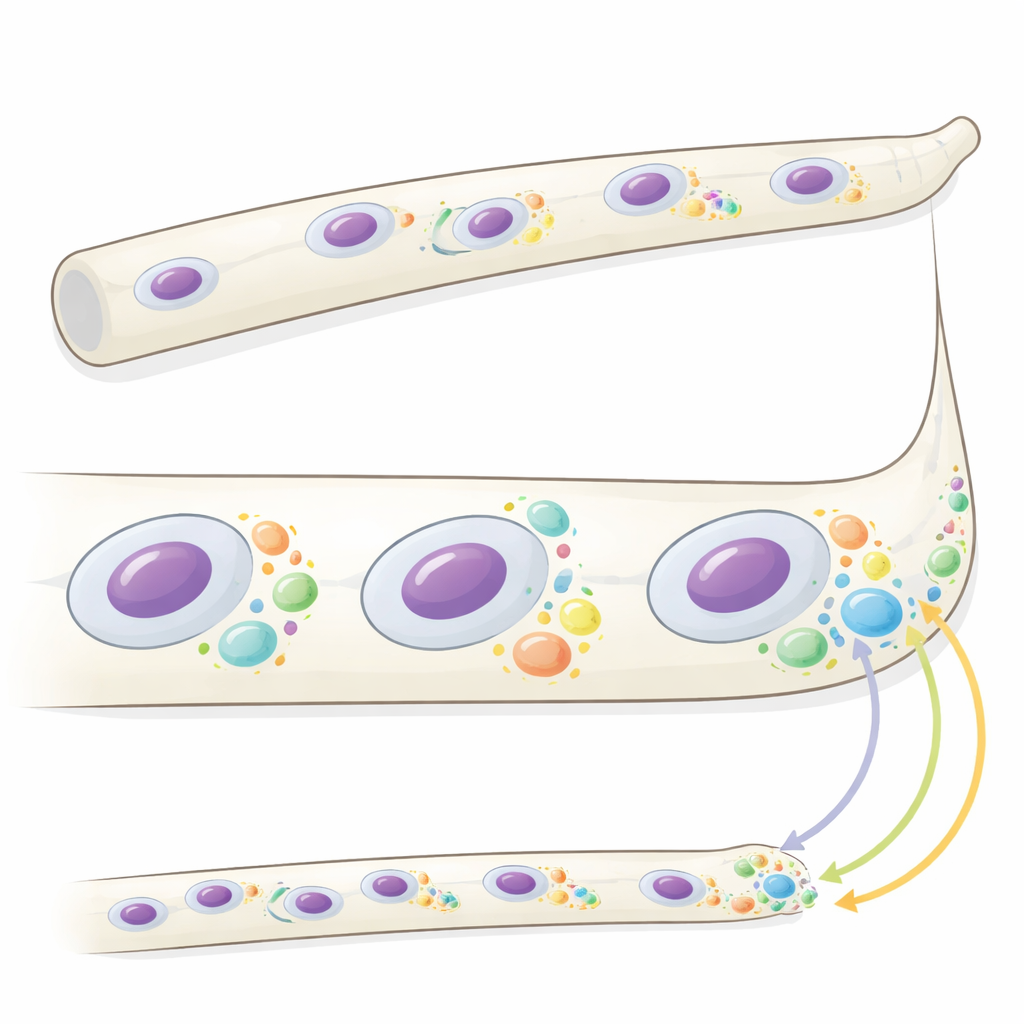
Producción proteica local escrita en el espacio y en el tiempo
Para ver si los condensados de Whi3 controlan dónde se producen las proteínas, el equipo midió la traducción —el proceso de convertir ARNm en proteína— de dos mensajeros importantes ligados a Whi3. Uno, CLN3, codifica una ciclina que ayuda a impulsar las células a través del ciclo de división; el otro, BNI1, codifica un factor que modela el crecimiento en la punta hifal. Usando un método fluorescente sensible que detecta ribosomas activos sobre ARNm endógenos individuales, los investigadores mostraron que CLN3 se traduce principalmente cerca de determinados núcleos y sólo durante fases específicas de su ciclo, especialmente alrededor de núcleos en mitosis. El ARNm de BNI1 se agrupa en las puntas hifales, pero su traducción allí suele ser escasa y variable. Cuando el comportamiento de Whi3 se altera por una mutación fosfo-mimética, la traducción de BNI1 se enriquece fuertemente en las puntas y el crecimiento de la punta se acelera, revelando que Whi3 puede reprimir o permitir la traducción según su estado y ubicación.
Piezas mínimas, muchos resultados
Para comprobar si este ajuste es una propiedad intrínseca de los componentes del condensado, los autores recrearon el sistema en extractos celulares libres. Unieron un reportero de luciferasa a las regiones regulatorias de los ARNm de CLN3 o BNI1 y mezclaron estos ARNm con Whi3 purificado a diferentes concentraciones. A niveles bajos, donde no se forman gotas, la traducción cambió poco. A niveles más altos que inducen la formación de condensados, la traducción ligada a CLN3 se reprimió fuertemente a medida que aumentaban la concentración de Whi3 y el tamaño del condensado. BNI1 se comportó de forma diferente: niveles moderados de condensado aumentaron su traducción, mientras que condensados más abundantes o más grandes convirtieron el sistema en represión. Versiones mutantes de Whi3 que formaban gotas más pequeñas o menos numerosas, o ARNm con menos sitios de unión a Whi3, desplazaron estas respuestas, aliviando a menudo la represión y potenciando la traducción. Estos experimentos muestran que los mismos ingredientes básicos —Whi3, sus ARNm diana y sus condensados— pueden generar un continuo de estados traduccionales simplemente alterando la concentración, la fuerza de interacción o el tamaño de la gota.
Dónde ocurre la traducción: en el borde de la gota
Los ensayos a granel promedian sobre muchas moléculas y no pueden revelar dónde ocurre la traducción dentro o alrededor de los condensados. Para visualizar esto directamente, el equipo usó un reportero "MoonTag" que se ilumina cuando emergen nuevas cadenas proteicas de los ribosomas. In vitro, observaron señales MoonTag acumulándose sobre y dentro de las gotas Whi3–ARN, lo que demuestra que estos condensados pueden ser sitios activos de traducción más que meros depósitos de almacenamiento. De forma llamativa, tanto los ribosomas como las señales de proteínas nacientes fueron más fuertes en la interfaz de la gota, formando un anillo brillante alrededor de cada condensado. Los condensados más pequeños, con más área superficial en relación con su volumen, soportaron más traducción por ARNm que las gotas más grandes, que fueron en conjunto más represivas. Cambiar la valencia del ARNm o el estado de carga de Whi3 desplazó si esta zona permisiva para la traducción se situaba en la superficie o más hacia el interior, indicando que rasgos moleculares sutiles del condensado ajustan la facilidad con la que la maquinaria de traducción puede acceder a los ARNm residentes.
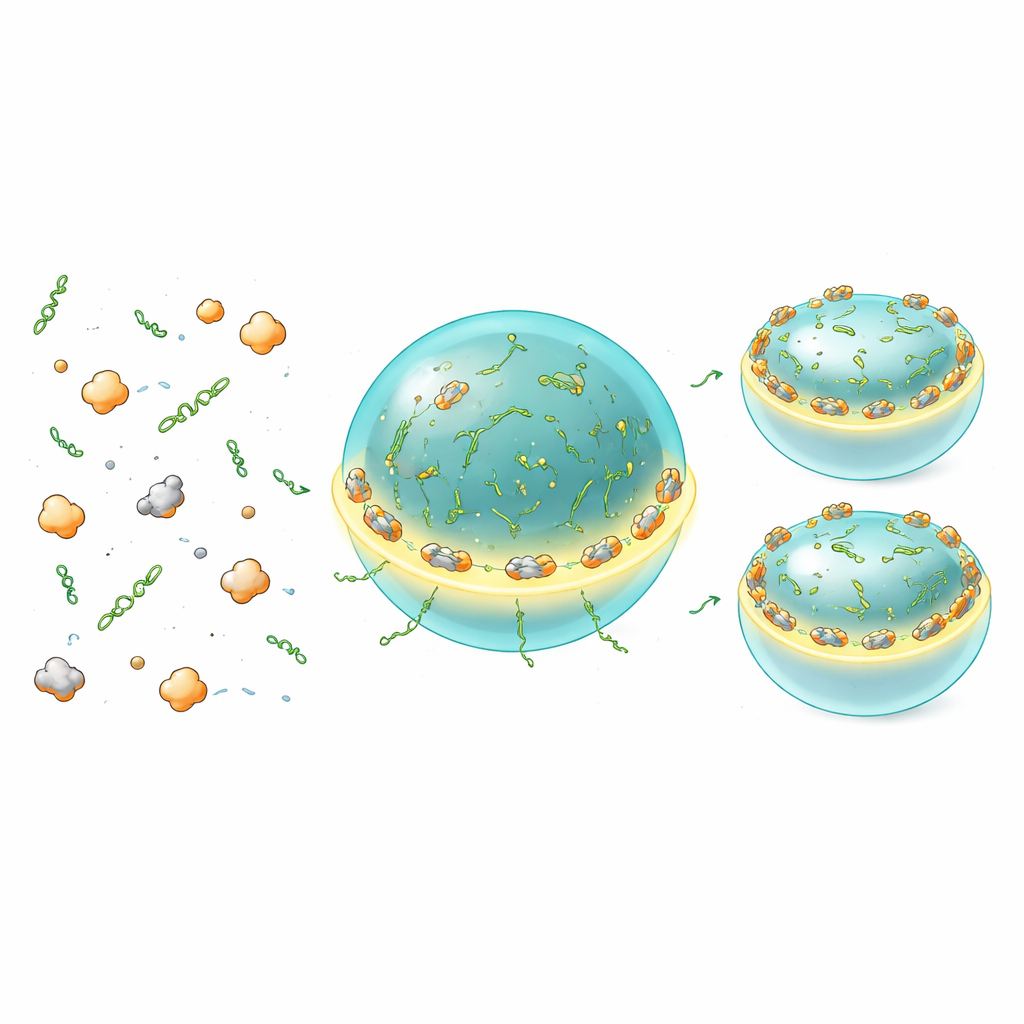
Dosis finamente ajustadas para un crecimiento equilibrado
En conjunto, el trabajo presenta a los condensados Whi3–ARN como válvulas ajustables que dosifican la proteína producida localmente en lugar de interruptores simples de apagado/encendido. En el hongo, esto significa que la ciclina CLN3 puede producirse en pulsos alrededor de núcleos seleccionados para mantener sus ciclos de división desfasados, mientras que BNI1 puede fabricarse en ráfagas intermitentes en las puntas hifales para sostener el crecimiento y a la vez evitar una expansión descontrolada en un único sitio. Cuando la formación o las propiedades de los condensados se alteran, se pierde este control matizado: la producción de proteínas se vuelve más uniforme en espacio y tiempo, los núcleos se dividen sincronizadamente, cambian los patrones de ramificación y se altera la morfología general. Para un público general, el mensaje clave es que las células pueden usar diminutas gotas separadas por fase como reactores espacial y temporalmente ajustables, permitiendo que células enormes y multinucleadas coordinen el crecimiento y la división a lo largo de grandes distancias al esculpir localmente cuándo y dónde se producen las proteínas.
Cita: Geisterfer, Z.M., Jalihal, A.P., Cole, S.J. et al. RNA-specific local translation is patterned by condensates for multinucleate cell growth. Nat Cell Biol 28, 507–519 (2026). https://doi.org/10.1038/s41556-026-01887-y
Palabras clave: condensados biomoleculares, traducción local, control del ciclo celular, hifas fúngicas, separación de fases