Clear Sky Science · es
La ubiquitinación en lisina 11 impulsa la inducción de interferón tipo I/III por cGAS–STING y los receptores Toll-like 3 y 4
Cómo nuestras células dan la alarma
Cuando virus o moléculas dañinas invaden el organismo, nuestras células deben decidir en minutos si ponen en marcha potentes señales antivirales llamadas interferones. Estas señales pueden salvarnos de infecciones graves, pero si se disparan inadecuadamente también provocan enfermedades autoinmunes dañinas. Este estudio revela un “centralita” molecular hasta ahora oculta dentro de las células que ayuda a decidir cuándo activar las respuestas de interferón y cuándo contenerlas. Comprender esta centralita ofrece pistas para mejorar vacunas, terapias antivirales y tratamientos para trastornos impulsados por interferones.
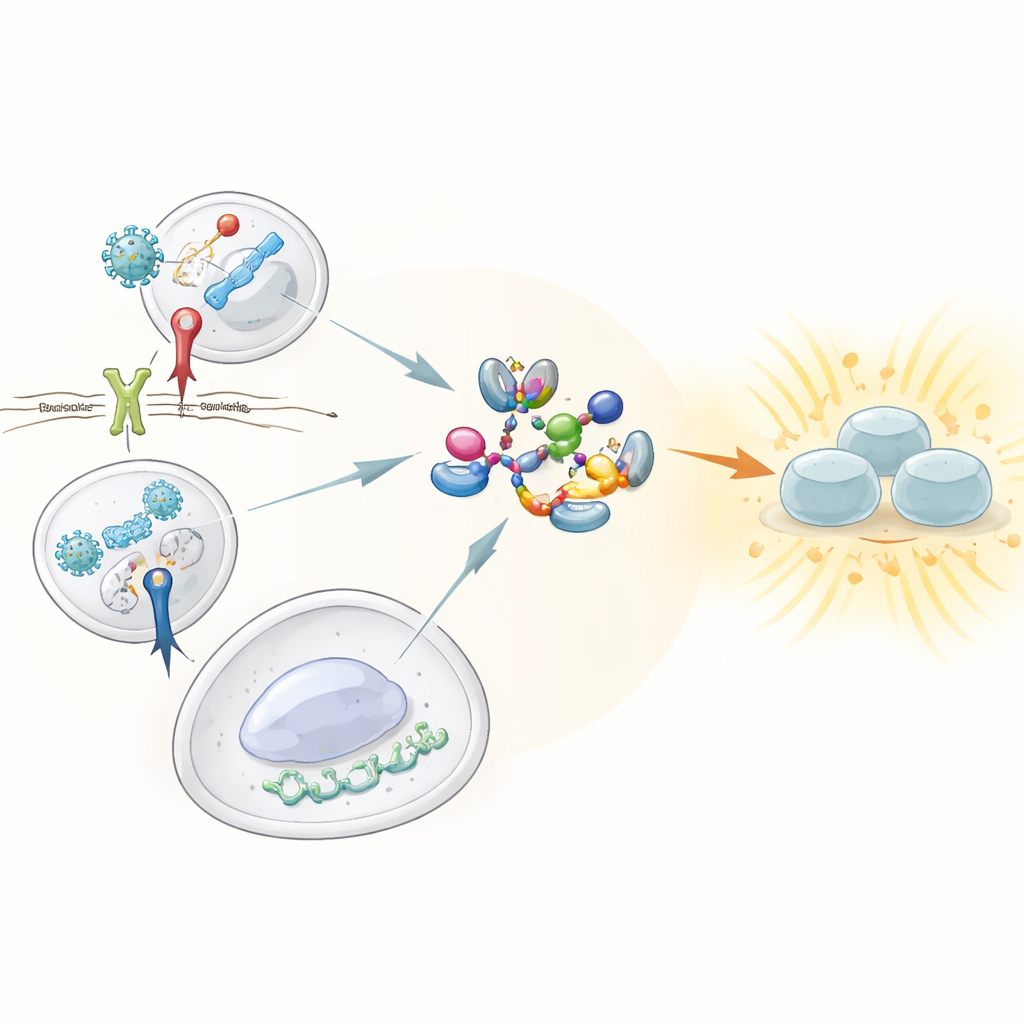
Guardianes que detectan peligro
Nuestro sistema inmune innato se apoya en centinelas conocidos como receptores de reconocimiento de patrones, que patrullan en busca de rasgos característicos de virus y bacterias. Entre ellos destacan tres por su capacidad para desencadenar fuertes respuestas de interferón: el receptor Toll-like 3 (TLR3), que detecta ARN viral de doble hebra; el receptor Toll-like 4 (TLR4), que percibe un componente de la pared bacteriana; y la vía cGAS–STING, que identifica ADN fuera de su sitio dentro de las células. Los tres deben activar una enzima central llamada TBK1, que a su vez activa el factor de transcripción IRF3 para impulsar la producción de interferones de tipo I y III. Hasta ahora no se comprendía bien cómo estos sensores convergían sobre TBK1 para convertirlo en su forma activa.
Un conector molecular oculto
Los investigadores descubrieron que una proteína llamada ANKIB1 actúa como un conector crucial entre estos sensores y TBK1. ANKIB1 es una enzima que une pequeñas etiquetas moleculares, conocidas como cadenas de ubiquitina, a otras proteínas. De manera importante, construye un tipo específico de cadena, basada en un enlace llamado «K11», que hasta ahora se conocía más por funciones en la división celular que en la inmunidad. En células humanas carentes de ANKIB1, la estimulación de TLR3 o la activación de STING ya no conducía a la activación adecuada de TBK1 e IRF3, y los genes de interferón apenas se activaban. Restaurar ANKIB1 devolvía la respuesta, mostrando que esta única enzima es a la vez necesaria y suficiente para impulsar esta rama de la alarma antiviral.
Construir una plataforma de acoplamiento para proteínas de relevo
Una inspección más detallada reveló cómo ejerce su influencia ANKIB1. Cuando TLR3 o STING detectan peligro, ensamblan plataformas multiproteicas llamadas signalosomas. ANKIB1 es reclutado a estas plataformas mediante una región que reconoce ubiquitina. Una vez allí, marca con cadenas de ubiquitina unidas por K11 a varios componentes clave —incluidos los adaptadores TRIF y la misma STING, así como a otras moléculas de señalización—. Estas cadenas no simplemente señalan proteínas para su destrucción; en cambio actúan como velcro molecular. Otra proteína, Optineurina (OPTN), se atrae específicamente a estos sitios modificados. Sirviendo como un adaptador de relevo, OPTN trae entonces a TBK1 al complejo para que pueda activarse y transmitir la señal hacia IRF3 y los genes de interferón. Cuando se eliminó OPTN, la activación de TBK1 colapsó, subrayando que el etiquetado ligado a K11 por ANKIB1 y la unión de OPTN forman un único eje esencial.
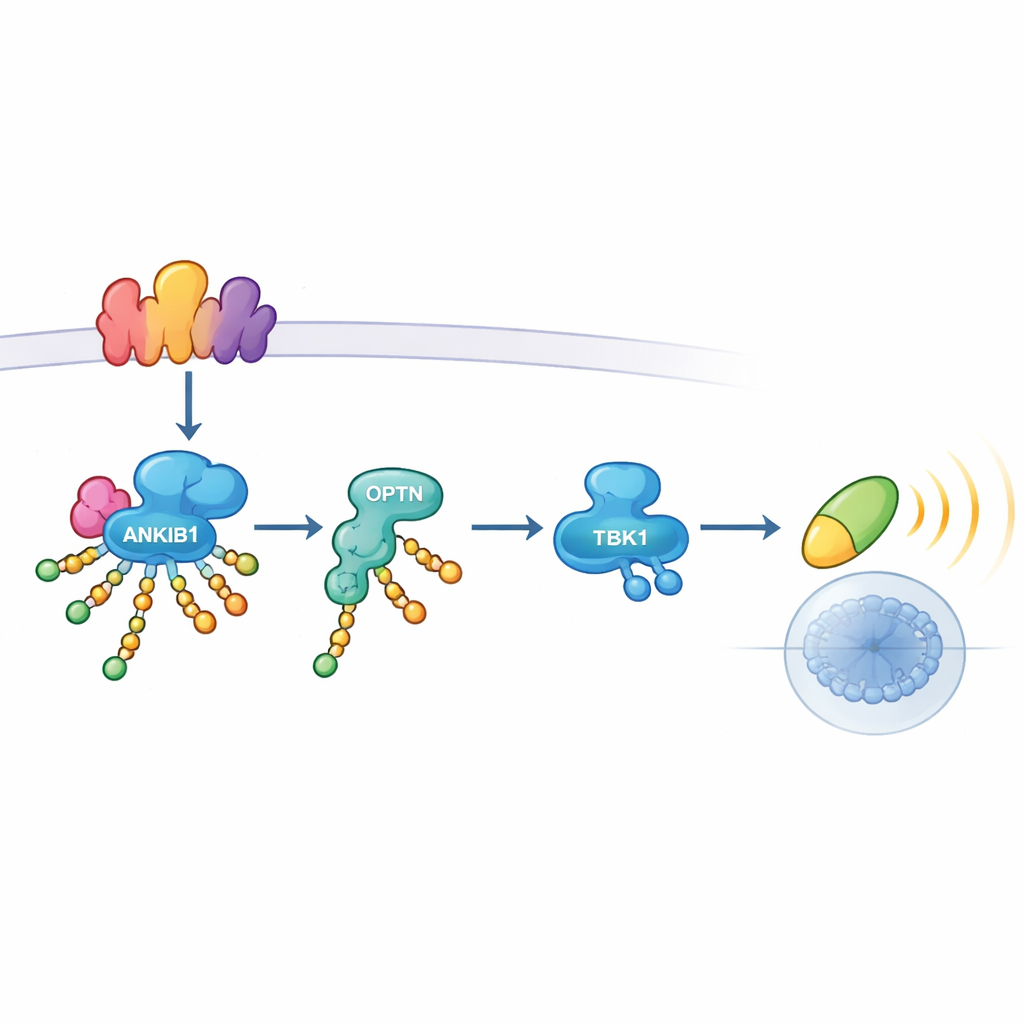
Cuándo importa esta vía —y cuándo no
El equipo se preguntó a continuación si este mecanismo es universal entre todos los sensores antivirales. Encontraron que ANKIB1 es vital para la inducción de interferón a través de TLR3, el brazo dependiente de TRIF de TLR4 y la vía cGAS–STING, todos los cuales usan a OPTN como adaptador principal hacia TBK1. En contraste, otro sensor, RIG-I, que detecta ARN viral, depende de un conjunto distinto de proteínas adaptadoras y no necesita ANKIB1 ni OPTN para activar TBK1. Experimentos en ratones reflejaron estos hallazgos celulares. Los animales sin Ankib1 produjeron mucho menos interferón tras activar TLR3 o STING, se mostraron protegidos frente a un síndrome inflamatorio letal impulsado por interferón, pero se volvieron mucho más vulnerables a la infección por herpes simple virus 1, un virus de ADN que depende en gran medida de la vía cGAS–STING para el control. Las respuestas al virus de la gripe, que es detectado principalmente por RIG-I, permanecieron en gran medida intactas.
Equilibrar protección y daño
En conjunto, estos resultados revelan las cadenas de ubiquitina unidas en K11 generadas por ANKIB1 como una moneda central en una rama mayor de la señalización antiviral innata. Al crear sitios de acoplamiento para OPTN, ANKIB1 ayuda a ensamblar el relevo molecular preciso que convierte el peligro detectado por TLR3, TLR4 (a través de TRIF) y cGAS–STING en una producción robusta de interferón. Este eje tiene doble filo: es esencial para la defensa contra ciertos virus, pero también alimenta la enfermedad inflamatoria impulsada por interferón cuando se sobreactiva. Dado que la actividad catalítica de ANKIB1 y dominios específicos son necesarios para esta función, presentan dianas atractivas para futuros fármacos diseñados ya sea para atenuar respuestas de interferón perjudiciales en condiciones autoinmunes o para potenciar la inmunidad antiviral cuando es demasiado débil.
Cita: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Palabras clave: inmunidad innata, señalización de interferón, ubiquitinación, vía cGAS–STING, infección viral