Clear Sky Science · es
El tejido adiposo peritumoral impulsa la evasión inmune en el cáncer colorrectal mediante la transformación adiposa–mesenquimal
Por qué importa la grasa abdominal alrededor de los tumores
El cáncer colorrectal crece dentro de la pared intestinal, pero se encuentra justo al lado de una gruesa capa de grasa abdominal. La mayoría de la gente considera que esta grasa es un relleno pasivo. Este estudio revela algo sorprendente: la grasa que rodea al tumor puede, silenciosamente, atraer las células inmunitarias que combaten el cáncer alejándolas del tumor, ayudando así al tumor a ocultarse del sistema inmune. Comprender esta lucha oculta sugiere nuevas formas de predecir quién responderá a la inmunoterapia y cómo mejorar la eficacia de estos tratamientos.
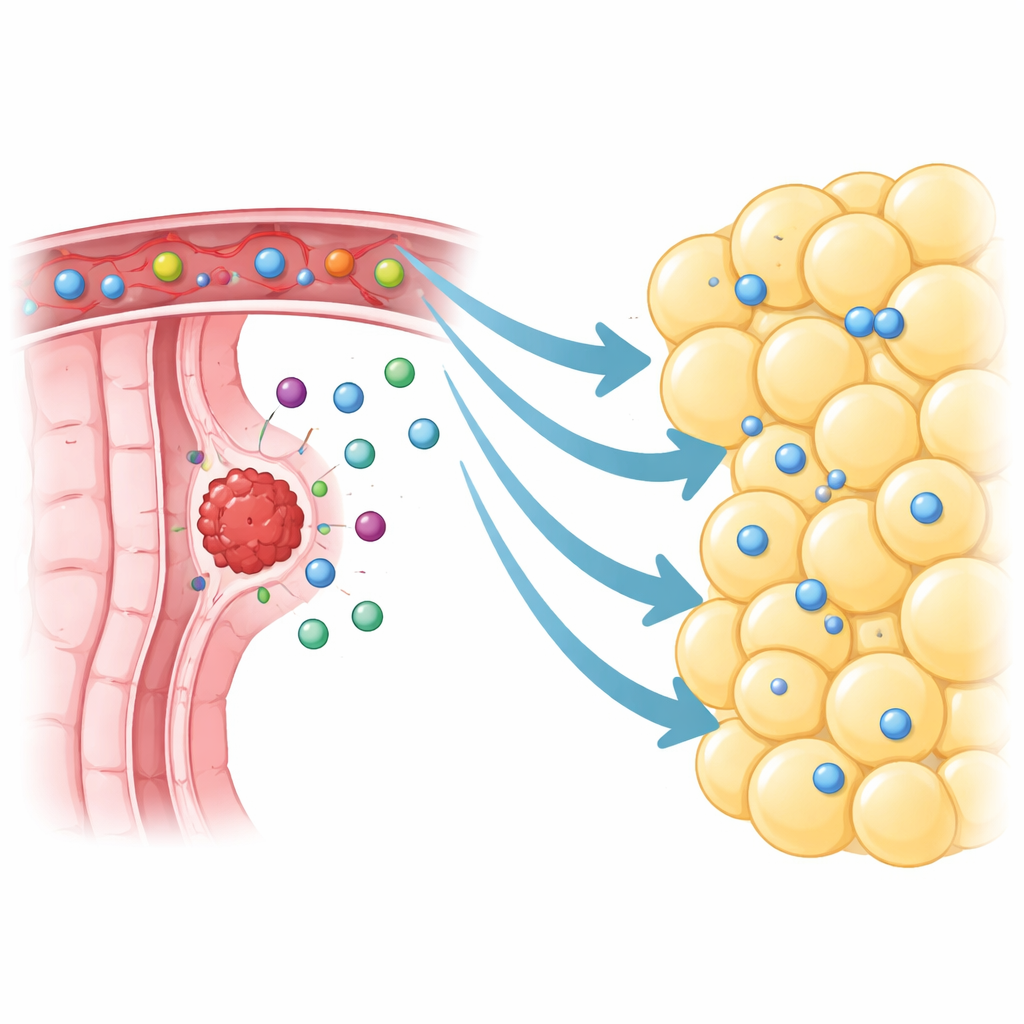
Un vecindario inmunitario activo junto al tumor
Los investigadores se centraron en la grasa visceral que rodea directamente los tumores colorrectales, denominada tejido adiposo visceral peritumoral. Usando secuenciación de ARN unicelular, cartografiaron más de 370.000 células individuales procedentes de tumores, grasa cercana, grasa distante y tejido normal. En lugar de ser silenciosa e inerte, la grasa junto a los tumores estaba repleta de células inmunitarias, especialmente linfocitos T y B. Incluso encontraron agrupaciones organizadas que semejaban pequeños ganglios linfáticos, indicios de que este tejido puede albergar reacciones inmunitarias activas. En comparación con la grasa tomada más lejos, la grasa peritumoral contenía muchas más células linfoides, incluidos linfocitos de memoria y células T citotóxicas específicas del tumor que, en principio, deberían patrullar en busca del cáncer.
Cuando las células inmunitarias útiles acaban en el lugar equivocado
Para ver si esta grasa rica en inmunidad ayudaba o perjudicaba, el equipo empleó modelos de ratón en los que se implantaron tumores cerca de una almohadilla grasa que imita la situación humana. A continuación, extirparon quirúrgicamente esa grasa cercana o la disolvieron químicamente. Contraintuitivamente, eliminar la grasa peritumoral ralentizó el crecimiento tumoral. Los tumores de ratones a los que se les había retirado esta grasa contenían más células T CD4 y CD8, incluidas células T que reconocían antígenos tumorales. Experimentos adicionales de seguimiento de células inmunitarias donantes mostraron que, cuando la grasa estaba presente, muchas de esas células se acumulaban en la almohadilla grasa en lugar de en el tumor. Quitar la grasa redirigió las células hacia el tumor, reforzando la respuesta antitumoral. En otras palabras, la grasa actuaba como un reservorio competitivo que absorbía las células inmunitarias y las impedía alcanzar su objetivo real.
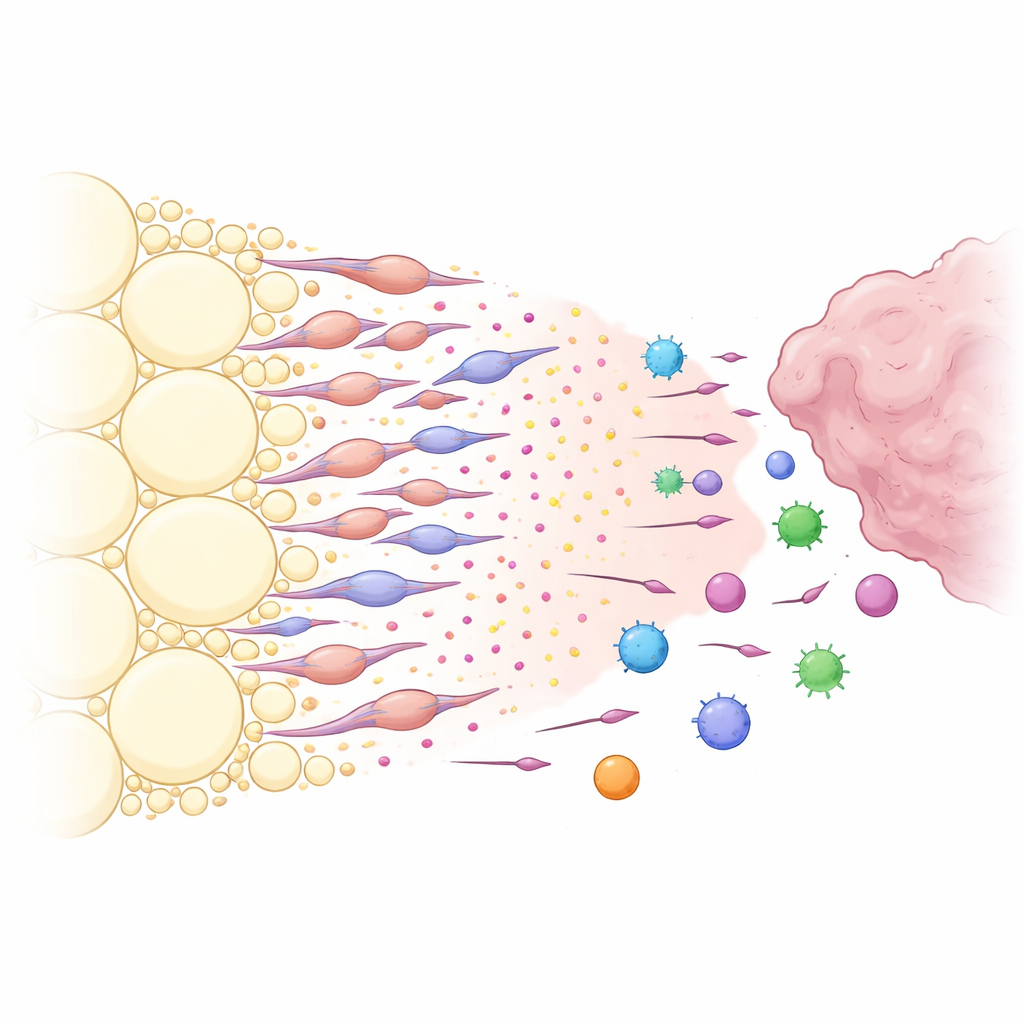
Un señuelo químico creado por células adiposas transformadas
¿Qué hacía que la grasa peritumoral fuera tan eficaz captando células inmunitarias? Al analizar las señales de comunicación entre tipos celulares, los investigadores identificaron una potente vía química centrada en la molécula CXCL12 y su receptor CXCR4. Las células estromales en la grasa cercana al tumor producían niveles elevados de CXCL12, mientras que muchas células inmunitarias expresaban CXCR4, volviéndolas sensibles a esta señal. Bloquear CXCL12 localmente en la grasa, o eliminarlo genéticamente en el estroma adiposo, hizo que los tumores se redujeran y permitió que más células inmunitarias CXCR4-positivas penetraran en el tumor en lugar de desviarse. El equipo descubrió entonces que los principales productores de CXCL12 no eran adipocitos ordinarios, sino un grupo especial de células derivadas de la grasa con aspecto de fibroblastos que denominaron fibroblastos asociados al cáncer derivados del tejido adiposo. Factores liberados por el tumor, especialmente el factor de crecimiento TGF-β1, empujaron a las células estromales adiposas locales a transformarse en estas células con aspecto fibroblástico, que a su vez secretaban grandes cantidades de CXCL12 y otras señales promotoras del crecimiento.
Convertir un escudo en un punto débil
Dado que estas células transformadas ayudan a desviar las células inmunitarias lejos de los tumores, los investigadores probaron si desmantelar este "sumidero inmunitario" podía mejorar la inmunoterapia. En ratones diseñados para que los fibroblastos asociados al cáncer derivados del tejido adiposo pudieran ser eliminados selectivamente, el tratamiento con un anticuerpo bloqueador de PD-1 resultó mucho más eficaz: los tumores crecieron menos y más células T específicas del tumor y positivas para CXCR4 infiltraron el cáncer. De manera similar, fármacos o anticuerpos que bloquearon CXCL12 o su receptor CXCR4 actuaron de forma sinérgica con el bloqueo de PD-1 en modelos de cáncer colorrectal subcutáneo y ortotópico. Estas combinaciones no solo redujeron el tamaño tumoral, sino que también remodelaron el paisaje inmune dentro del tumor.
Pistas de las exploraciones de pacientes y próximos pasos
El equipo se preguntó luego si sus hallazgos tenían relevancia en pacientes reales. En un grupo de personas con cáncer colorrectal localmente avanzado que recibían quimiorradioterapia combinada e inmunoterapia con bloqueo de PD-1, quienes obtuvieron una respuesta completa tendían a tener un menor volumen de grasa visceral peritumoral en la resonancia magnética previa al tratamiento. Cuantitativamente, el área de esta grasa predijo la respuesta terapéutica mejor que algunos marcadores tisulares estándar, y los pacientes con grandes volúmenes de grasa peritumoral presentaron tasas de respuesta mucho menores. Para un no especialista, la conclusión es contundente: no solo el tumor en sí, sino también la grasa que lo rodea inmediatamente, puede determinar cuánto funciona la inmunoterapia. Al centrarse en esta grasa —ya sea midiéndola para orientar decisiones de tratamiento o apuntando a sus células estromales transformadas y a la señal CXCL12–CXCR4— puede ser posible convertir un escudo protector del tumor en un punto débil terapéutico.
Cita: Wang, JH., Zheng, YQ., Qian, ZY. et al. Peritumoural adipose tissue drives immune evasion in colorectal cancer via adipose–mesenchymal transformation. Nat Cell Biol 28, 581–595 (2026). https://doi.org/10.1038/s41556-026-01885-0
Palabras clave: cáncer colorrectal, microambiente tumoral, grasa visceral, inmunoterapia, CXCL12 CXCR4