Clear Sky Science · es
Genómica funcional con resolución temporal mediante aprendizaje profundo revela un control jerárquico global de la autofagia
Cómo las células se reciclan a sí mismas — y saben cuándo parar
Nuestras células sobreviven a tiempos de escasez reciclando sus propias partes mediante un proceso llamado autofagia — literalmente, “comerse a sí mismas”. Muy poco reciclaje provoca la acumulación de componentes dañados; demasiado y la célula se canibaliza. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones para el envejecimiento y la enfermedad: ¿cómo activa y desactiva una célula viva la autofagia en los momentos adecuados al subir y bajar los nutrientes?
Siguiendo a miles de células durante un ciclo de abundancia a inanición
Para abordar esto, los investigadores usaron la levadura de panadería como modelo y observaron casi seis mil cepas mutantes distintas mientras pasaban por inanición y recuperación. Cada cepa de levadura llevaba etiquetas fluorescentes que marcaban estructuras implicadas en la autofagia, lo que permitió a un microscopio de alta potencia capturar imágenes cada hora mientras los nutrientes se retiraban y luego se restauraban. En lugar de clasificar esas imágenes manualmente, el equipo entrenó algoritmos de aprendizaje profundo para reconocer cuándo una célula estaba en un estado autofágico, basándose completamente en características de la imagen y no en el juicio humano. Esto produjo series temporales precisas de la actividad autofágica para casi todo el genoma de la levadura, revelando cuán rápido y con qué intensidad respondía cada mutante a los cambios de nutrientes. 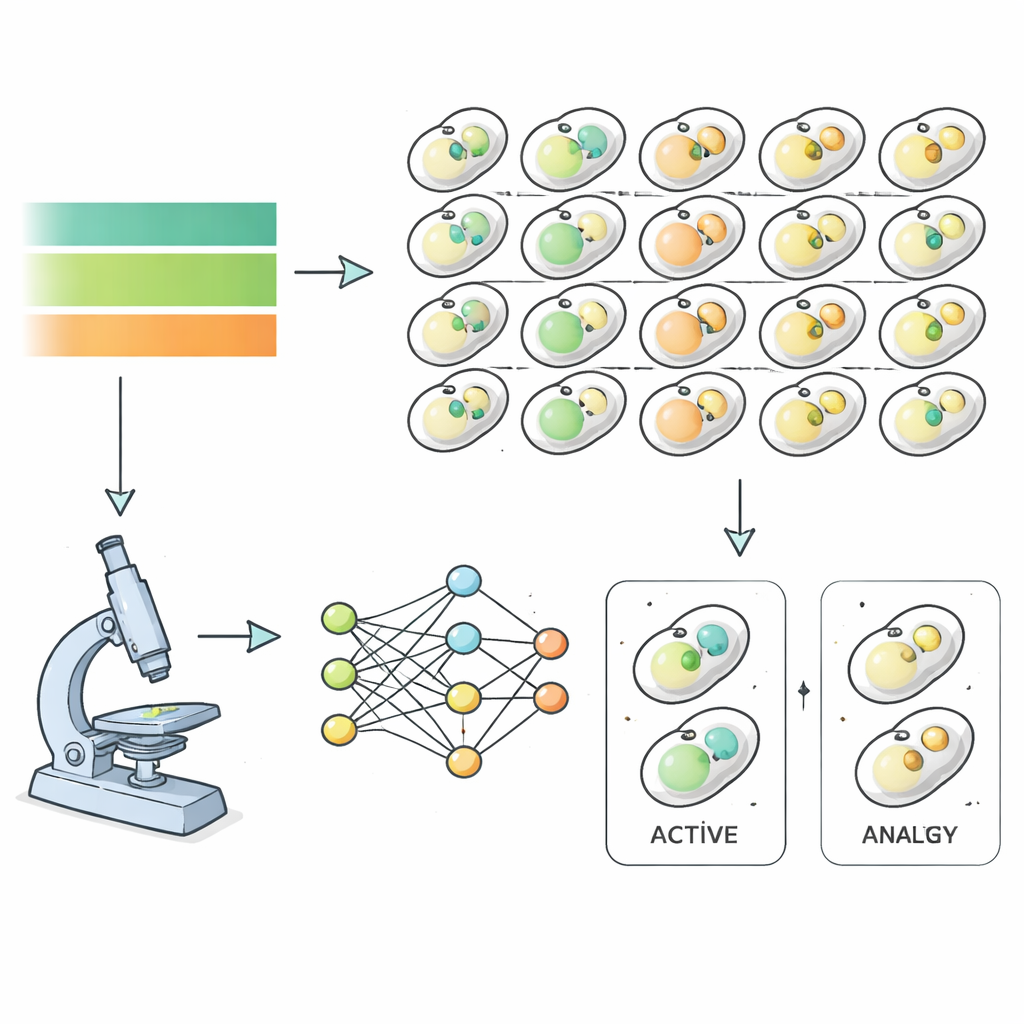
Seis maneras distintas en que las células gestionan mal el reciclaje
Al ajustar matemáticamente estas series temporales, los autores extrajeron detalladas “huellas cinéticas” para cada mutante: qué tan rápido se activaba la autofagia, cuánto tiempo se mantenía alta y con qué brusquedad se apagaba. Agrupar estas firmas desenmascaró seis grandes tipos de comportamiento. Algunos mutantes eran “ultrasensibles”, respondiendo muy rápido tanto a la inanición como a la vuelta de los nutrientes. Otros eran “hiposensibles”, reaccionando con lentitud. Un grupo “hiperactivo” mostraba un reciclaje basal anormalmente alto, mientras que varios grupos presentaban distintos grados de incapacidad para montar una respuesta adecuada. Es importante destacar que genes nucleares conocidos de la autofagia cayeron en las clases más severas, lo que valida que el método captura biología genuina y no ruido de medición.
Mapeando una jerarquía de control sobre la autofagia
La autofagia no ocurre de forma aislada; está integrada en las redes regulatorias más amplias de la célula. El equipo superpuso sus perfiles dinámicos sobre grandes mapas de interacciones genéticas y proteicas en levadura. Los genes cuya pérdida causaba defectos fuertes en la autofagia tendían a situarse cerca de la “máquina central” conocida de la autofagia en esas redes, mientras que los mutantes más sutiles estaban más alejados, coherente con un control más indirecto. Al examinar qué procesos celulares estaban enriquecidos en cada clase de comportamiento, hallaron que la activación desencadenada por inanición está fuertemente moldeada por vías que gestionan ARN, producción proteica y metabolismo energético, mientras que el apagado de la autofagia tras la recuperación de nutrientes depende más del tráfico y fusión de membranas que eliminan las vesículas de reciclaje.
Detallando cómo se forman y se eliminan las vesículas
La autofagia progresa en dos etapas principales: construir vesículas cargadas de material y luego fusionarlas con el compartimento de reciclaje de la célula para su degradación. Para diseccionar estas etapas, los investigadores extrajeron el “espacio latente” dentro de su red neuronal —la representación comprimida que ésta usa para distinguir imágenes. Proyectando esa representación interna en un mapa bidimensional, pudieron ver cómo las poblaciones celulares se desplazaban desde una región sin vesículas, pasando por otra con muchas vesículas libres, y finalmente a una región donde las vesículas habían sido eliminadas. Usando comparaciones estadísticas frente a mutantes de referencia bloqueados en distintas etapas, cuantificaron para cada gen si afectaba principalmente la formación de vesículas, su eliminación o ambas. Este análisis mostró que el control de la formación de vesículas es altamente sensible a los niveles de nitrógeno a lo largo del tiempo, mientras que la maquinaria de eliminación se comporta con mayor constancia y a menudo es el principal factor limitante del flujo global de reciclaje. 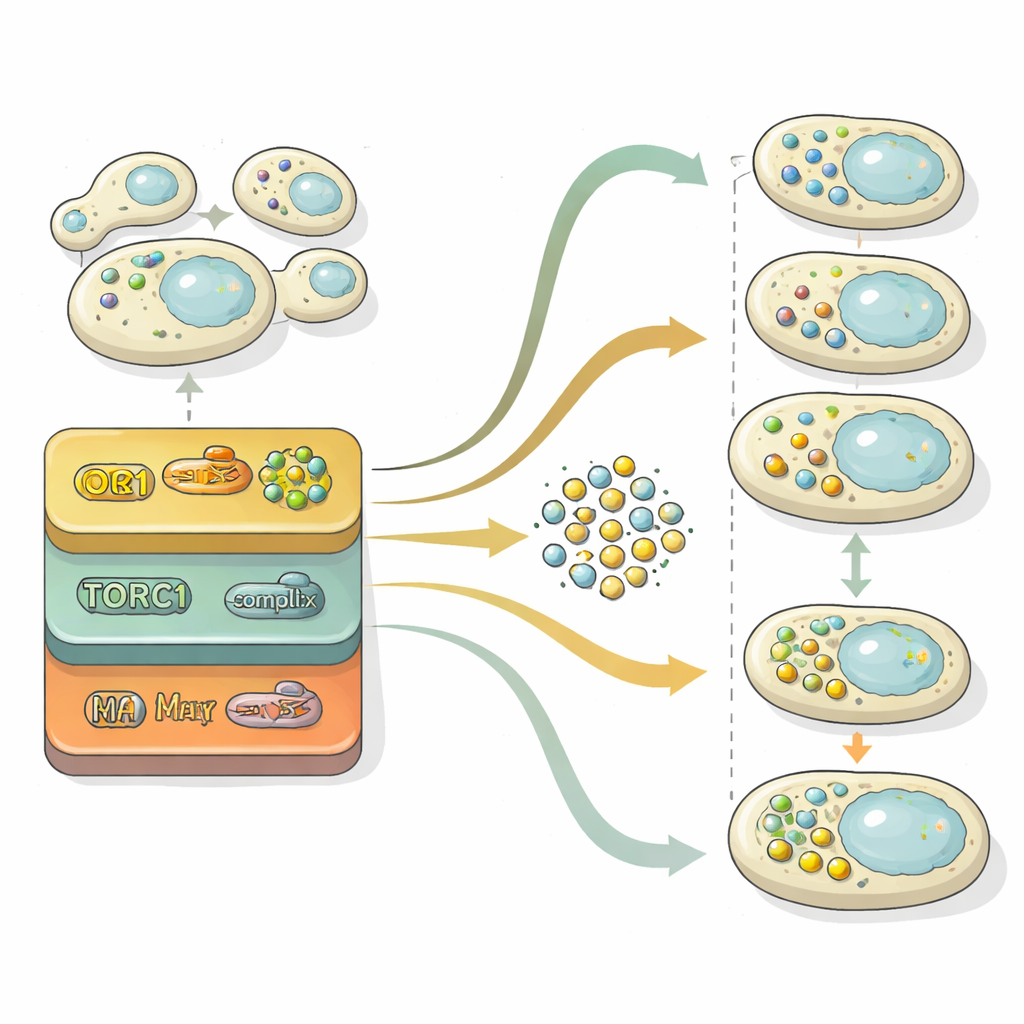
Un freno oculto al reciclaje: la vía retrógrada
Uno de los descubrimientos más llamativos concierne a la llamada vía retrógrada (RTG), que transmite señales desde las mitocondrias al núcleo. Las células de levadura sin componentes RTG producían demasiados autofagosomas incluso cuando los nutrientes eran abundantes y tenían dificultades para eliminarlos una vez que los nutrientes volvían. Experimentos de seguimiento detallados mostraron que esta vía controla la expresión de genes clave de la autofagia, especialmente el iniciador maestro ATG1, en gran medida independiente del conocido sensor de nutrientes TORC1, diana de fármacos como la rapamicina. En efecto, la señalización RTG actúa como un freno que varía en el tiempo y evita una autofagia descontrolada en condiciones ricas y ayuda a terminar la respuesta cuando las condiciones mejoran.
Por qué esto importa para la salud y la terapia
En conjunto, este trabajo ofrece un mapa a escala genómica y con resolución temporal de cómo las células ajustan la autofagia ante cambios en las condiciones de nutrientes. Revela que la activación y el apagado no son imágenes especulares: muchos más genes influyen en cómo comienza el reciclaje que en cómo se detiene, y el equilibrio a largo plazo depende en gran medida de la eliminación de vesículas y de frenos transcripcionales como la vía RTG. Para un lector general, la conclusión clave es que el autocánibalismo celular está sometido a un control estratificado y jerárquico, y que ahora podemos cartografiar esas capas con alta precisión. Esta visión a nivel de sistemas podría, con el tiempo, guiar terapias más matizadas que ajusten la autofagia en fases específicas —potenciando el reciclaje beneficioso sin desencadenar los efectos dañinos de una autodegradación crónica y descontrolada.
Cita: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
Palabras clave: autofagia, aprendizaje profundo, genética de la levadura, detección de nutrientes, reciclaje celular