Clear Sky Science · es
Fenotipado refinado de las respuestas a vacunas revela determinantes transcriptómicos de la heterogeneidad de anticuerpos neutralizantes
Por qué algunas vacunas funcionan mejor en ciertas personas
Cuando nos pinchamos para recibir una vacuna contra la COVID-19, podríamos suponer que el sistema inmune de todo el mundo reacciona igual. En realidad, las personas varían mucho en la rapidez y la intensidad con que generan anticuerpos protectores. Este estudio siguió a adultos que recibieron vacunas inactivadas contra el SARS-CoV-2 y muestra que las respuestas a la vacuna se agrupan en patrones distintos, cada uno impulsado por señales inmunitarias tempranas diferentes escritas en nuestros genes y células sanguíneas. Comprender estos patrones podría permitir en el futuro ajustar los calendarios de vacunación para que cada persona obtenga la protección que necesita.
Tres caminos hacia la protección tras la misma inyección
Los investigadores siguieron a 73 adultos sanos que recibieron dos dosis de una vacuna inactivada contra la COVID-19. Midieron anticuerpos neutralizantes —aquellos capaces de bloquear el virus— antes de la vacunación, una semana después de la segunda dosis y de nuevo aproximadamente un mes más tarde. En lugar de dividir simplemente a la gente en “respondedores altos” y “bajos”, usaron métodos impulsados por los datos para agrupar a las personas según cómo cambiaron sus niveles de anticuerpos con el tiempo. Surgieron tres patrones claros: un grupo “bajo-retardado” con un aumento lento y modesto de anticuerpos; un grupo “rápido-estabilizado” cuyos anticuerpos se dispararon rápidamente y luego se estabilizaron; y un grupo de “aumento continuo” cuyos anticuerpos siguieron subiendo hasta alcanzar los niveles más altos. Estos patrones no se explicaron por la edad, el sexo o el peso corporal y solo en parte por la marca de vacuna inactivada que recibieron.
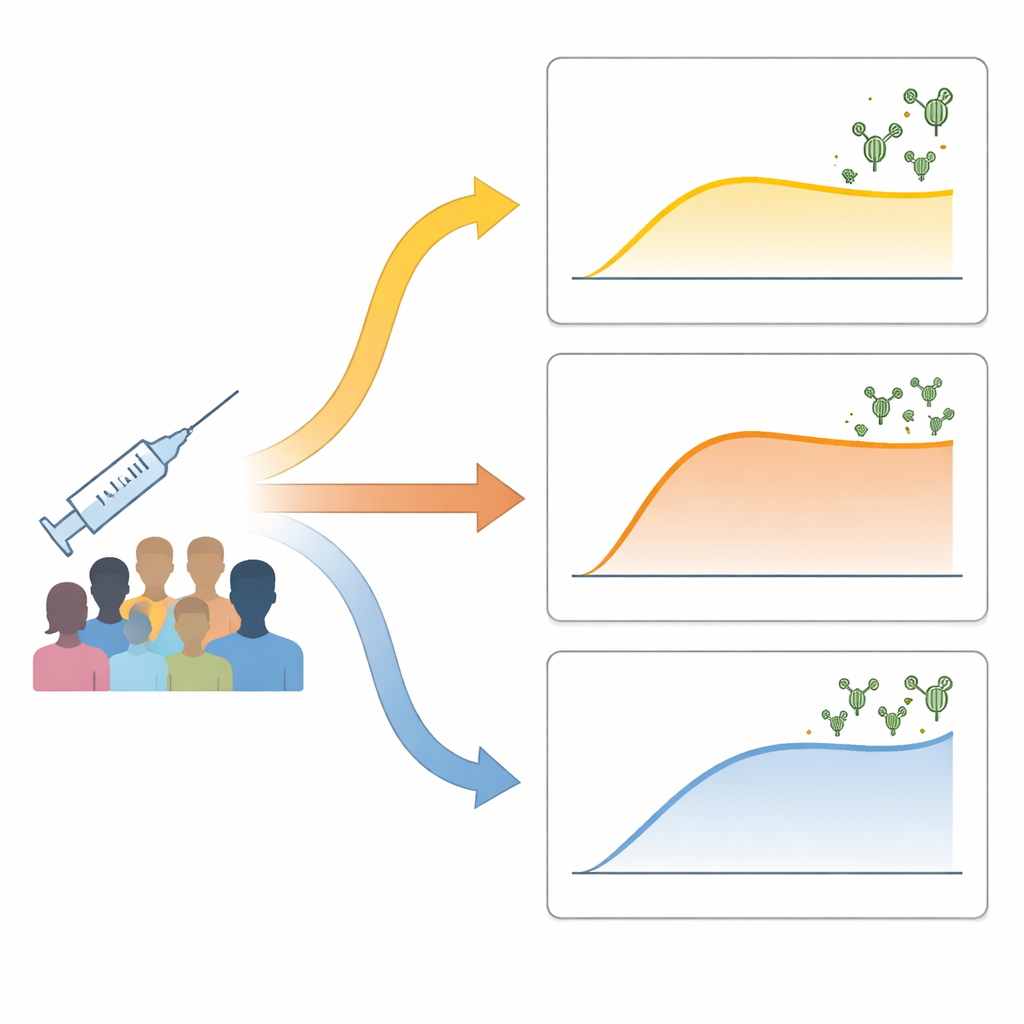
Cómo la actividad inmune temprana moldea el resultado
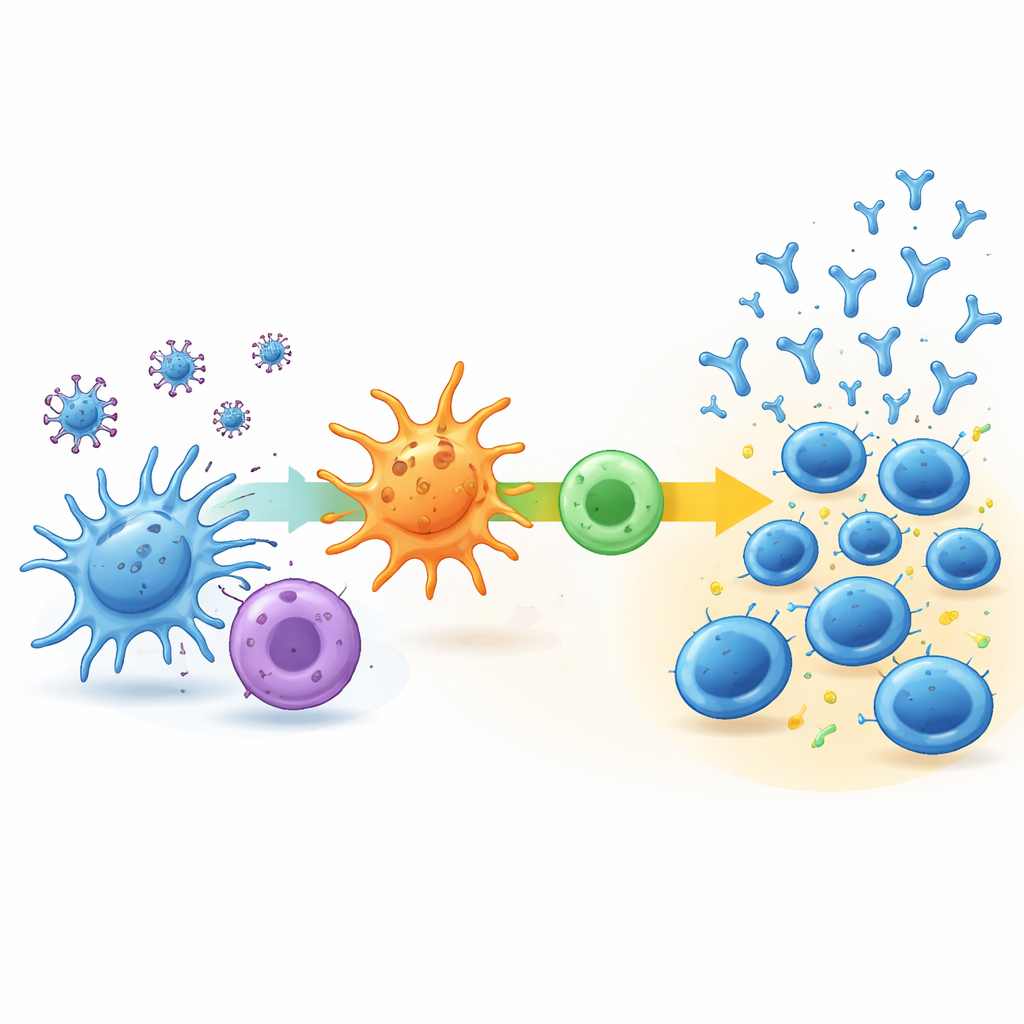
Para averiguar qué impulsa estos distintos trayectos, el equipo analizó la actividad genética de las células inmunitarias en sangre al inicio y una semana después de la segunda dosis. En el grupo bajo-retardado, casi no hubo cambios: las vías inmunitarias clave apenas se activaron y la composición de tipos celulares en la sangre permaneció en gran medida igual. En contraste, los grupos rápido-estabilizado y aumento continuo mostraron signos claros de activación inmune temprana. En los respondedores más fuertes hubo actividad coordinada en vías que procesan fragmentos virales, los presentan a otras células inmunitarias y favorecen un tipo de respuesta de células T helper conocida por potenciar la producción de anticuerpos. Estas personas también tendían a tener más células B naïvas y células T helper listas para responder, y más adelante mostraron una actividad algo mayor de células T específicas contra el virus.
Capas ocultas de control en el ARN y las células B
Más allá de los cambios sencillos de encendido/apagado génico, los científicos examinaron capas más sutiles de regulación presentes en el ARN, las moléculas intermedias entre el ADN y las proteínas. En el grupo con mejor respuesta, los genes inmunes implicados en presentar fragmentos virales al sistema inmunitario mostraron patrones diferentes de “splicing” y regiones terminales más cortas en su ARN. Se piensa que estas características facilitan la producción de ciertas proteínas y mantienen una señalización fuerte. El equipo también reconstruyó el repertorio de receptores de células B —las antenas únicas en las células productoras de anticuerpos— a partir de las mismas muestras de sangre. Aunque la diversidad global resultó similar entre los grupos, cada patrón de respuesta utilizó combinaciones y configuraciones ligeramente distintas de estos receptores, y los respondedores más fuertes favorecieron tipos de receptor previamente asociados con anticuerpos potentes frente a la proteína de la espiga del coronavirus.
Detectar probablemente a los respondedores bajos antes de la vacunación
Dado que las personas del grupo bajo-retardado pueden quedar menos protegidas tras un calendario de vacunación estándar, los investigadores preguntaron si sería posible identificarlas de antemano. Se centraron en un pequeño conjunto de genes que diferían de forma modesta en línea base entre los respondedores más débiles y los más fuertes. Usando métodos de aprendizaje automático, construyeron un modelo basado en la actividad de solo ocho genes medidos antes de la vacunación. Este modelo pudo distinguir con alta precisión a los respondedores bajo-retardado en su conjunto de datos, con dos genes implicados en la señalización celular básica y la inflamación aportando la mayor parte del poder predictivo. Aunque este enfoque debe validarse en grupos más grandes y diversos, sugiere que una simple prueba sanguínea podría en el futuro orientar planes de vacunación más personalizados.
Qué implica esto para las vacunas futuras
En conjunto, este estudio demuestra que las personas no se limitan a montar respuestas de anticuerpos “fuertes” o “débiles”; siguen cursos temporales distintos moldeados por eventos inmunitarios tempranos y difíciles de ver. Los individuos más protegidos activan redes coordinadas de genes y células que les permiten reconocer la vacuna con rapidez y generar anticuerpos duraderos, mientras que los respondedores bajos muestran una reacción temprana atenuada. Al mapear estas diferencias internas y crear herramientas para predecir quién responderá de forma pobre, el trabajo sienta las bases para la vacunación personalizada —por ejemplo, refuerzos más tempranos o formulaciones alternativas para las personas en riesgo— de modo que la promesa de las vacunas pueda repartirse de forma más equitativa.
Cita: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
Palabras clave: respuestas a vacunas, anticuerpos neutralizantes, vacunación contra COVID-19, heterogeneidad inmunitaria, vacunas personalizadas