Clear Sky Science · es
Inmunogenicidad y protección de candidatos a vacuna antigripal octavalente usando proteínas con adyuvante o mRNA-LNP en ratones vírgenes
Por qué importa una mejor vacuna contra la gripe
Las vacunas estacionales contra la gripe salvan muchas vidas, pero su protección puede variar mucho de un año a otro. Una razón es que las vacunas actuales entrenan principalmente al sistema inmunitario para reconocer una sola proteína viral, dejando otros objetivos útiles poco aprovechados. Este estudio en ratones explora vacunas antigripales de nueva generación que enseñan al sistema inmunitario a reconocer dos proteínas virales clave a la vez y compara un enfoque tradicional basado en proteínas con una tecnología más reciente de mRNA similar a la usada en las vacunas contra la COVID-19.
Dos objetivos en lugar de uno
Las vacunas actuales se centran mayoritariamente en la hemaglutinina, o HA, una proteína que ayuda al virus a adherirse a nuestras células. Los investigadores añadieron una segunda proteína viral, la neuraminidasa, o NA, que ayuda al virus a escapar de las células infectadas y propagarse. Combinando cuatro variantes de HA y cuatro variantes de NA de las cepas estacionales 2018–2019, construyeron una vacuna “octavalente” pensada para cubrir dos tipos de influenza A y dos linajes de influenza B. Luego encapsularon estos ocho componentes de dos formas distintas: como proteínas purificadas mezcladas con un ingrediente potenciador de la respuesta inmune, y como mRNA envuelto en pequeñas burbujas lipídicas (mRNA-LNP) que inducen a las propias células del cuerpo a producir las proteínas virales.
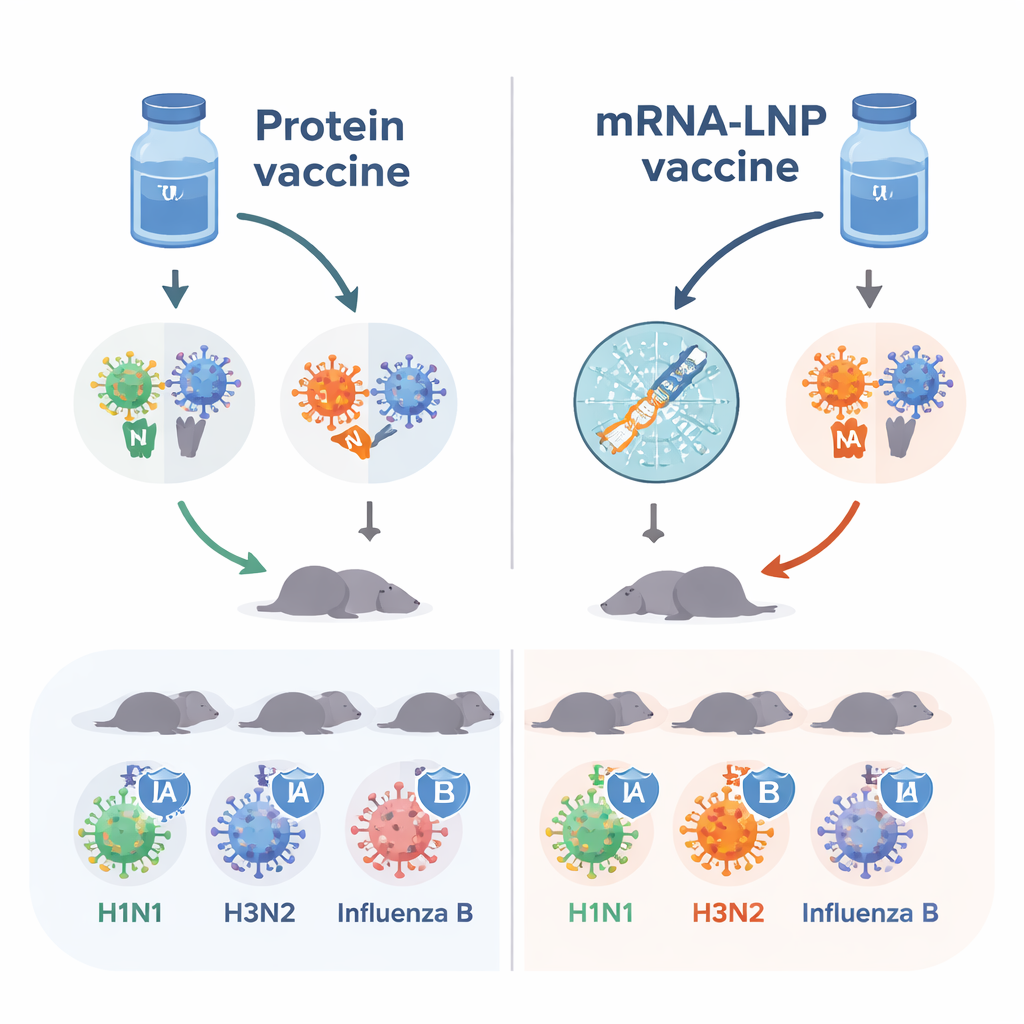
Respuestas de anticuerpos más fuertes con mRNA
Ratones vírgenes —animales que nunca habían visto virus gripales ni vacunas— recibieron dos dosis ya fuera de la vacuna de proteínas o de la versión mRNA-LNP. El equipo midió anticuerpos que reconocen HA y NA en la sangre. Ambas vacunas generaron respuestas útiles, pero las inyecciones de mRNA-LNP produjeron de forma consistente niveles más altos de anticuerpos contra la mayoría de los componentes HA y NA. En particular, los anticuerpos que bloquean la actividad de la NA, que se sabe contribuyen de manera independiente a la protección, fueron generalmente más fuertes tras la vacunación con mRNA-LNP. Estos hallazgos sugieren que, al menos en este modelo animal, la plataforma de mRNA hace que los mismos objetivos virales sean más visibles para el sistema inmunitario.
Protección frente a cepas coincidentes y actuales
La prueba real fue si estas vacunas podían salvar a los ratones de enfermedad grave. A dosis escaladas para ser similares a una dosis humana, ambos formatos de vacuna protegieron por completo a los animales frente a infecciones letales con virus H1N1 y de influenza B que coincidían estrechamente con los componentes de la vacuna, así como frente a virus tipo H3N2 diseñados cuando las cepas humanas estándar no enferman a los ratones. Los ratones vacunados mantuvieron su peso corporal y sobrevivieron, mientras que los animales no vacunados perdieron peso y a menudo murieron. Para estas cepas estrechamente relacionadas, las vacunas tradicionales de proteínas y las de mRNA-LNP tuvieron un comportamiento similar en términos de supervivencia, aunque los detalles de los anticuerpos diferían.
Ventaja frente a virus gripales antiguos y no coincidientes
Donde el enfoque mRNA-LNP destacó fue en pruebas más exigentes de “desajuste”. Los investigadores desafiaron a ratones vacunados con cepas históricas de H3N2 de 1968, 1975 y 1982 —virus que difieren de las cepas modernas que la vacuna pretendía imitar. Todos los ratones no vacunados y la mayoría de los animales tratados con vacunas de proteínas murieron, pero todos los ratones que habían recibido la vacuna octavalente mRNA-LNP sobrevivieron, aunque aún mostraron signos de enfermedad. Esta ventaja en supervivencia persistió casi un año después de la vacunación, indicando una protección duradera. Cuando el equipo transfirió suero sanguíneo de animales vacunados a ratones no vacunados, solo el suero que contenía anticuerpos generados por las vacunas mRNA-LNP contra la HA protegió contra la muerte por un virus no coincidente, lo que apunta a los anticuerpos HA cruz-reactivos como un factor clave.
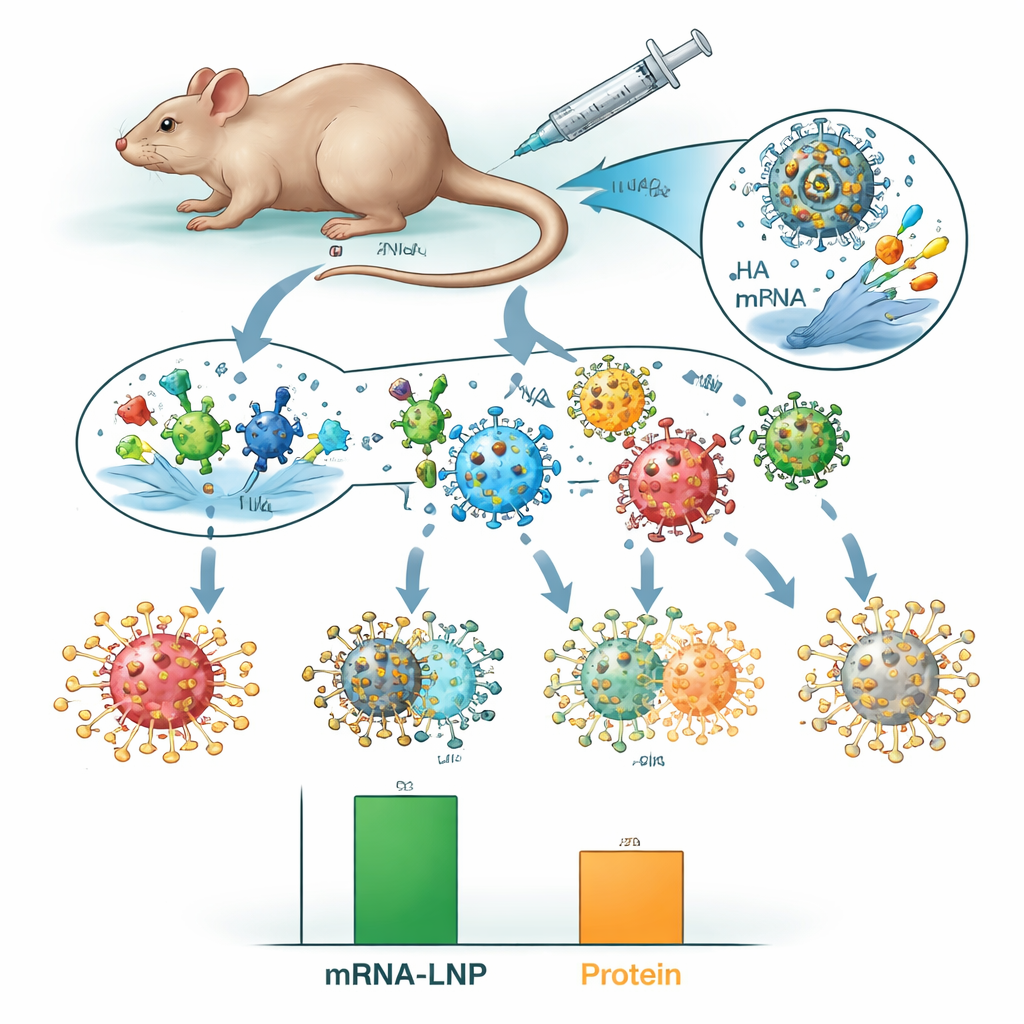
Qué significa esto para las futuras vacunas antigripales
Para un público no especialista, el mensaje es que ambos estilos de vacuna protegieron a los ratones contra los tipos de cepas gripales para las que fueron diseñadas, pero la versión mRNA-LNP también ofreció una protección más amplia y duradera frente a virus antiguos y desactualizados. Al incluir ambas proteínas principales de la superficie viral y usar mRNA para presentarlas al sistema inmune, esta estrategia podría ayudar a reducir la diferencia entre temporadas de gripe efectivas y menos efectivas. Aunque los resultados en ratones no garantizan éxito en humanos, y adyuvantes más potentes podrían todavía mejorar las vacunas de proteínas, el trabajo respalda la idea de que vacunas antigripales multicomponentes basadas en mRNA podrían algún día ofrecer una protección más fiable frente a un rango más amplio de cepas de influenza circulantes y emergentes.
Cita: Catani, J.P.P., Smet, A., Ysenbaert, T. et al. Immunogenicity and protection of octavalent influenza vaccine candidates using adjuvanted proteins or mRNA-LNPs in naïve mice. npj Vaccines 11, 57 (2026). https://doi.org/10.1038/s41541-026-01378-z
Palabras clave: vacuna contra la gripe, mRNA-LNP, hemaglutinina, neuraminidasa, protección cruzada