Clear Sky Science · es
Rentabilidad de las estrategias de vacuna materna y/o anticuerpo monoclonal frente al virus respiratorio sincitial en lactantes belgas
Por qué importa esto a los padres y a los planificadores sanitarios
Cada invierno, un virus común llamado VRS (virus respiratorio sincitial) lleva a miles de niños pequeños belgas al hospital. Nuevas herramientas prometen proteger a los bebés durante sus primeros meses de vida, cuando son más frágiles: una vacuna administrada a mujeres embarazadas y anticuerpos de larga duración administrados directamente a los lactantes. Este estudio plantea una pregunta sencilla pero crucial para las familias y los contribuyentes: dado su beneficio y su elevado precio, ¿cuál de estas opciones ofrece los mejores resultados en salud por el dinero gastado en Bélgica?
El peso oculto de un virus invernal
Antes de introducir cualquier protección nueva, el VRS ya provoca una carga considerable en los niños belgas menores de cinco años. Siguiendo una cohorte anual de recién nacidos durante cinco años, los investigadores estiman alrededor de 116.000 episodios de VRS, incluidos muchos casos leves en casa y decenas de miles de consultas médicas. Los problemas más graves se concentran en los más pequeños: los bebés menores de tres meses presentan las probabilidades más altas de hospitalización o de necesitar cuidados intensivos. Cada año, el VRS se asocia con unas 8.600 hospitalizaciones ordinarias, más de 400 ingresos en cuidados intensivos y alrededor de cinco muertes, con un coste para el sistema sanitario de aproximadamente 43 millones de euros y casi 1.000 años de vida saludable perdidos cuando se consideran tanto la enfermedad como las muertes prematuras.
Nuevas formas de proteger a los bebés más pequeños
Bélgica ha empezado a disponer recientemente de dos nuevas formas de prevenir el VRS grave en lactantes. Una vacuna materna se administra en la última etapa del embarazo para que los anticuerpos protectores atraviesen la placenta y cubran los primeros meses tras el nacimiento. Un anticuerpo monoclonal de larga acción, nirsevimab, se administra al bebé en una única inyección y bloquea directamente el virus. El equipo comparó varios diseños de programas realistas: vacunar a las embarazadas todo el año o solo las gestaciones cuya fecha probable de parto cae en la temporada de VRS; administrar nirsevimab únicamente a los bebés nacidos en temporada o también a los nacidos antes mediante una gran ronda de puesta al día; y un enfoque combinado que ofrece ambas herramientas en distintas circunstancias. Supusieron que la vacuna materna alcanzaría a menos familias (40% de cobertura) que nirsevimab (90%), reflejando la adopción habitual de vacunas en el embarazo y de vacunas infantiles en Bélgica.
Ganancias en salud frente a los precios de los programas
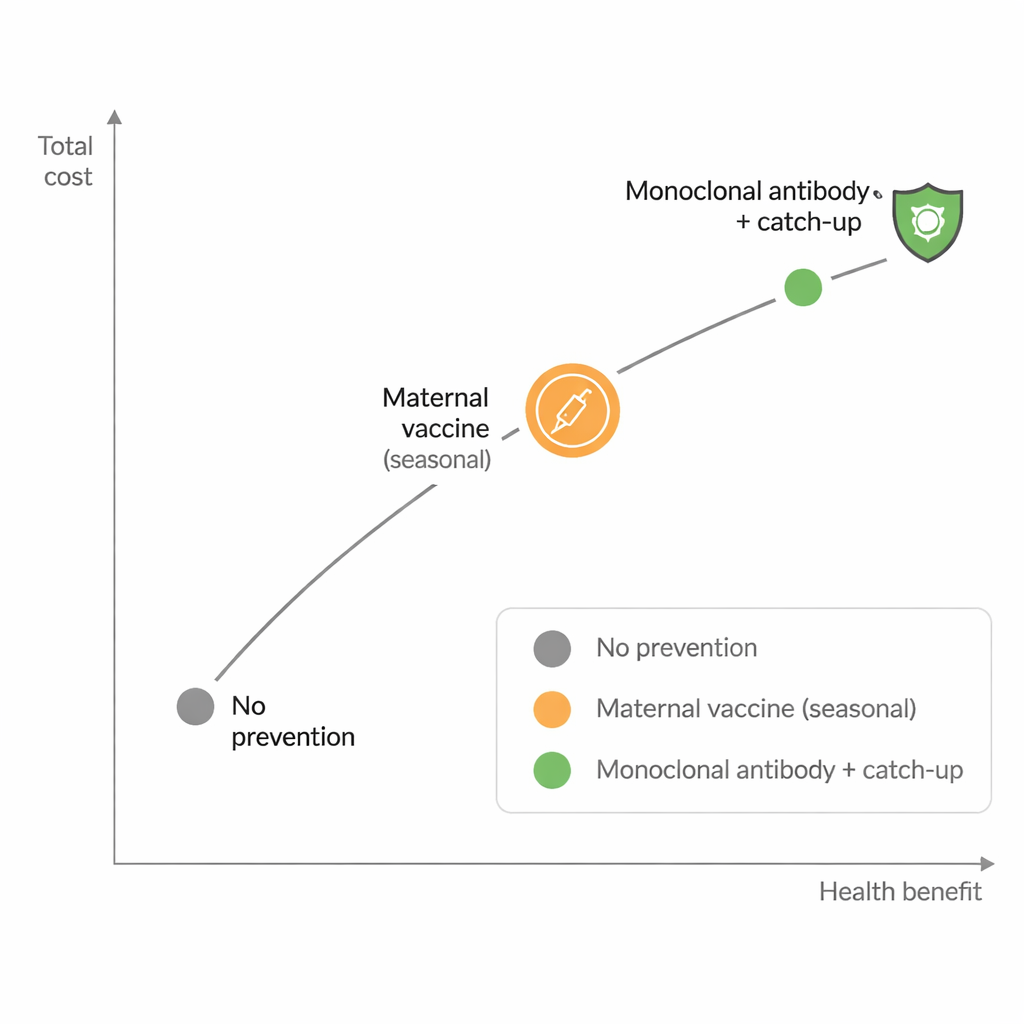
El plan de nirsevimab más amplio —protegiendo a los bebés nacidos durante la temporada de VRS y alcanzando a los nacidos justo antes de ella— previno con diferencia más enfermedad, evitando casi 20.000 infecciones y ganando más de 200 años adicionales de vida saludable en lactantes, a la vez que ahorró alrededor de 19 millones de euros en costes de tratamiento. La vacunación materna estacional fue menos potente, previniendo algo más de 3.000 casos y ganando 47 años de vida saludable con la cobertura asumida del 40%. Sin embargo, los propios programas de prevención son caros. A los precios públicos actuales en Bélgica (unos 186 € por dosis de vacuna materna y casi 778 € por dosis de nirsevimab), nirsevimab estacional con puesta al día costaría aproximadamente 76 millones de euros implementarlo, frente a unos 5 millones para la vacuna materna estacional.
¿Cuándo merece la pena pagar por una opción?
Para valorar la relación coste‑beneficio, los autores usaron métodos económicos sanitarios estándar que comparan el coste adicional con el beneficio adicional en salud, expresado como coste por año adicional de vida saludable ganado. Desde la perspectiva del pagador sanitario y usando los precios públicos actuales, solo la estrategia de vacunación materna estacional se mantuvo por debajo de los umbrales informales comúnmente usados en Bélgica (menos de 50.000 € por año de vida saludable). Las estrategias con nirsevimab, a pesar de ser más eficaces, resultaron demasiado costosas por unidad de salud ganada. Cuando los investigadores exploraron un escenario en el que ambos productos costaran 200 € por dosis, la situación cambió: nirsevimab estacional, especialmente con puesta al día, se volvió muy atractiva e incluso podría acercarse a ser coste‑ahorradora, porque el coste extra del programa se compensaba con menos hospitalizaciones. Un análisis bidimensional de precios mostró exactamente qué combinaciones de precios de la vacuna materna y de nirsevimab harían que cada estrategia fuera la preferida a distintos niveles de disposición a pagar.
Qué implica esto para la futura protección frente al VRS
Por ahora, el estudio sugiere que, a los precios públicos actuales, un programa de vacunación materna estacional dirigido es la única opción claramente coste‑efectiva en Bélgica, aunque nirsevimab prevenga más enfermedad. Si el precio real de compra de nirsevimab fuera mucho menor que el precio público, o si se confirmaran beneficios fuertes a largo plazo, como la reducción de sibilancias y asma, los amplios programas de anticuerpos infantiles también podrían resultar una buena inversión. El análisis muestra además que los resultados son muy sensibles a cuántas hospitalizaciones por VRS ocurren realmente y a la efectividad de cada producto para prevenirlas. En términos prácticos, Bélgica puede afirmar con seguridad que proteger a los lactantes contra el VRS merece la pena, pero aprovechar al máximo estas nuevas herramientas dependerá de duras negociaciones de precio, un diseño de programas cuidadoso y un seguimiento continuado de la frecuencia de hospitalizaciones infantiles y del rendimiento real de las intervenciones.
Cita: Li, X., Willem, L., Roberfroid, D. et al. Cost-effectiveness of maternal vaccine and/or monoclonal antibody strategies against respiratory syncytial virus in Belgian infants. npj Vaccines 11, 52 (2026). https://doi.org/10.1038/s41541-026-01372-5
Palabras clave: virus respiratorio sincitial, inmunización infantil, vacunación materna, anticuerpos monoclonales, economía de la salud