Clear Sky Science · es
Desarrollo de un modelo severo de síndrome de realimentación en ratas y modelado matemático de la hipofosfatemia asociada
Por qué volver a comer puede ser peligroso
Cuando personas que han estado gravemente desnutridas reciben finalmente alimentos o nutrición intravenosa, los médicos deben actuar con cautela. Una avalancha súbita de calorías puede desencadenar el “síndrome de realimentación”, una complicación que altera los electrolitos y puede dañar el corazón, los músculos y los pulmones. Un protagonista clave es el fósforo, un mineral necesario para la energía en todas las células. Este estudio utilizó ratas y modelado por ordenador para descubrir por qué el fósforo en la sangre puede desplomarse tan dramáticamente durante la realimentación y cómo podríamos prevenir mejor esta caída peligrosa.
Una mirada más cercana a los problemas de la realimentación
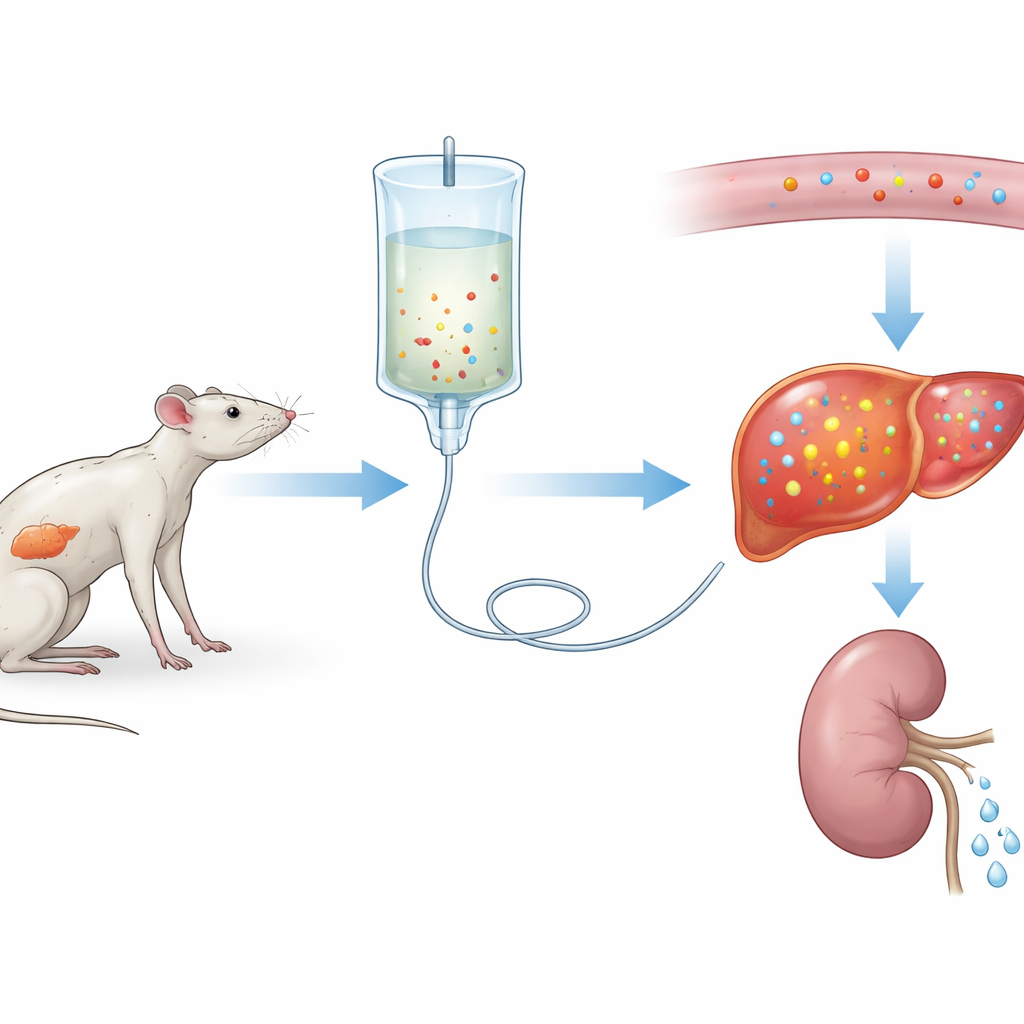
Los investigadores primero crearon una versión severa del síndrome de realimentación en ratas. Durante tres semanas, un grupo comió una dieta normal mientras otro recibió muy poca proteína, imitando la desnutrición prolongada. Ambos grupos recibieron luego la misma nutrición intravenosa durante tres días. Las ratas con dieta baja en proteínas mostraron una caída pronunciada del fósforo en sangre —aproximadamente un 75%— junto con cambios en otros electrolitos y signos de lesión orgánica, especialmente en el hígado y los músculos. Estas alteraciones se asemejaban al síndrome de realimentación grave en pacientes, lo que sugiere que el equipo había construido un modelo experimental fiel.
Qué ocurre con el fósforo durante la realimentación
Para entender cómo se mueve el fósforo en el organismo a lo largo del tiempo, los científicos tomaron muestras repetidas de sangre y orina de las mismas ratas. Encontraron que los niveles sanguíneos de fósforo caían tanto en animales normales como en los desnutridos tras el inicio de la alimentación, pero la caída fue mucho más profunda y prolongada en el grupo subalimentado. Sorprendentemente, los riñones redujeron la pérdida de fósforo en la orina inmediatamente después de la realimentación, por lo que el mineral no se estaba eliminando. En cambio, el fósforo era atraído desde el torrente sanguíneo hacia los tejidos, particularmente el hígado, cuyos depósitos se habían agotado tras semanas de dieta deficitaria. Cálculos por ordenador confirmaron que las ratas desnutridas empezaron con mucho menos fósforo dentro de sus células y luego lo absorbieron de forma agresiva una vez que llegaron los nutrientes.
La insulina no lo explica todo
Como la realimentación eleva la glucemia y la hormona insulina, los médicos han culpado durante mucho tiempo a la insulina de impulsar el fósforo hacia las células. El equipo puso a prueba esta idea atenuando la liberación de insulina con la hormona somatostatina. Como era de esperar, la glucemia subió, pero la caída del fósforo sanguíneo apenas mejoró. Al mismo tiempo, aumentaron los niveles de aminoácidos libres —los bloques de construcción de las proteínas—. En un experimento aparte, los científicos retiraron los aminoácidos de la infusión. Entonces, los niveles de fósforo se mantuvieron mucho más estables y se evitó la caída severa, aunque los niveles de insulina fueron similares. Estos resultados apuntan a un efecto combinado: tanto la insulina como los aminoácidos, no solo la insulina, estimulan a las células a captar fósforo adicional durante la realimentación.
Una red de control oculta en hígado y riñón
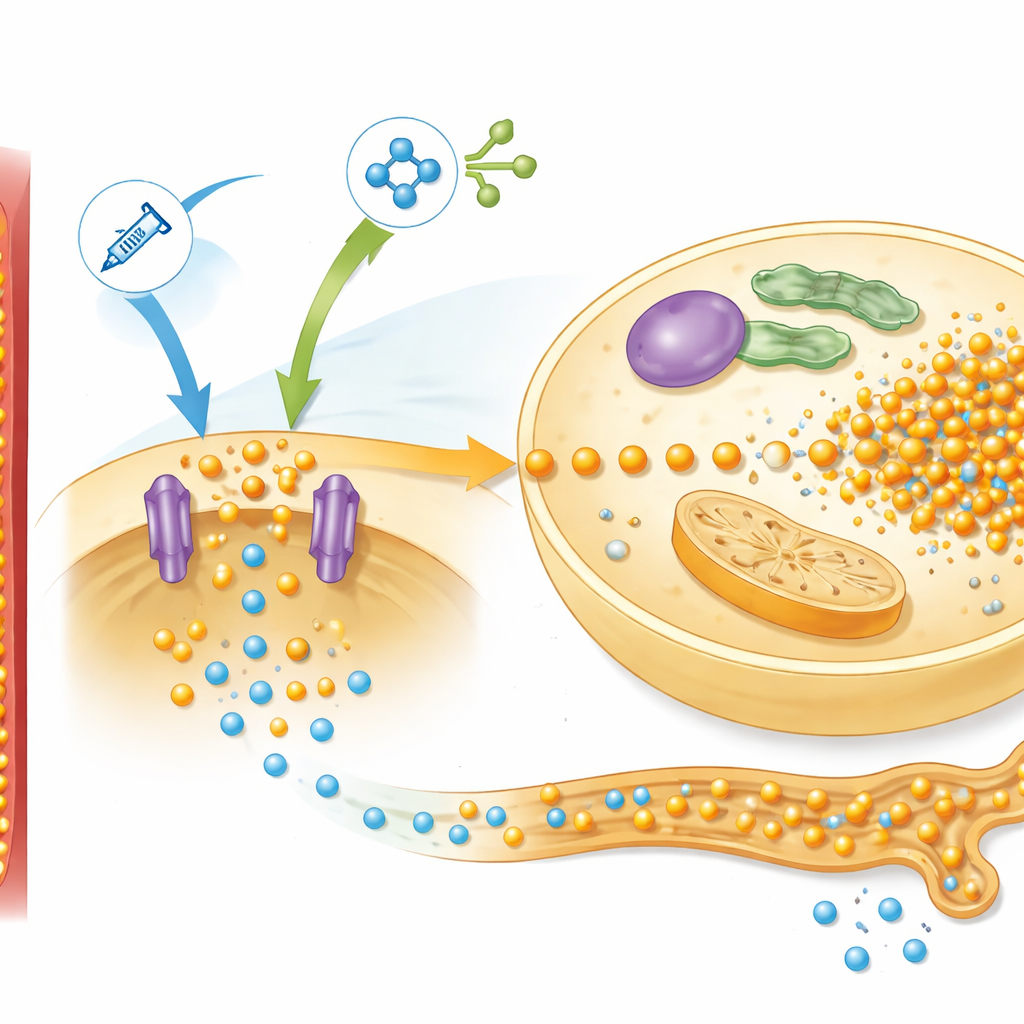
Profundizando, los investigadores examinaron proteínas hepáticas implicadas en la detección de nutrientes, centrándose en una vía conocida como mTOR, que responde a insulina y aminoácidos. En las ratas con baja proteína, la realimentación activó fuertemente esta vía e incrementó los niveles de un transportador de fosfato llamado Pit2, que ayuda a las células hepáticas a captar fósforo. El patrón coincidió con el comportamiento predicho por su modelo matemático, que agrupó esta red en una única señal de control que llamaron “simTOR”. El modelo también requirió un factor de retroalimentación separado para explicar cómo los riñones ajustan la pérdida de fósforo en la orina. Las mediciones de una hormona derivada del hueso, FGF-23, encajaron bien en este papel: sus niveles se desplomaron al comenzar la alimentación, limitando la excreción de fósforo, y luego diver-gieron entre ratas normales y desnutridas de una manera que reflejaba la señal de retroalimentación simulada.
Usar las matemáticas para probar estrategias de prevención
Al ajustar distintos mandos en su modelo por ordenador, los autores pudieron plantear preguntas de “qué pasaría si” que serían difíciles o riesgosas de testar directamente en pacientes. El análisis destacó tres influencias principales sobre la profundidad y recuperación de la caída de fósforo: el fósforo intracelular inicial, la fuerza del sistema de captación impulsado por mTOR y la tasa de aporte de fósforo desde la nutrición. Las simulaciones sugirieron que añadir una gran cantidad de fosfato en el momento de la realimentación sería difícil de equilibrar de forma segura. Sin embargo, administrar fósforo adicional antes de la realimentación —permitiendo que los órganos reconstruyan tranquilamente sus reservas internas— podría atenuar la posterior caída en los niveles sanguíneos. Reducir la carga de aminoácidos, especialmente aquellos que activan fuertemente mTOR e insulina, también pareció protector en los experimentos animales.
Qué significa esto para los pacientes
Para personas en riesgo de síndrome de realimentación —como quienes tienen trastornos alimentarios de larga duración o fragilidad severa— este trabajo sugiere que el peligro proviene de algo más que un pico de glucemia. Los órganos hambrientos inician la realimentación con los depósitos de fósforo vacíos y, bajo el empuje combinado de insulina y aminoácidos, absorben rápidamente el mineral desde la sangre mientras los riñones lo retienen temporalmente. El resultado es una escasez marcada y transitoria en la circulación que puede dañar tejidos vitales. El modelo en ratas y el marco matemático desarrollados aquí apuntan a una prevención más específica: uso cauteloso temprano de suplementos de fósforo, control cuidadoso de la nutrición rica en aminoácidos y atención a las hormonas que regulan la excreción renal. En conjunto, estos enfoques pueden ayudar a que los clínicos alimenten con más seguridad a los pacientes vulnerables.
Cita: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
Palabras clave: síndrome de realimentación, hipofosfatemia, metabolismo del fósforo, señalización mTOR, nutrición parenteral