Clear Sky Science · es
El FBA espacial revela nichos de Warburg heterogéneos en tumores renales y consumo de lactato en el cáncer colorrectal
Por qué importa el metabolismo tumoral en el espacio
Las células cancerosas no se comportan todas igual, ni siquiera dentro de un mismo tumor. Unas viven cerca de vasos sanguíneos, otras en regiones mal nutridas, y esas ubicaciones condicionan cómo obtienen y usan combustible. Este estudio presenta una nueva forma de leer ese “mapa metabólico” oculto a partir de datos espaciales de expresión génica de última generación. Al hacerlo, los autores descubren patrones sorprendentes en cómo distintos tumores manejan una molécula clave, el lactato, desafiando la visión clásica de que los cánceres solo expulsan lactato como residuo.
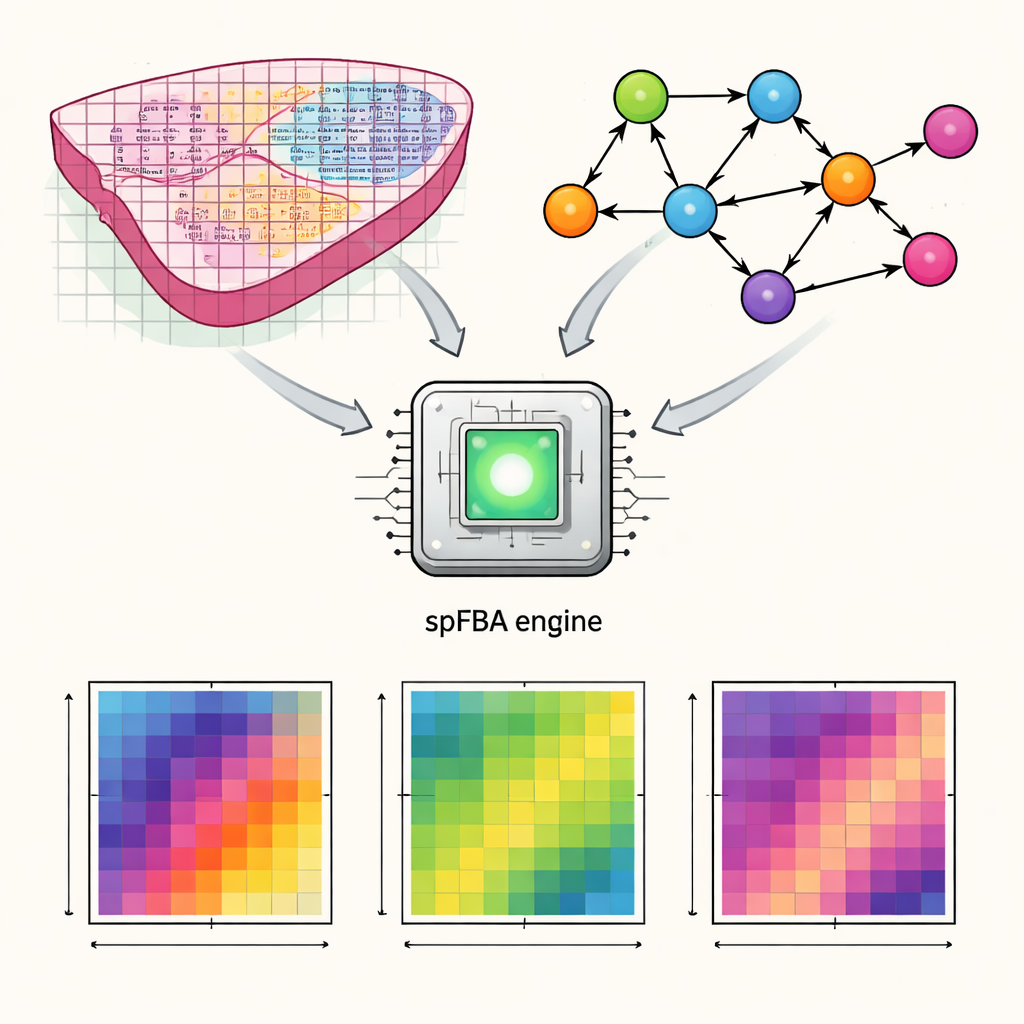
Transformar mapas génicos en actividad metabólica
Los autores desarrollaron un marco computacional llamado análisis de balance de flujos espacial, o spFBA. Las tecnologías de transcriptómica espacial miden qué genes están activos en miles de puntos diminutos a lo largo de una fina sección de tejido. spFBA combina estos mapas espaciales de actividad génica con modelos detallados del metabolismo humano, que describen cómo nutrientes como la glucosa, el oxígeno y los aminoácidos se transforman dentro de las células. En lugar de asumir que todas las regiones de un tejido persiguen el mismo objetivo metabólico, spFBA trata cada punto de forma independiente, explorando qué patrones de reacciones son posibles allí según las leyes de la química y el balance de masas. La salida es un conjunto de “puntuaciones de enriquecimiento de flujo” que indican, para cada ubicación, con qué intensidad es probable que fluyan distintas reacciones metabólicas y en qué dirección.
Probar el método en tumores renales
Para comprobar si spFBA genera resultados biológicamente coherentes, el equipo empezó por el carcinoma de células claras renales, un cáncer de riñón conocido por depender intensamente de la degradación de azúcar (glucólisis) y la liberación de lactato, un fenómeno llamado efecto Warburg. Usando datos espaciales publicados de diez muestras de tumores renales, preguntaron si los patrones metabólicos predichos coincidían con la estructura tisular conocida. Encontraron que los puntos agrupados según sus flujos metabólicos inferidos se alineaban bien con la organización histológica observada al microscopio y con los clústeres basados solo en expresión génica. De forma importante, spFBA recuperó el contraste metabólico esperado entre tumor y tejido renal normal: las regiones tumorales mostraron mayor uso de glucosa, una producción de biomasa más fuerte (un proxy del crecimiento celular) y una secreción robusta de lactato. Al mismo tiempo, el consumo de oxígeno siguió siendo sustancial, revelando que distintas partes del mismo tumor pueden mezclar fermentación y respiración según el suministro sanguíneo local.
Los cánceres colorrectales revelan otra historia del lactato
Los investigadores aplicaron luego el mismo flujo de trabajo a nuevos conjuntos de datos espaciales de alta resolución de un paciente con cáncer colorrectal primario y metástasis hepáticas emparejadas, así como a un conjunto público independiente de cáncer colorrectal generado con otra tecnología. Aquí los resultados fueron notablemente distintos. En lugar de exportar lactato como residuo, la mayoría de las regiones del cáncer colorrectal—tanto en el tumor de colon original como en las metástasis hepáticas—se predijeron que importaban lactato del entorno. Las células del estroma en el tejido de soporte cercano tendían a liberar pequeñas cantidades de lactato, mientras que las células tumorales actuaban como potentes consumidoras. Al rastrear patrones de flujo a nivel de reacción, los autores muestran que estas células metastásicas no se limitan a oxidar lactato en el ciclo energético mitocondrial habitual. Más bien, convierten el lactato en bloques de construcción que alimentan rutas para fabricar lípidos y otros componentes necesarios para el crecimiento celular, un “seudo–efecto Warburg inverso” en el que el lactato se transforma en materia prima para la biosíntesis.
Nichos metabólicos y la frontera tumor-estroma
Puesto que spFBA conserva la disposición espacial, puede localizar con precisión dónde ocurren intercambios metabólicos particulares. En tumores renales, el método reveló «vecindarios» metabólicos coexistentes: interfaces mejor oxigenadas y ricas en sangre donde las células cancerosas respiran y fermentan, y núcleos más profundos y pobremente vascularizados que dependen en mayor medida de la fermentación. En las metástasis hepáticas colorrectales, spFBA destacó contrastes agudos en la frontera entre tumor y estroma, donde la gestión de glutamato y lactato cambiaba de dirección, lo que sugiere un intercambio intenso en el frente invasivo. En todos los conjuntos de datos, los flujos predichos relacionados con el crecimiento se correlacionaron con medidas independientes basadas en genes de proliferación, lo que respalda el realismo biológico del modelo. Crucialmente, el mismo algoritmo predijo secreción de lactato en el cáncer renal pero captación de lactato en el colorrectal, indicando que las diferencias observadas provienen de los datos y no de un sesgo incorporado en el modelo.
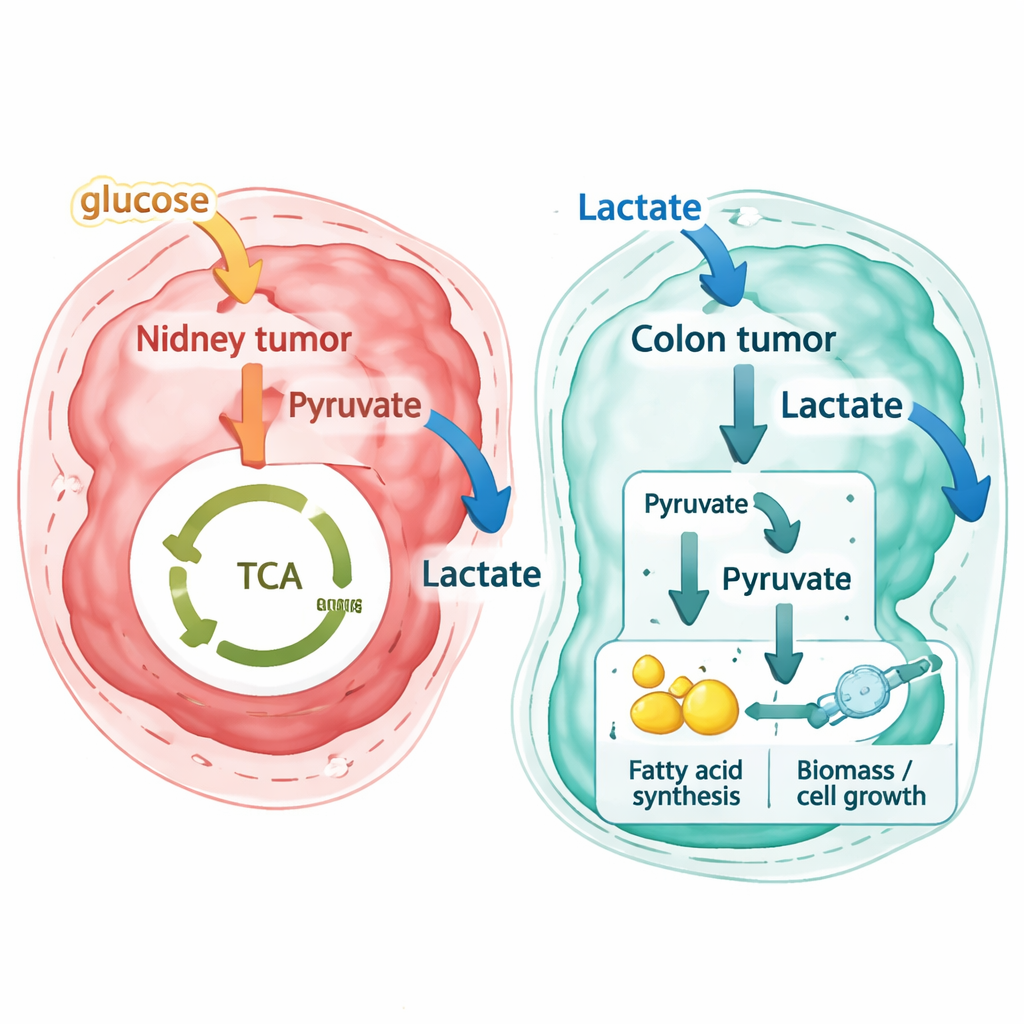
Qué significa esto para entender y tratar el cáncer
Para no especialistas, el mensaje clave es que el metabolismo del cáncer no solo es anómalo—también es altamente local. Un mismo tumor puede albergar múltiples nichos metabólicos, y tumores de aspecto similar en órganos distintos pueden usar las mismas moléculas de manera opuesta. Este trabajo muestra que al superponer la expresión génica espacial sobre modelos metabólicos detallados, los investigadores pueden inferir dónde es probable que los tumores tengan hambre de nutrientes concretos como el lactato. En el cáncer colorrectal, el descubrimiento de que las células tumorales consumen extensamente lactato y lo canalizan hacia procesos relacionados con el crecimiento plantea nuevas preguntas sobre cómo la dieta, la microbiota intestinal y el propio metabolismo hepático influyen en la progresión de la enfermedad, y si bloquear el uso de lactato podría hacer a estos tumores más vulnerables a la terapia.
Cita: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Palabras clave: metabolismo del cáncer, transcriptómica espacial, lactato, efecto Warburg, cáncer colorrectal