Clear Sky Science · es
El análisis dinámico de redes revela acoplamientos de residuos a larga distancia en la interfaz pMHC que subyacen a la mayor inmunogenicidad
Cómo pequeños fragmentos virales orientan nuestras defensas inmunitarias
Nuestras células T citotóxicas patrullan el cuerpo en busca de señales de infección o cáncer. Lo hacen examinando diminutos fragmentos proteicos, llamados péptidos, que se muestran en la superficie celular mediante moléculas conocidas como MHC de clase I. Este estudio plantea una cuestión sutil pero importante: ¿cómo puede un único pequeño cambio en uno de estos péptidos hacer que las células T respondan mucho más intensamente—o que no respondan en absoluto? La respuesta implica no solo la estructura estática, sino cómo todo el ensamblaje molecular se mueve y flexiona con el tiempo.
La cerradura, la llave y las piezas móviles
Para entender el trabajo, ayuda imaginar el complejo péptido–MHC (pMHC) como una cerradura y el receptor de células T (TCR) como una llave. El péptido se asienta en una ranura del MHC y, juntos, forman la superficie que el TCR explora. Investigaciones previas han demostrado que tanto la secuencia exacta del péptido como la variante concreta de MHC influyen fuertemente en si una célula T responde. Los científicos también han diseñado “ligandos peptídicos alterados” que incorporan pequeños cambios para ajustar las respuestas inmunitarias, incluso en inmunoterapia contra el cáncer. Pero mientras conocemos bastante sobre las formas estáticas de estos complejos, sabemos mucho menos sobre cómo los movimientos en un punto del péptido pueden afectar partes distantes de la interfaz donde el TCR realmente se une.
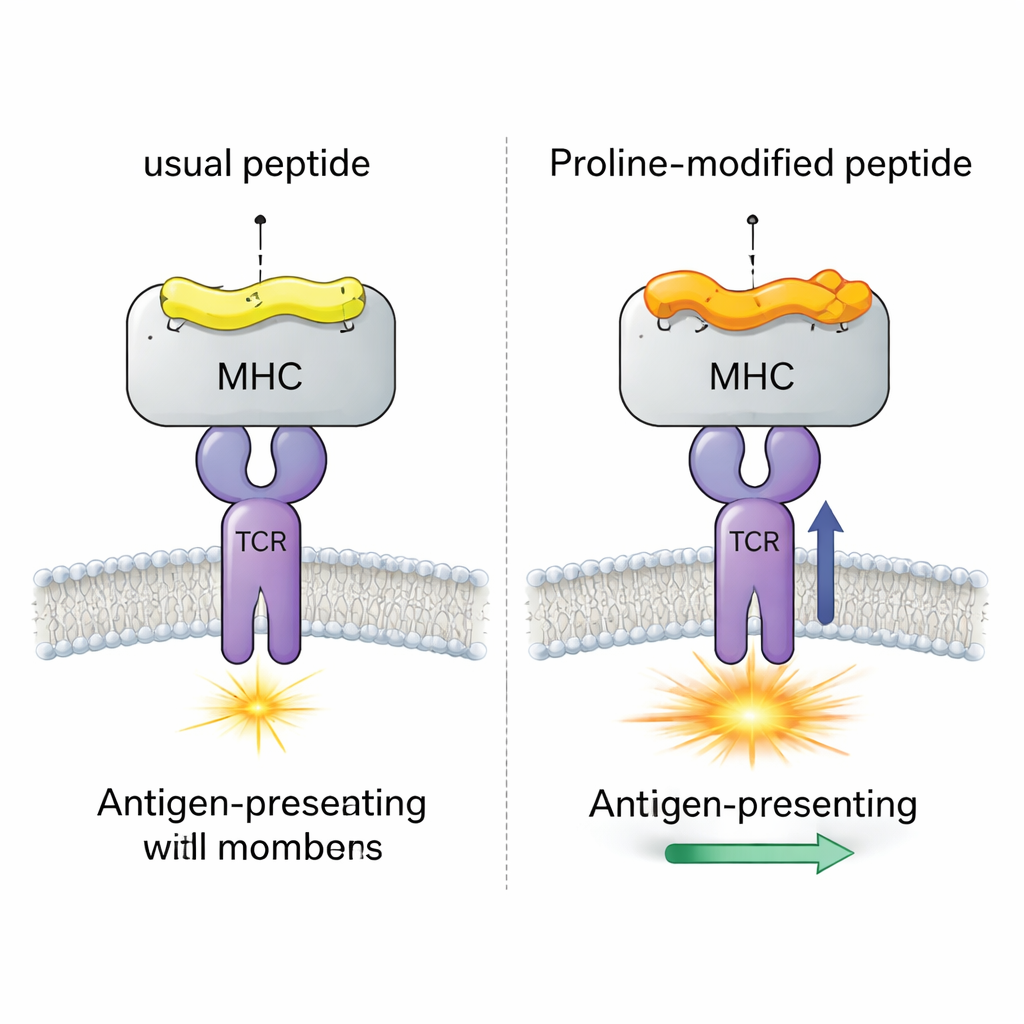
Un caso viral de prueba con cuatro péptidos casi idénticos
El equipo se centró en un sistema bien estudiado de ratón (LCMV) que implica el péptido gp33, que normalmente provoca fuertes respuestas de células T CD8+. Compararon cuatro versiones estrechamente relacionadas de este péptido, todas unidas al mismo MHC (H-2Db). Una versión es el péptido viral original; otra porta una mutación de escape inmune que las células T apenas reconocen; y dos son candidatos vacunales “alterados con prolina” donde un solo aminoácido cerca del inicio del péptido se cambia por prolina. Experimentos anteriores mostraron que este intercambio por prolina aumenta la afinidad del complejo péptido–MHC y la respuesta de un TCR modelo (llamado P14), pero el mecanismo detallado seguía siendo poco claro.
Ver a las moléculas menearse: simulaciones y cristalografía
Para descubrir qué ocurre, los autores combinaron estructuras cristalinas de alta resolución con largas simulaciones computacionales átomo por átomo de cada complejo pMHC en movimiento. Examinaron cuánto fluctúa cada residuo aminoacídico a lo largo del tiempo y cómo cambian estas fluctuaciones cuando la posición tres del péptido se convierte en prolina. Al correlacionar patrones de movimiento a través de muchas simulaciones emparejadas, construyeron un “mapa dinámico” de qué residuos se mueven juntos, incluso cuando están alejados en el espacio. Luego transformaron este mapa en una red, donde cada residuo es un nodo y las aristas representan movimientos estadísticamente vinculados, y analizaron esa red con herramientas de teoría de grafos similares a las usadas en el análisis de redes sociales.
Comunicación a larga distancia dentro de la cerradura inmunitaria
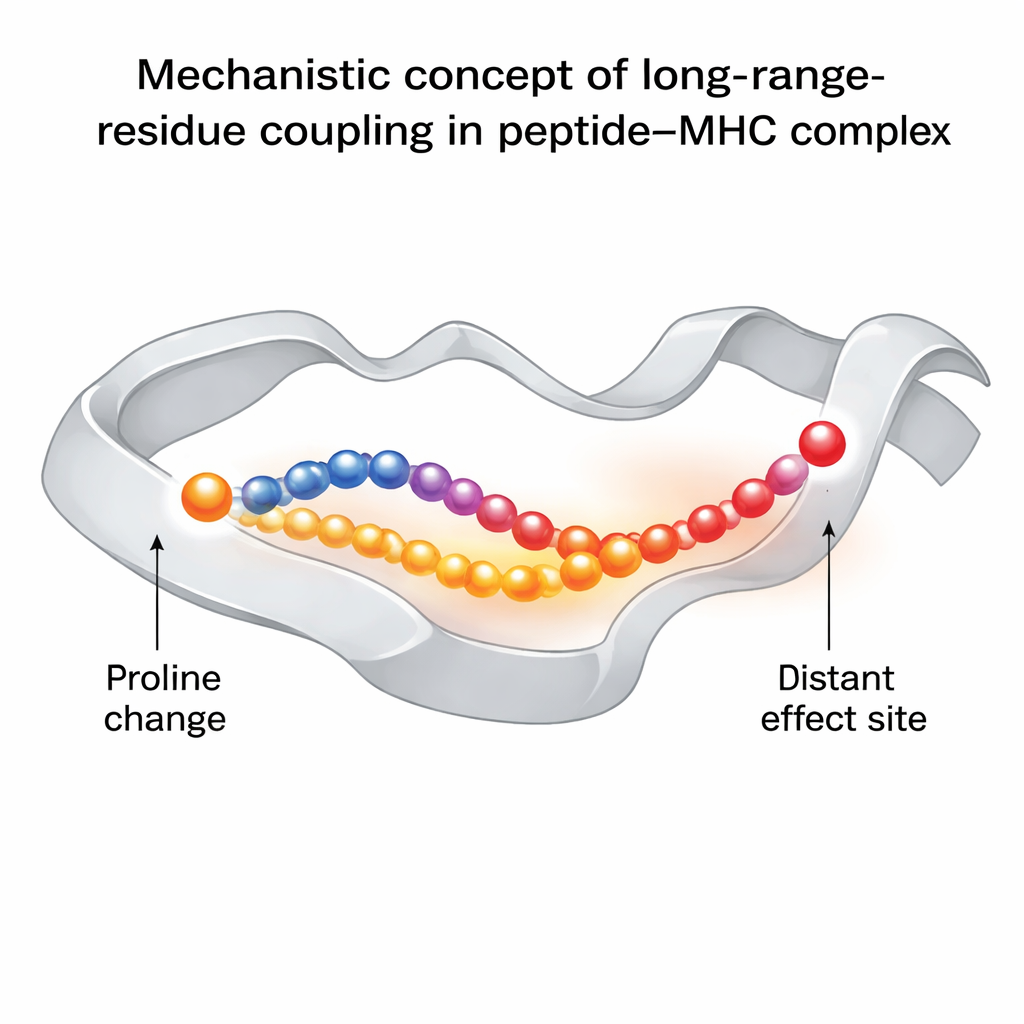
El hallazgo central es que alterar el tercer residuo del péptido por prolina hace más que simplemente endurecer ese punto local. Cambia cómo se transmite el movimiento a lo largo de una de las hélices del MHC que bordea la ranura de unión al péptido. Esto, a su vez, afecta el comportamiento de otro residuo peptídico, la posición seis, que se sitúa justo debajo de la huella del TCR y es crítico para el reconocimiento. En las versiones “buenas” modificadas con prolina, este residuo explora una gama más amplia de conformaciones, incluidas aquellas óptimas para la unión al TCR. En la variante de escape inmune sin prolina, ese residuo está más bloqueado y rara vez adopta la orientación compatible con el TCR. El análisis de red revela que esta influencia viaja a través de aminoácidos específicos en la ranura del MHC, formando una cadena de residuos dinámicamente acoplados que enlaza el sitio del cambio por prolina con la región de contacto del TCR.
Por qué esto importa para vacunas e inmunoterapia
Estos resultados muestran que la inmunogenicidad—qué tan fuertemente un péptido activa a las células T—no depende solo de si las formas encajan en un momento dado, sino también de cómo el complejo respira y se flexiona con el tiempo. Un cambio sutil en una posición puede propagarse a través de la red molecular, haciendo que los residuos clave de contacto sean más propensos a presentarse en posturas compatibles con el TCR. El flujo de trabajo computacional de los autores ofrece una forma de detectar sistemáticamente estos acoplamientos a larga distancia, lo que podría orientar el diseño de péptidos alterados para vacunas y terapias contra el cáncer. En términos sencillos, demuestran que, al elegir cuidadosamente dónde modificar un péptido, podemos empujar a toda la cerradura hacia un estado dinámico más “lista para ser abierta” por la llave del sistema inmunitario.
Cita: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
Palabras clave: Reconocimiento por células T, péptido MHC, dinámica de proteínas, ligandos peptídicos alterados, inmunogenicidad