Clear Sky Science · es
Modelado in silico de la diferenciación del endodermo del intestino anterior hacia progenitores epiteliales pulmonares
Convertir células madre en células que construyen pulmones
Los científicos están aprendiendo a inducir las propias células madre de un paciente para que se conviertan en tejido pulmonar de reemplazo, lo que algún día podría reparar daños causados por enfermedades como la EPOC, la fibrosis o infecciones graves. Este artículo explora cómo los investigadores usaron el modelado por ordenador para mapear y afinar un paso crucial en ese trayecto: transformar un tipo celular intermedio, llamado endodermo del intestino anterior, en progenitores epiteliales pulmonares tempranos —las células iniciales que pueden formar más adelante las vías respiratorias y los alvéolos del pulmón.
Por qué importan las células iniciadoras pulmonares
Las células madre pluripotentes inducidas humanas (iPSC) pueden reprogramarse a partir de tejidos adultos y luego orientarse hacia muchos órganos distintos. Para construir tejido pulmonar, estas células primero atraviesan varios puntos de control del desarrollo. Uno de ellos es el endodermo del intestino anterior, una capa que normalmente da lugar a partes del sistema respiratorio y digestivo en el embrión. A partir de ahí, con las señales químicas adecuadas, las células pueden convertirse en progenitores epiteliales pulmonares, que expresan marcadores pulmonares tempranos y pueden madurar más tarde en células especializadas de las vías aéreas o alveolares. Dado que las futuras terapias celulares requerirán miles de millones de estas células, los investigadores necesitan formas de aumentar los rendimientos de manera fiable y adaptar los protocolos a líneas celulares de distintos pacientes sin recurrir a ensayo y error constante en el laboratorio.
Construir una versión virtual de la diferenciación celular
El equipo amplió un marco matemático previo para construir lo que, según su conocimiento, es el primer modelo a nivel de población de esta transición específica del endodermo anterior a progenitores pulmonares. Consideraron dos formas de representar las células: una versión simple que sigue solo el número total de células vivas, y una versión más detallada que sigue por separado las células del endodermo anterior y los progenitores pulmonares. En ambos casos, el modelo también rastrea la glucosa y el lactato en el medio de cultivo, representando nutrientes y desechos. Usando herramientas de biología de sistemas, los investigadores construyeron muchas ecuaciones candidatas sobre cómo las células crecen, mueren y se diferencian, y luego emplearon pruebas de identificabilidad para descartar modelos cuyos parámetros nunca podrían determinarse, incluso con datos perfectos.
Diseñar experimentos más inteligentes con el modelo
En lugar de ajustarse solo a los datos disponibles, los investigadores dejaron que el modelo guiara cómo deberían realizarse nuevos experimentos. Usaron datos simulados para preguntar con qué frecuencia necesitarían medir el número de células y los niveles de nutrientes para estimar con precisión los parámetros del modelo, equilibrando la precisión estadística con el coste y el trabajo de muestreos frecuentes. Esto les llevó a un plan práctico: mediciones diarias de glucosa y lactato, y recuentos celulares cada uno o dos días, bajo cuatro condiciones que variaban la intensidad del fraccionamiento de los cultivos en el día 10 y si el medio de crecimiento se renovaba diariamente. A continuación llevaron a cabo estos experimentos, midiendo tanto la población celular total como, mediante citometría de flujo, las fracciones que seguían siendo células del endodermo o se habían convertido en progenitores pulmonares.
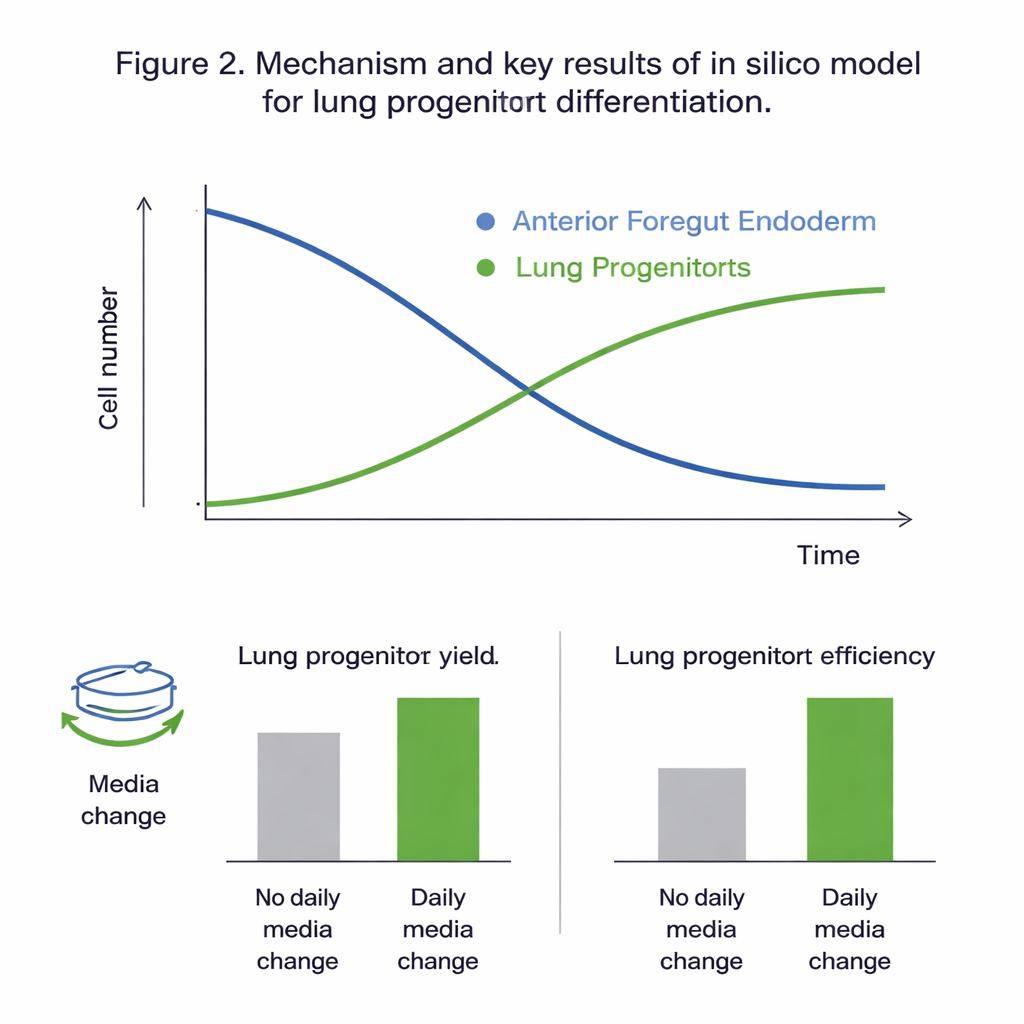
Qué revelaron los experimentos virtuales
Ajustar todos los modelos candidatos a los datos experimentales mostró que el modelo de dos poblaciones, que sigue por separado las células del endodermo y los progenitores pulmonares, podía calibrarse de forma fiable y capturaba mejor el comportamiento observado. Las comprobaciones estadísticas indicaron que, en la ventana temporal estudiada (días 11 a 15 del protocolo), la dinámica estaba impulsada principalmente por la proliferación y diferenciación de las células del endodermo, mientras que la proliferación de los propios progenitores pulmonares contribuyó poco. El análisis de sensibilidad global reforzó este panorama, destacando las tasas de crecimiento, muerte y diferenciación de las células del endodermo —y la influencia de la glucosa— como las palancas principales que controlan el resultado. El modelo calibrado reprodujo datos no vistos con errores comparables a la variabilidad natural de los experimentos, lo que sugiere que era lo bastante preciso como para explorar escenarios de «qué pasaría si» in silico.
Optimizar cambios de medio y fraccionamiento celular
Con un sistema virtual fiable en mano, el equipo probó cómo afectan dos decisiones prácticas del protocolo a los resultados: cuánto se diluye el cultivo (la proporción de fraccionamiento) en el día 10 y si el medio de crecimiento se reemplaza cada día. Las simulaciones predijeron que los cambios diarios de medio casi duplican el número de progenitores pulmonares y el rendimiento por célula inicial, principalmente al evitar el agotamiento de nutrientes y la acumulación de desechos y moléculas de señalización inestables. Los experimentos concordaron estrechamente con estas predicciones. El modelo también sugirió que usar proporciones de fraccionamiento mayores —esparcir las células más en el día 10— mejora el «rendimiento por célula de entrada» en torno a un cuarto, aunque reduce el número absoluto de células. En ambos casos, estos cambios tuvieron poco efecto sobre la proporción final de progenitores pulmonares dentro del cultivo, desplazando principalmente cuántas células podían producirse de forma eficiente.
Qué significa esto para futuras terapias pulmonares
Para un lector no especialista, el mensaje clave es que los autores han construido una especie de simulador de vuelo para un paso crítico en el crecimiento de células pulmonares a partir de células madre. Al combinar experimentos cuidadosamente diseñados con modelado matemático riguroso, muestran cómo elecciones sencillas del protocolo —como la frecuencia de cambio del medio de cultivo y la densidad de siembra— pueden influir drásticamente en cuántas células constructoras de pulmón se producen, sin alterar su calidad. Este tipo de modelado in silico puede ayudar a racionalizar futuros protocolos, reducir las conjeturas experimentales y, en última instancia, respaldar una producción más fiable y escalable de progenitores pulmonares para investigación, modelado de enfermedades y, eventualmente, terapias regenerativas.
Cita: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Palabras clave: células progenitoras pulmonares, células madre pluripotentes inducidas, modelado in silico, diferenciación celular, medicina regenerativa