Clear Sky Science · es
Asociación de alteraciones en el número de copias con el paisaje transcriptómico inmune en el cáncer
Por qué nuestros genes importan para la inmunoterapia del cáncer
La inmunoterapia contra el cáncer actúa ayudando al sistema inmune a reconocer y atacar los tumores, pero solo una minoría de pacientes obtiene un beneficio duradero. Este estudio plantea una pregunta fundamental con grandes consecuencias clínicas: ¿cómo moldea el caos genético dentro de las células tumorales —en particular, las ganancias y pérdidas extensas de ADN llamadas alteraciones en el número de copias— la reacción inmune frente al cáncer, y podemos leer esos efectos a partir de los patrones de actividad génica?
Una visión panorámica de los datos sobre cáncer
Para abordar esto, los investigadores reunieron una colección enorme de 294.159 perfiles de actividad génica procedentes de tumores y otros tejidos. Estos perfiles, tomados de varias bases de datos públicas principales, capturan qué genes están activados o silenciados en miles de muestras que abarcan muchos tipos de cáncer y condiciones experimentales. En lugar de analizar genes individuales uno por uno, el equipo empleó un método matemático para descomponer cada perfil en "componentes" subyacentes: patrones recurrentes de genes que tienden a aumentar o disminuir conjuntamente, cada uno reflejando un proceso biológico como una respuesta inmune o el efecto de un cambio en el ADN.
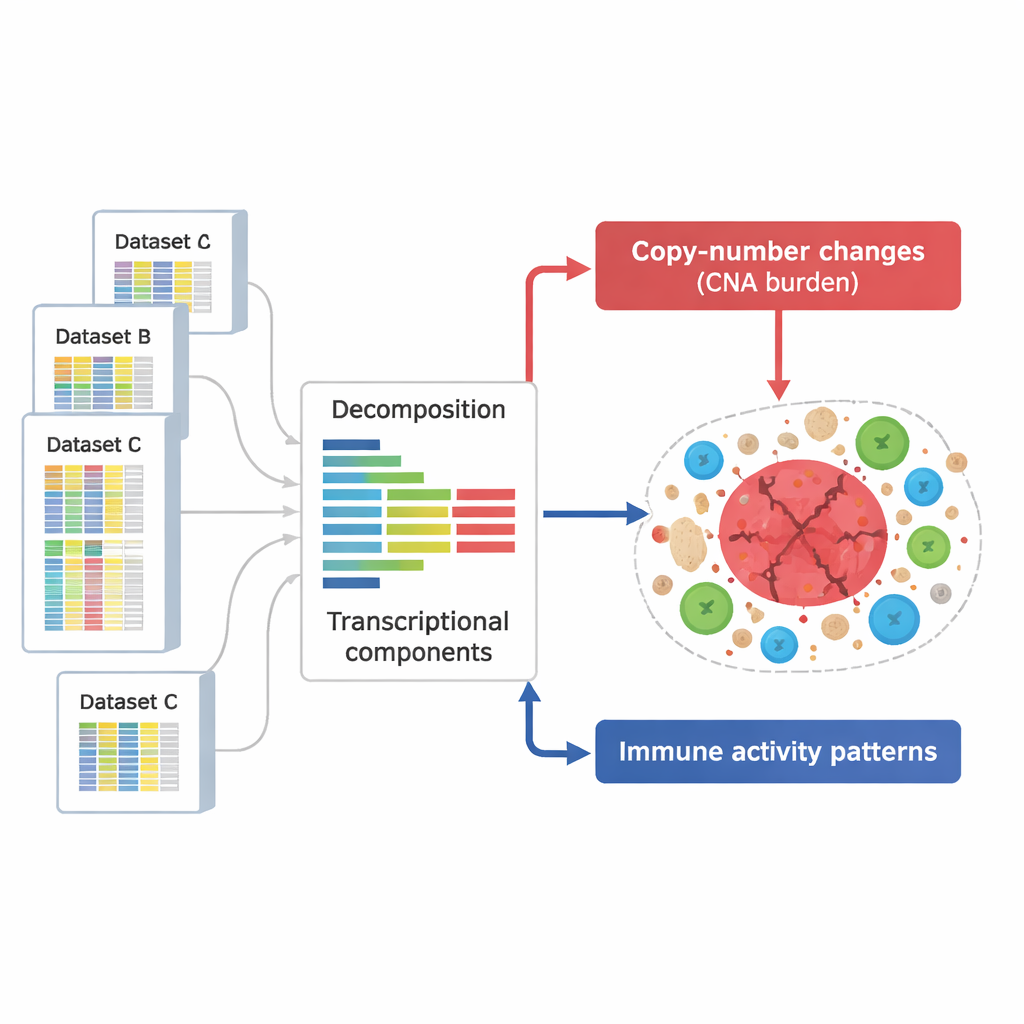
Separando las señales de daño en el ADN de las señales inmunes
A partir de estos componentes, los científicos definieron dos grupos clave. Un grupo capturó los efectos de las alteraciones en el número de copias: tramos de cromosomas que se ganan o pierden repetidamente en las células cancerosas. Estos patrones cubrieron casi todo el genoma, lo que indica que la mayoría de las regiones afectadas por tales alteraciones dejaron una huella detectable en la actividad génica. Un segundo grupo de componentes se enriqueció en genes implicados en funciones inmunes, como la activación de linfocitos T, la actividad de células asesinas naturales y la presentación de antígenos. En total, identificaron 657 componentes relacionados con el ADN y 283 componentes relacionados con la inmunidad, muchos de los cuales pudieron observarse de forma reproducible en conjuntos de datos y tecnologías independientes, lo que sugiere que representan rasgos robustos y generales de la biología tumoral.
Vinculando patrones con la respuesta al tratamiento
El equipo preguntó entonces si estos patrones relacionados con la inmunidad podrían ayudar a predecir quién responde a los inhibidores de puntos de control inmunitario, una clase importante de fármacos de inmunoterapia contra el cáncer. Usando datos de 13 estudios clínicos que abarcan 1.167 pacientes con siete tipos de cáncer, entrenaron modelos computacionales para distinguir respondedores de no respondedores basándose únicamente en la actividad de los componentes inmunes en muestras tumorales previas al tratamiento. Algunos modelos rindieron de forma sólida incluso cuando se probaron en grupos de pacientes completamente independientes; por ejemplo, un modelo entrenado en una cohorte de cáncer de mama predijo con precisión las respuestas en una cohorte separada de cáncer de mama y mostró un rendimiento útil en varios otros cánceres. Un pequeño conjunto de patrones inmunes, incluidos los vinculados a respuestas a interferón, células asesinas naturales y activación de linfocitos T, contribuyó con mayor peso a estas predicciones.
Cómo el caos genético remodela la inmunidad tumoral
Con este marco en marcha, los investigadores relacionaron sistemáticamente la carga global de alteraciones en el número de copias —una medida de hasta qué punto el ADN de un tumor está ganado o perdido— con la actividad de cada patrón inmune a lo largo de muchos tipos de cáncer. La mayoría de los patrones inmunes mostraron una relación inversa: los tumores con alta carga de alteraciones en el ADN tendían a tener menor actividad de componentes asociados a funciones inmunes beneficiosas, como la presentación de antígenos y la infiltración por células inmunes clave. Sin embargo, una minoría notable de patrones se movió en la dirección opuesta. Los tumores con alta carga de alteraciones a menudo mostraron señales aumentadas de tipos celulares inmunosupresores, incluidas células T reguladoras y ciertos macrófagos, así como células inflamatorias que pueden promover el crecimiento tumoral en lugar de su destrucción. Análisis espaciales de cortes tumorales confirmaron que las regiones con cambios amplios en el ADN coincidían con frecuencia con baja actividad de patrones inmunes útiles y con zonas “excluidas inmunológicamente” donde las células inmunes quedaban confinadas a los márgenes del tumor.
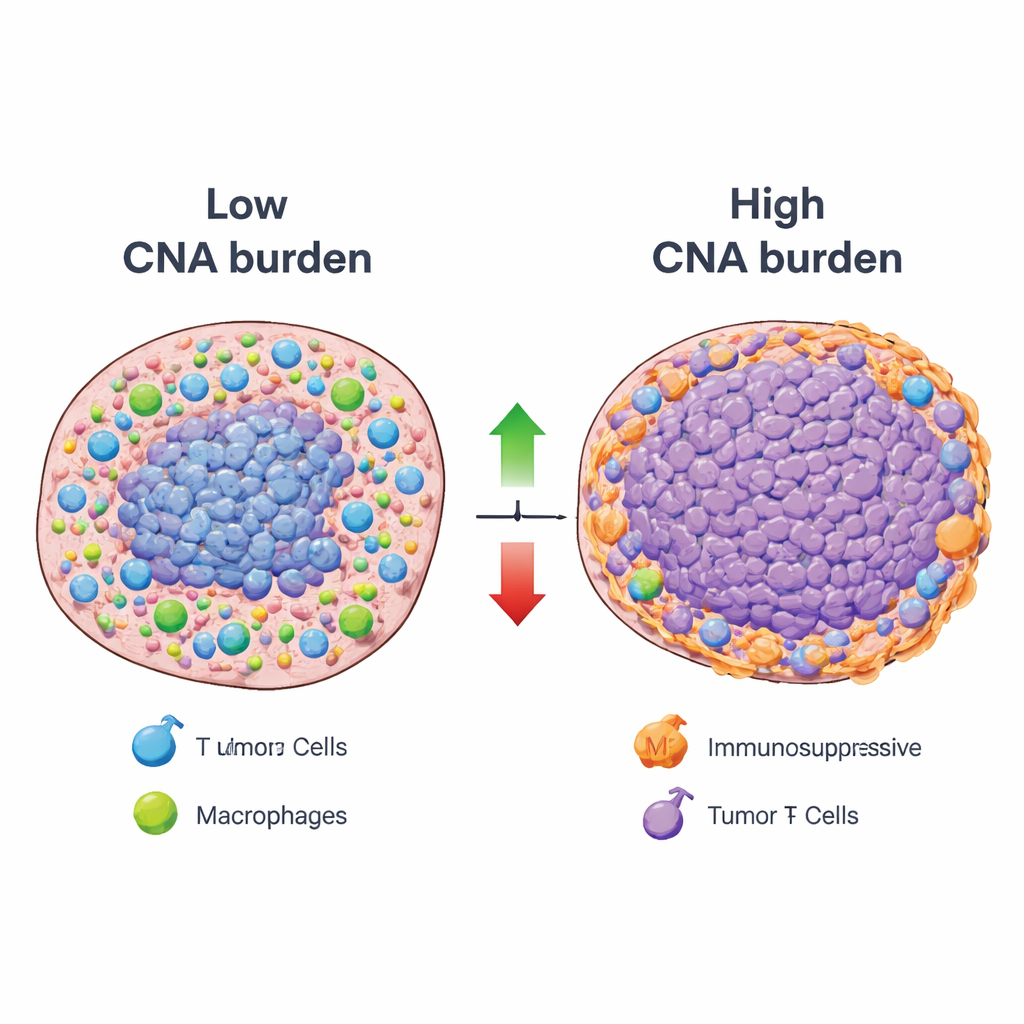
Qué significa esto para el tratamiento futuro del cáncer
En términos sencillos, el estudio muestra que los tumores cargados de ganancias y pérdidas de ADN a gran escala tienden tanto a atenuar las respuestas inmunes útiles como a fomentar ambientes inmunes supresores o promotores del tumor. Sin embargo, no son inmunológicamente mudos; en su lugar, exhiben estados inmunes específicos y recurrentes que pueden ser vulnerables a terapias dirigidas, como fármacos que bloqueen la señalización de IL-17 o IL-23 o estrategias que reprogramen determinados macrófagos. Al cartografiar estas relaciones entre ADN e inmunidad a través de los cánceres y hacer que el recurso esté disponible públicamente, el trabajo ofrece una guía detallada sobre por qué algunos tumores genéticamente inestables resisten las inmunoterapias actuales y sugiere nuevas estrategias de tratamiento combinadas para ayudar al sistema inmune a superar esa resistencia.
Cita: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
Palabras clave: inmunoterapia contra el cáncer, alteraciones en el número de copias, microambiente tumoral, inhibidores de puntos de control inmunitario, transcriptómica