Clear Sky Science · es
Control del crecimiento del glioma óptico mediado por asma a través de interacciones entre células T y microglía: un modelo matemático
Cuando los problemas respiratorios se conectan con tumores cerebrales
El asma y los tumores cerebrales parecen pertenecer a mundos distintos: uno afecta cómo respiramos, el otro cómo vemos, pensamos y nos movemos. Sin embargo, los médicos han observado un patrón desconcertante: los niños con asma parecen tener menos probabilidad de desarrollar ciertos tumores del nervio óptico. Este artículo explora cómo una enfermedad pulmonar crónica podría, inesperadamente, defender el cerebro, utilizando un modelo matemático para trazar las conversaciones químicas ocultas entre células inmunitarias y células tumorales.
Un tumor de crecimiento lento con mucho en juego
Los gliomas ópticos son tumores generalmente de crecimiento lento que se forman a lo largo del nervio óptico, con mayor frecuencia en niños con una condición genética llamada neurofibromatosis tipo 1 (NF1). Aunque estos tumores se consideran “de bajo grado”, pueden causar pérdida de visión y problemas hormonales. En la NF1, un gen defectuoso provoca que una proteína de señalización llamada RAS se vuelva hiperactiva. Esa hiperactividad activa la producción de otra molécula, midkina, que actúa como un altavoz en el nervio óptico, atrayendo células inmunitarias y remodelando el entorno local de modos que suelen ayudar al tumor en lugar de combatirlo.
Una conversación que alimenta al tumor entre nervio y células inmunes
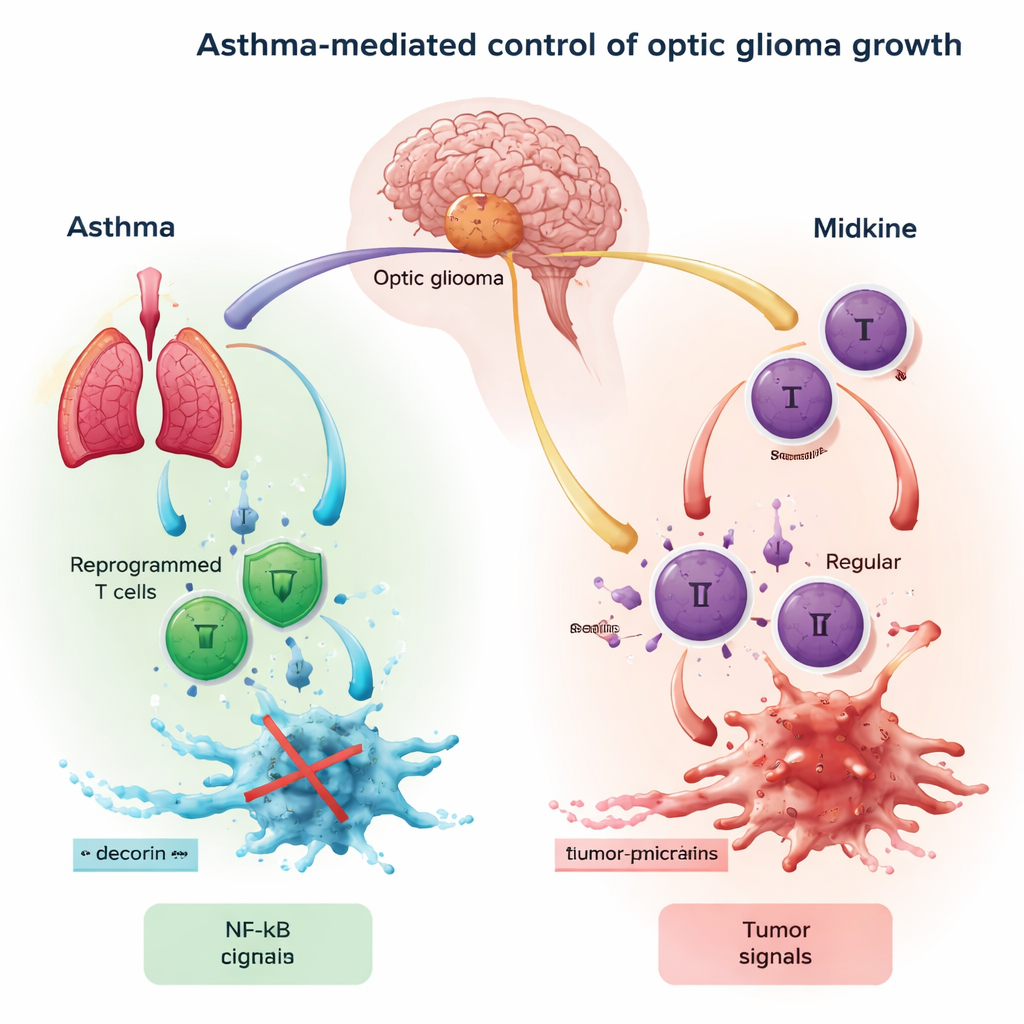
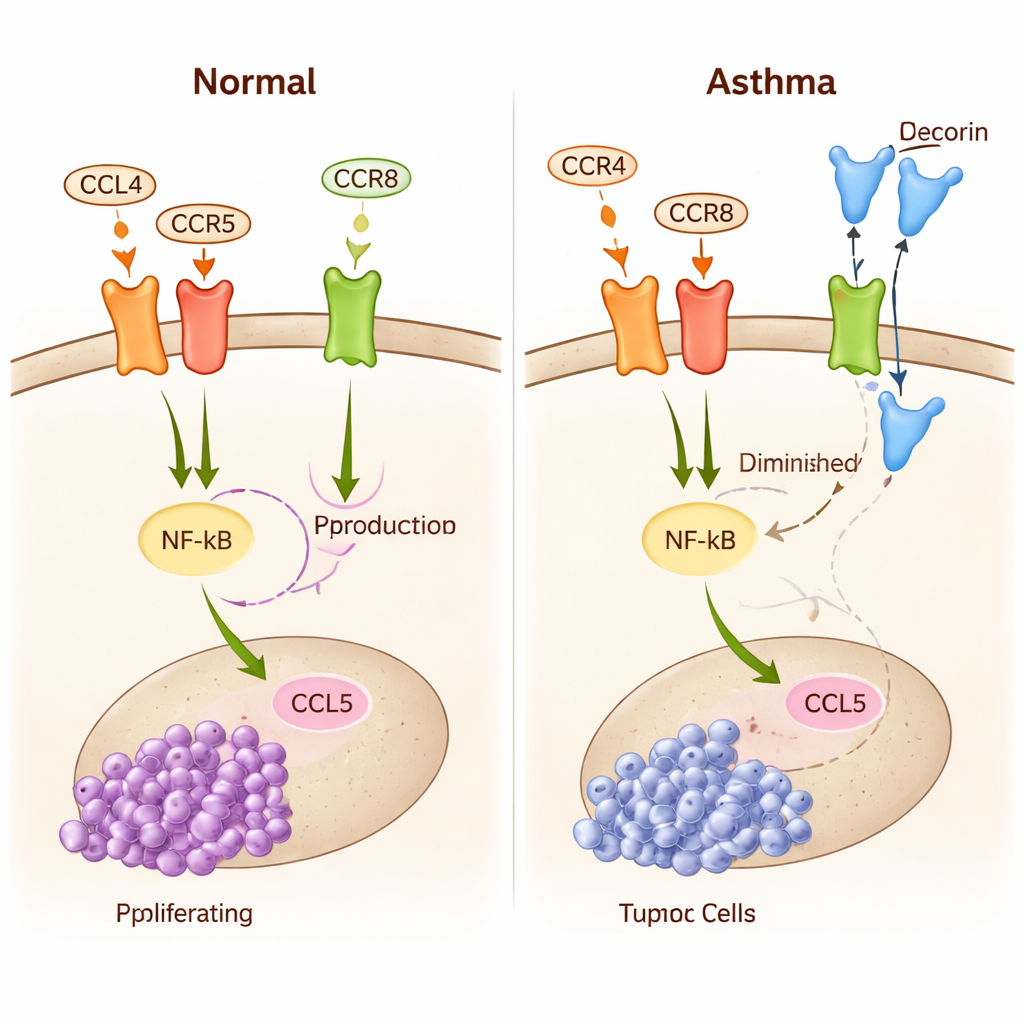
Los autores se centran en una cadena de eventos que conecta el nervio óptico, las células inmunitarias y el crecimiento tumoral. La midkina procedente del nervio óptico primero activa las células T, un tipo de glóbulo blanco, induciéndolas a liberar una señal llamada CCL4. Esa señal se une entonces a receptores (CCR5 y CCR8) en la microglía, las células inmunitarias residentes del cerebro. Cuando suficiente CCL4 se engancha a estos receptores, activa un interruptor maestro dentro de la microglía conocido como NF-κB. Una vez activado, NF-κB impulsa la producción de otra señal, CCL5, que fomenta que las células del glioma óptico crezcan, migren y evadan el ataque inmunitario. En efecto, el eje midkina–CCL4–NF-κB–CCL5 forma una señal circular de “adelante” para la expansión tumoral.
Cómo el asma reprogr ama las células T para frenar al tumor
El asma es más conocida como una enfermedad de inflamación crónica de las vías respiratorias. Pero en las personas con asma, algunas células T se “reprograman” hacia un estado distinto: pierden buena parte de su poder citotóxico directo y, en su lugar, secretan moléculas que remodelan su entorno. Una de estas moléculas es la decorina, una proteína pequeña con propiedades antitumorales reconocidas. La idea clave en este trabajo es que las células T primadas por el asma pueden viajar desde el pulmón hasta el cerebro y liberar decorina en el entorno del glioma óptico. La decorina compite con CCL4 por el receptor CCR8 en la microglía, bloqueando efectivamente parte de la conversación que alimenta al tumor y reduciendo la actividad de NF-κB y CCL5 dentro de las células inmunitarias del cerebro.
Usar las matemáticas para seguir una red invisible
Debido a que esta red de señales es demasiado compleja para entenderla solo por intuición, los investigadores construyeron un modelo matemático detallado usando ecuaciones diferenciales. El modelo sigue los niveles de moléculas clave (midkina, CCL4, decorina, NF-κB, CCL5), la actividad de los receptores en la microglía y el crecimiento de las células tumorales a lo largo del tiempo. Usaron datos experimentales para calibrar la intensidad de cada interacción y luego simularon muchos escenarios. El modelo muestra cómo pequeños cambios en la fuerza de unión—qué tan fácilmente CCL4 o la decorina se adhieren a sus receptores—pueden cambiar a la microglía entre dos modos: un estado promotor del tumor con NF-κB y CCL5 altos, y un estado supresor del tumor con fuerte unión de decorina y señales débiles de CCL4. Un índice simple basado en la proporción de receptores unidos a decorina frente a receptores unidos a CCL4 predice con precisión si el tumor tenderá a crecer o a estancarse.
Diseñar tratamientos inmunológicos más inteligentes
Más allá de explicar por qué el asma podría proteger contra el glioma óptico, el modelo se utiliza para explorar estrategias terapéuticas. Sugiere que terapias que aumenten los niveles de decorina o debiliten la afinidad de CCL4 por sus receptores podrían ralentizar el crecimiento tumoral. Los autores prueban digitalmente enfoques como infusiones repetidas de células T productoras de decorina o el uso del mensajero inmune IL-2 para expandir estas células beneficiosas dentro del organismo. Curiosamente, las simulaciones revelan que no solo importa la dosis total sino también la programación temporal de dichos tratamientos: dosis moderadas y bien espaciadas pueden mantener a la microglía en el estado supresor tan eficazmente como dosis mayores y menos frecuentes, con potencialmente menos efectos secundarios.
Qué significa esto para pacientes y familias
Para el público general, el mensaje central es que la inflamación crónica del asma, normalmente vista como perjudicial, puede a veces redefinir el sistema inmune de maneras que dificultan ciertos tumores cerebrales. Al convertir a las células T en fábricas de decorina, el asma parece inclinar la balanza en el nervio óptico desde un entorno favorable al crecimiento hacia uno más hostil para el cáncer. Si bien nadie está proponiendo el asma como terapia, los mecanismos descubiertos aquí podrían inspirar nuevos tratamientos que reproduzcan sus aspectos protectores—usando terapias con células T diseñadas o fármacos que imiten la acción bloqueadora de la decorina—para proteger a los niños en riesgo de glioma óptico.
Cita: Lee, D., Lawler, S. & Kim, Y. Asthma-mediated control of optic glioma growth via T cell-microglia interactions: A mathematical model. npj Syst Biol Appl 12, 26 (2026). https://doi.org/10.1038/s41540-026-00647-w
Palabras clave: glioma óptico, asma, decorina, células T, modelado matemático