Clear Sky Science · es
El licopeno mitiga la ferroptosis hepática inducida por la toxina T-2 al actuar sobre el eje Nrf2/mitofagia en ratones
Por qué importa una micotoxina presente en cereales cotidianos
Muchos alimentos básicos, como el trigo y el maíz, pueden estar contaminados por una micotoxina llamada toxina T-2. Este contaminante invisible sobrevive a la cocción y al procesado, y la exposición prolongada puede dañar silenciosamente órganos vitales, especialmente el hígado. El estudio resumido aquí plantea dos preguntas urgentes: ¿cómo daña exactamente la toxina T-2 al hígado, y puede un compuesto natural de los alimentos—el licopeno, el pigmento rojo presente en tomates y otras frutas—ayudar a proteger contra ese daño?
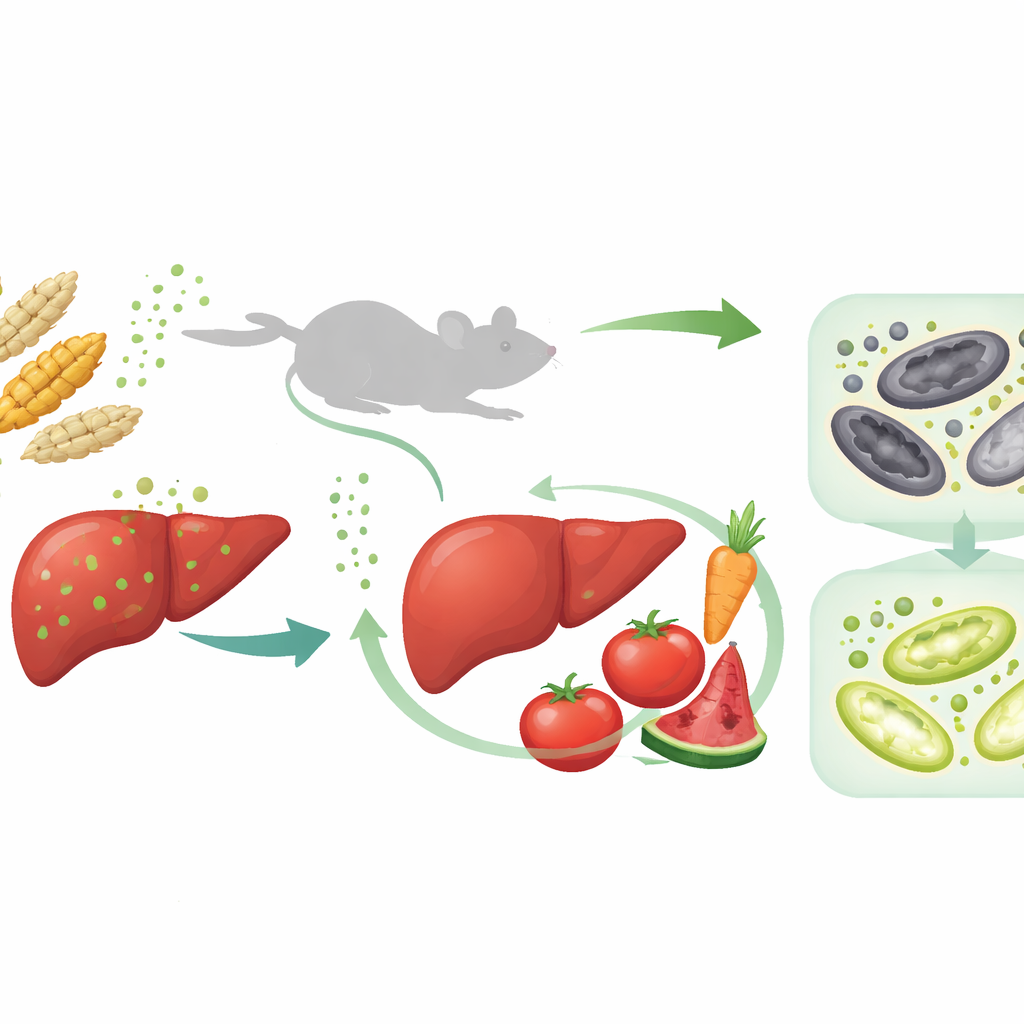
Cómo la toxina daña el hígado
Los investigadores alimentaron primero a ratones con dosis graduadas de toxina T-2 durante cuatro semanas para imitar una exposición dietética continuada. A medida que aumentaban los niveles de toxina, los animales ganaron menos peso, sus hígados se agrandaron y adquirieron un tono amarillento, y los análisis de sangre mostraron niveles crecientes de enzimas hepáticas indicativas de lesión. Al microscopio, el tejido hepático se veía edematoso y desorganizado, con vacuolas dentro de las células y signos de muerte celular. Un estudio proteómico a gran escala de las muestras hepáticas reveló que muchas de las rutas más alteradas estaban relacionadas con el manejo del hierro, el metabolismo de los lípidos y una forma específica de muerte celular llamada ferroptosis, impulsada por el hierro y la oxidación descontrolada de las grasas.
Sobrecarga de hierro y una muerte celular tipo óxido
Ahondando más, el equipo midió marcadores clásicos de la ferroptosis. En los hígados expuestos a la toxina, el contenido de hierro aumentó, mientras que las moléculas que indican daño lipídico se incrementaron y la actividad de una enzima protectora clave, GPx-4, descendió. Las proteínas que normalmente almacenan el hierro de forma segura dentro de las células se elevaron, pero el principal “exportador” de hierro en las células hepáticas disminuyó, lo que sugiere que el hierro quedaba atrapado dentro. Cuando los científicos administraron a algunos ratones un fármaco que bloquea específicamente la ferroptosis, la estructura y la función hepáticas mejoraron: la hinchazón se redujo, las puntuaciones de lesión bajaron y los indicadores químicos de daño oxidativo disminuyeron. Esto vinculó de forma clara la toxicidad hepática de la toxina T-2 con una forma de muerte celular impulsada por hierro, parecida a la oxidación o “oxidación por herrumbre”.
Mitocondrias, limpieza celular y un interruptor protector
El grupo se centró entonces en las mitocondrias, las centrales energéticas de las células, que son a la vez fuente y objetivo del estrés oxidativo. En los ratones tratados con la toxina, la producción de energía mitocondrial descendió mientras aumentaban la liberación de citocromo c y las especies reactivas de oxígeno, y la microscopia electrónica mostró mitocondrias reducidas y dañadas estructuralmente. Al mismo tiempo, el sistema de control de calidad celular—la mitofagia, un proceso selectivo de “limpieza” que elimina mitocondrias defectuosas—se activó mediante una vía que involucra las proteínas PINK1 y Parkin. Cuando los investigadores usaron ratones carentes de Parkin, y por tanto incapaces de realizar una mitofagia normal, la toxina T-2 provocó una acumulación de hierro aún mayor, señales de ferroptosis más intensas y un daño hepático más grave. Esto demostró que la mitofagia actúa como un freno protector que limita la lesión inducida por la toxina.
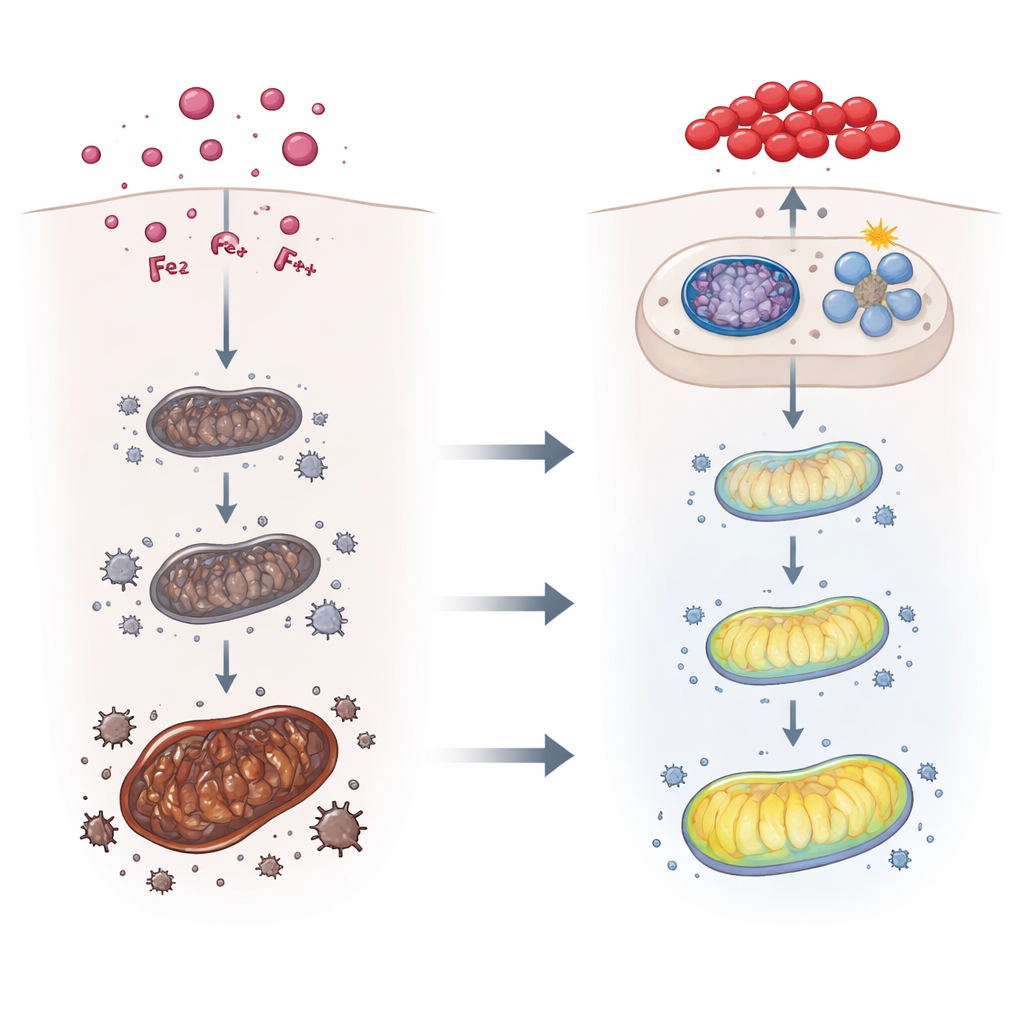
Una vía protectora interna y el papel del licopeno
Dado que el equilibrio del hierro, el estrés oxidativo y la mitofagia parecían interconectados, los autores buscaron un regulador aguas arriba y se centraron en Nrf2, un interruptor maestro que activa genes antioxidantes y de desintoxicación. La propia toxina T-2 activó parcialmente a Nrf2, pero cuando a los ratones se les administró un compuesto conocido por activar Nrf2, la exportación de hierro hepático mejoró, los marcadores de ferroptosis disminuyeron y la mitofagia aumentó, todo lo cual atenuó el impacto de la toxina. El equipo preguntó entonces si el licopeno podría actuar como un potenciador natural de Nrf2. Modelos computacionales sugirieron que el licopeno puede unirse físicamente tanto a Nrf2 como a su proteína represora Keap1 de maneras que favorecerían la activación de Nrf2. En ratones vivos, el tratamiento con licopeno antes y durante la exposición a la toxina mejoró el peso corporal, restauró la apariencia del hígado y los análisis sanguíneos, redujo la acumulación de hierro y el daño oxidativo, y activó aún más a Nrf2 y la vía mitofágica PINK1–Parkin.
Qué implica esto para la seguridad alimentaria y la dieta
En términos claros, el estudio muestra que la toxina T-2 lesiona el hígado al atrapar el exceso de hierro dentro de las células, dañar las mitocondrias y desencadenar la ferroptosis. El organismo responde activando Nrf2 y la mitofagia para eliminar mitocondrias dañadas y reequilibrar el hierro, pero esta defensa puede verse desbordada. El licopeno parece fortalecer este escudo interno, ayudando al hígado a exportar hierro, limpiar mitocondrias defectuosas y resistir la muerte celular por ferroptosis. Aunque se necesita más trabajo antes de trasladar estos hallazgos a humanos, la investigación sugiere que ciertos compuestos vegetales, como el licopeno, podrían algún día formar parte de estrategias para reducir el impacto sobre la salud de toxinas alimentarias inevitables.
Cita: Yang, X., Song, W., Lu, Z. et al. Lycopene mitigates T-2 toxin-induced hepatic ferroptosis by targeting the Nrf2/mitophagy axis in mice. npj Sci Food 10, 94 (2026). https://doi.org/10.1038/s41538-026-00736-4
Palabras clave: toxina T-2, licopeno, lesión hepática, ferroptosis, mitofagia