Clear Sky Science · es
Terapia dual con células derivadas del tejido adiposo potencia la arteriogénesis y la preservación de las extremidades mediante la integración vascular en la isquemia crítica de extremidades
Salvar piernas haciendo crecer nuevos vasos sanguíneos
Cuando las arterias de las piernas se obstruyen gradualmente, las personas pueden sufrir dolores incapacitantes, úlceras persistentes e incluso enfrentarse a la amputación. Esta fase grave, llamada isquemia crítica de extremidades, es notoriamente difícil de tratar porque muchos pacientes no pueden someterse a bypass u otros procedimientos estándar. El estudio resumido aquí explora una estrategia nueva: usar dos tipos de células con propiedades similares a las madre, extraídas de la propia grasa del paciente, para ayudar al cuerpo a generar vasos sanguíneos nuevos y robustos que puedan rescatar el tejido de la extremidad privado de riego.
Una enfermedad común con opciones limitadas
La enfermedad arterial periférica ocurre cuando las arterias de las piernas se estrechan, restringiendo el flujo sanguíneo. En su forma más grave, la isquemia crítica de extremidades, las personas pueden sufrir dolor constante, necrosis en los dedos y un alto riesgo de perder parte de la extremidad. Las terapias actuales, como los fármacos para reducir el colesterol, la angioplastia o el bypass quirúrgico, pueden ayudar, pero muchos pacientes no responden o están demasiado enfermos para estos procedimientos. Intentos previos con un solo tipo de célula madre han fomentado en su mayoría vasos frágiles y diminutos que no aportan suficiente flujo para salvar la extremidad de forma fiable. Por ello, los investigadores buscaron construir un “sistema de tuberías” más completo combinando dos tipos celulares que cooperen entre sí.
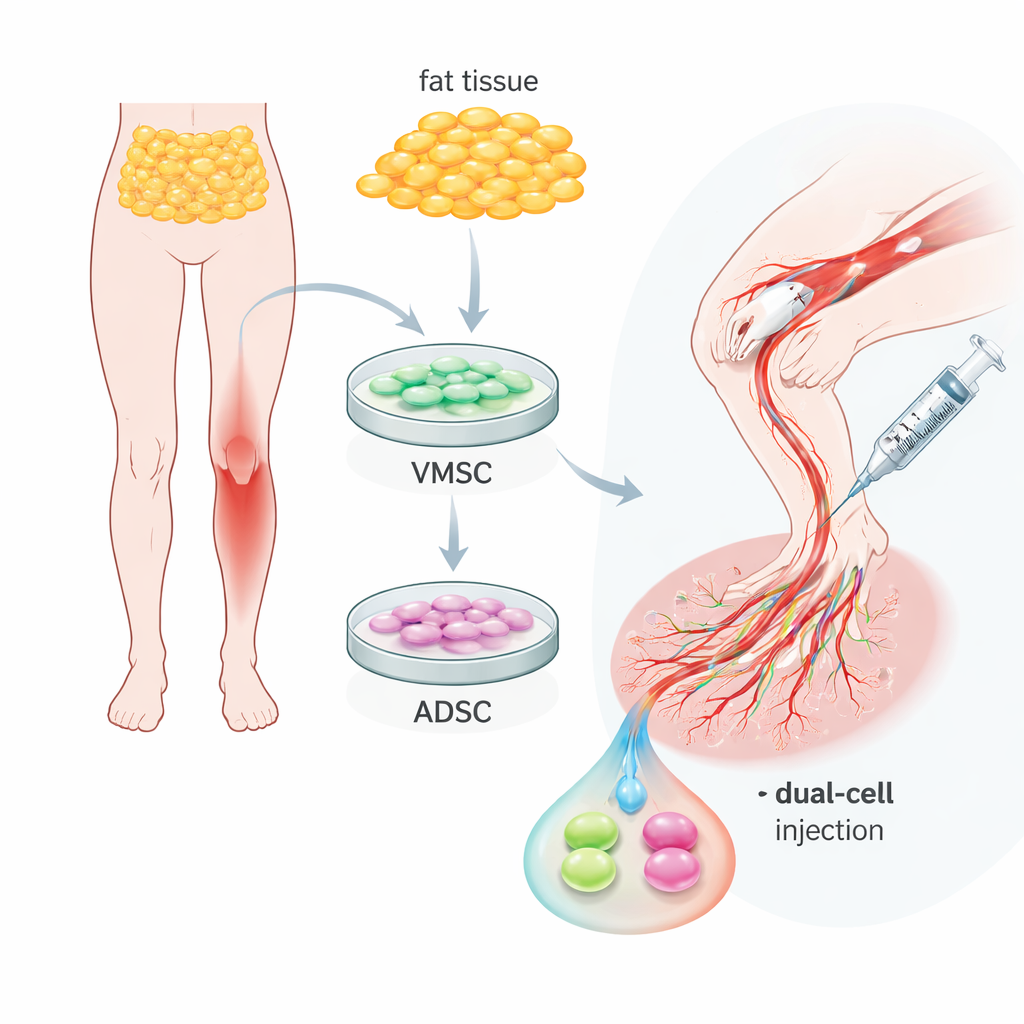
Dos tipos celulares útiles en la grasa corporal común
El equipo se centró en el tejido adiposo—la grasa corporal habitual—que puede recogerse mediante procedimientos relativamente menores. A partir de la misma muestra aislaron dos poblaciones celulares relacionadas pero distintas. Un grupo, denominado células madre multipotentes vasculares, se comportó como células precursoras de la capa interna de los vasos: mostraron marcadores de superficie típicos de células endoteliales y pudieron organizarse en tubos semejantes a capilares en placas de cultivo. El segundo grupo, células madre derivadas del adipocito, se asemejaba más a células de soporte que rodean los vasos, con marcadores propios de músculo liso y células perivasculares. Ambos tipos proliferaron bien y podían diferenciarse en adipocitos, osteocitos o condrocitos, confirmando su plasticidad, pero sus papeles naturales alrededor de los vasos eran claramente distintos y complementarios.
Trabajando juntos bajo estrés
Para imitar el ambiente hostil e inflamado de una extremidad enferma, los investigadores expusieron las células a una señal inflamatoria intensa. Ambos tipos sobrevivieron y ajustaron su comportamiento liberando mezclas de factores de crecimiento y enzimas que facilitan el movimiento celular y la remodelación del tejido circundante. Cuando se cultivaron por separado sobre un gel que favorece la formación vascular, las células tipo endotelial pudieron formar tubos básicos, mientras que las células de soporte tendían a agruparse. Sin embargo, al mezclarlas en una proporción de dos a uno, los tubos resultaron más densos, más continuos y más resistentes al estrés inflamatorio. Esto sugiere que, juntas, las dos poblaciones pueden formar no solo más vasos, sino redes más maduras y estables.
Probando la terapia dual en extremidades enfermas de ratón
Los científicos pasaron luego a un modelo murino de isquemia crítica de extremidades creado al ocluir una arteria principal de la pierna. En el músculo de la extremidad privada de riego inyectaron las células humanas mezcladas. Durante cuatro semanas, los ratones no tratados frecuentemente perdieron dedos o pies enteros, y sus músculos mostraron cicatrización e inflamación intensa. En contraste, los animales que recibieron el tratamiento con las dos células conservaron en gran medida sus extremidades. Las exploraciones del flujo sanguíneo mostraron que la circulación en las piernas tratadas se recuperó hasta aproximadamente el 70% de la normal, comparado con menos del 20% en los controles. Imágenes microscópicas y tridimensionales revelaron la razón: los músculos tratados contenían muchos más vasos de calibre medio y grande—ramificaciones tipo arteriola—con fuertes “mangas” de células de soporte, en lugar de un enredo de capilares diminutos e inestables.
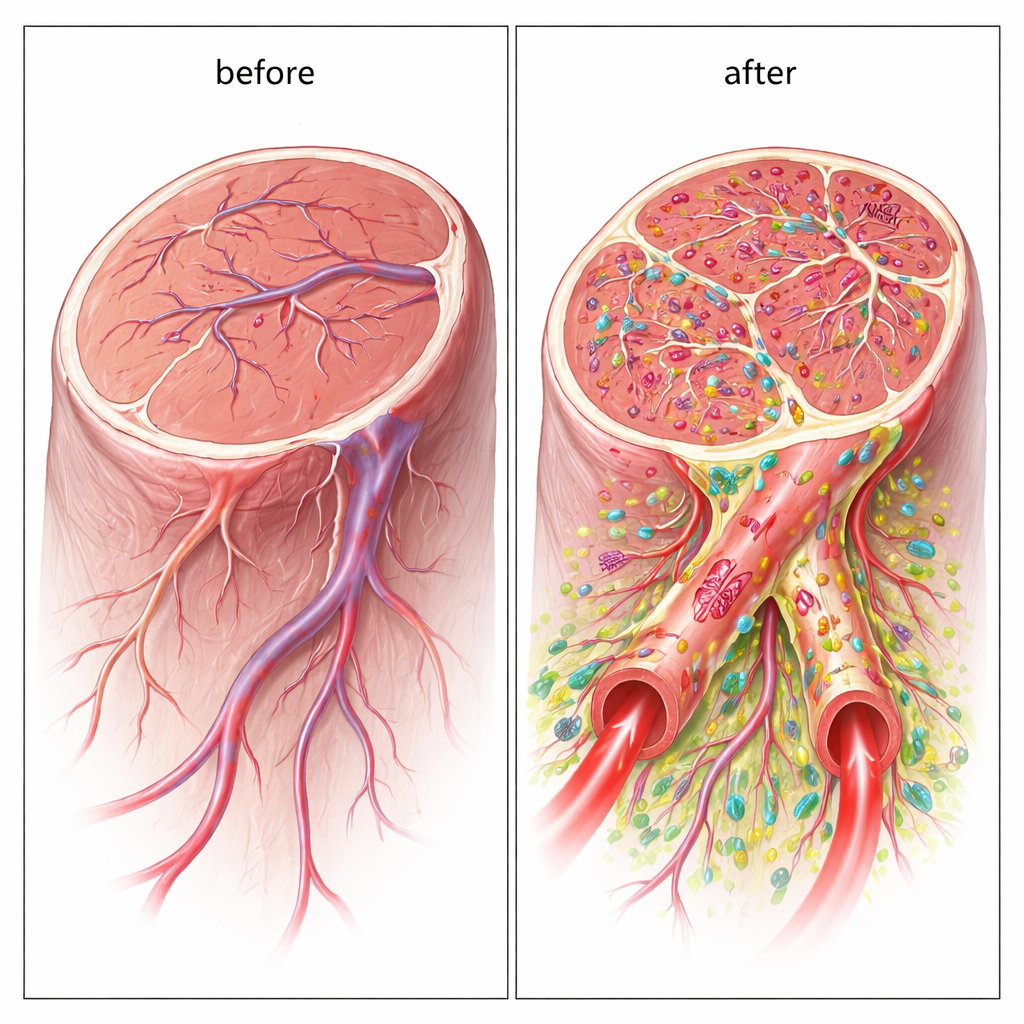
Vasos híbridos construidos a partir de células donantes
Es importante que los nuevos vasos no solo fueron estimulados por las células; en realidad contenían las células humanas trasplantadas como parte de sus paredes. Usando marcadores específicos humanos, los investigadores observaron que las células tipo endotelial contribuyeron a formar el revestimiento interno, mientras que las células de soporte rodearon el exterior. Muchos de estos vasos híbridos eran lo bastante anchos para funcionar como conductos adecuados para la sangre, y trazadores fluorescentes confirmaron que la sangre fluía a través de ellos. Esta construcción directa de vasos grandes y perfundidos distingue el enfoque de doble célula de la mayoría de las terapias con células madre previas, que dependen principalmente de señales químicas más que de una integración estructural duradera.
Qué podría significar esto para los pacientes
Para un público no especialista, el mensaje es que los científicos podrían estar aprendiendo a “re-tuberizar” extremidades moribundas usando células derivadas de la propia grasa de la persona. Al emparejar dos tipos celulares—uno que forma el conducto interno y otro que construye el soporte exterior—la terapia genera arterias y arteriolas fuertes y bien revestidas en lugar de brotes frágiles. En ratones, esto bastó para restaurar el flujo sanguíneo y prevenir la pérdida de la extremidad. Aunque hace falta más trabajo para demostrar la seguridad y eficacia a largo plazo en humanos, el estudio apunta a un futuro en el que una extracción de grasa mínimamente invasiva podría proporcionar mezclas celulares personalizadas para reconstruir la circulación en pacientes con alto riesgo de amputación.
Cita: Kim, D.Y., Hwang, D.Y., Park, G. et al. Adipose-derived dual cell therapy enhances arteriogenesis and limb preservation through vascular integration in critical limb ischemia. npj Regen Med 11, 13 (2026). https://doi.org/10.1038/s41536-026-00458-x
Palabras clave: isquemia crítica de extremidades, terapia con células madre, células derivadas del tejido adiposo, neovascularización, enfermedad arterial periférica