Clear Sky Science · es
La inhibición de CDK8 rescata la consolidación ósea deteriorada por isquemia
Por qué la circulación importa cuando los huesos se rompen
La mayoría de las fracturas acaban consolidándose por sí solas, pero para millones de personas cada año ese proceso se detiene. Un flujo sanguíneo deficiente alrededor de la fractura —conocido como isquemia— aumenta de forma drástica el riesgo de que una fractura cure lentamente, de forma deficiente o no llegue a consolidar. Este estudio explora por qué ocurre esto a nivel celular y evalúa una pastilla experimental que parece impulsar al organismo a abandonar la reparación tipo cicatriz y volver hacia la regeneración ósea verdadera.
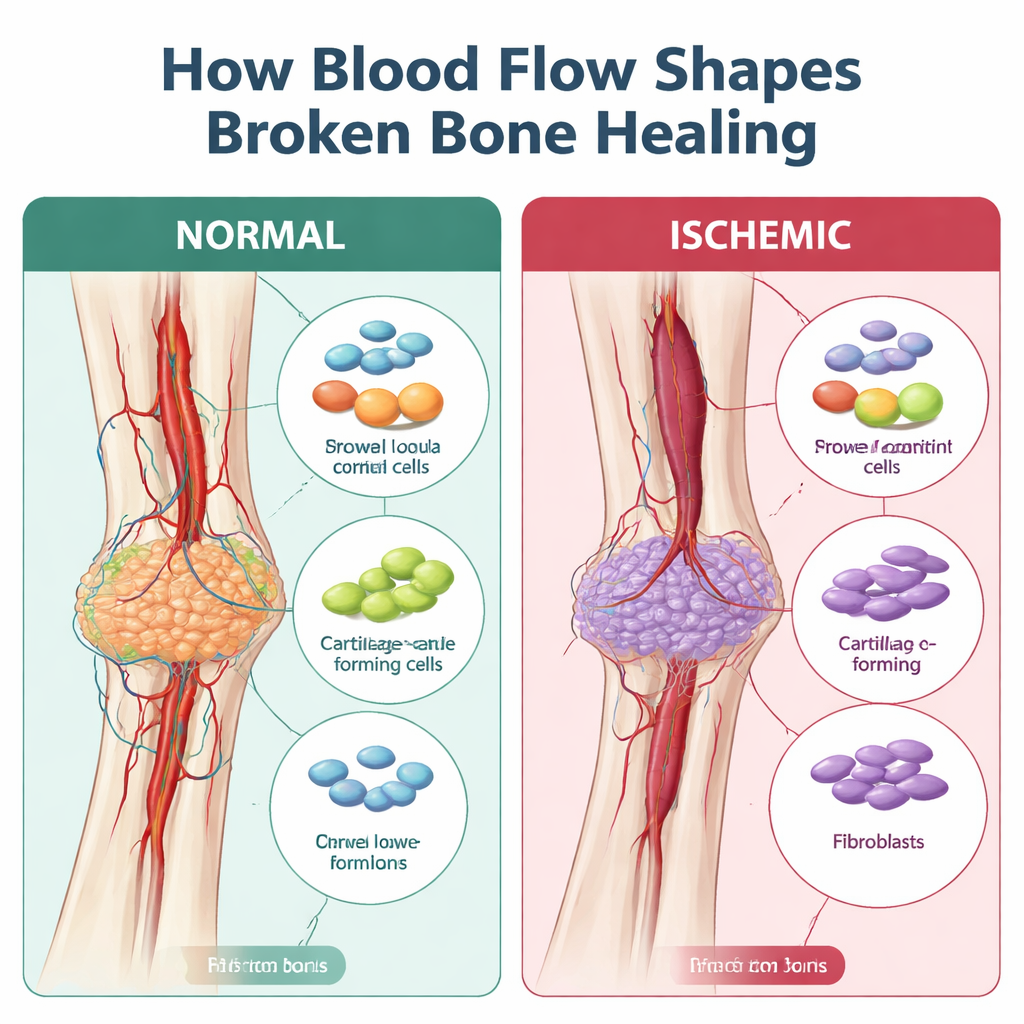
Cuando la curación deriva en cicatrización en lugar de reconstrucción
El hueso normalmente cura formando un puente blando de cartílago que se reemplaza gradualmente por hueso duro. Ese puente, llamado callo, depende de un suministro de células de apoyo con características de progenitores, células inmunitarias y vasos sanguíneos que coordinan la reparación. En las fracturas isquémicas, trabajos previos mostraron que el callo tiende a ser más pequeño, más débil y estar relleno de tejido fibroso, más parecido a una cicatriz que a un parche sólido de hueso nuevo. Lo que faltaba era un mapa detallado de qué células se desvían y cuándo durante este trayecto erróneo de la curación.
Las células individuales revelan un desvío hacia la fibrosis
Los investigadores usaron un modelo murino en el que una arteria de la pierna se daña quirúrgicamente en el momento de la fractura, reproduciendo de cerca la pérdida de flujo sanguíneo observada en lesiones graves o en personas con enfermedad vascular o que fuman. Luego aplicaron secuenciación de ARN de una sola célula, una técnica que lee los genes activos en miles de células individuales, al callo de la fractura a los cuatro y siete días tras la lesión. En fracturas bien perfundidas, el callo temprano estaba lleno de células inmunitarias que pronto daban paso a la expansión de células estromales —las células de apoyo que se convierten en cartílago y hueso. Sin embargo, en condiciones isquémicas hubo muchas menos células formadoras de cartílago y hueso y muchas más fibroblastos, las células que depositan tejido fibroso. Un análisis computacional de “trayectorias” mostró que, en lugar de madurar de forma continua desde progenitores tempranos a cartílago, las células estromales en hueso isquémico a menudo se desviaban mediante un estado similar a fibroblastos, lo que coincide con el aspecto más cicatricial del callo observado al microscopio.
Un freno molecular sobre las células formadoras de hueso
Al profundizar en la actividad génica de estas células, el equipo detectó una fuerte señal de estrés celular en los callos isquémicos, incluidos niveles elevados de proteínas de choque térmico. Entre los cambios más llamativos se observó un aumento en la actividad de un gen llamado Cdk8, que codifica una enzima reguladora integrada en un gran complejo de transcripción y que puede ralentizar o redirigir la forma en que las células responden a señales. Se sabe que Cdk8 bloquea la diferenciación celular en otros contextos. Aquí, estaba especialmente elevado en progenitores estromales tempranos en hueso isquémico. Células estromales mesenquimales humanas cultivadas en condiciones de bajo oxígeno —que imitan el pobre flujo sanguíneo— también aumentaron CDK8, vinculando directamente la falta de oxígeno con este posible “freno” sobre la formación de cartílago y hueso.
Apagar CDK8 para rescatar la reparación
Los investigadores se preguntaron si bloquear CDK8 podría liberar a las células estromales para reanudar la curación adecuada. En cultivo celular, tratar progenitores murinos y humanos con inhibidores selectivos de CDK8 aumentó genes clave del cartílago y la producción de matriz cartilaginosa, y también potenció la mineralización cuando las mismas células se indujeron hacia destino óseo. El equipo probó entonces un inhibidor oral de CDK8/19 llamado SNX631-6 en ratones con fracturas isquémicas. Administrado durante la ventana temprana de formación de cartílago, el fármaco incrementó la cantidad de cartílago en el callo. Cuando el tratamiento se prolongó hasta la transición posterior de cartílago a hueso, los callos mostraron más hueso total, mayor contenido mineral y un tamaño global mayor en micro–TC y en secciones de tejido, lo que indica una reparación estructural más robusta.
Del hallazgo en el laboratorio a posibles nuevas terapias
En conjunto, los resultados sugieren que la isquemia orienta a las células reparadoras hacia un destino estresado y fibrótico en parte aumentando CDK8, lo que limita su capacidad de convertirse en cartílago y hueso. Bloquear esta enzima parece liberar ese freno, permitiendo que se forme más cartílago al principio y que se deposite más hueso después, incluso cuando el suministro sanguíneo está comprometido. Dado que los inhibidores de CDK8 ya se están probando en pacientes con cáncer, podrían en el futuro reutilizarse para ayudar a personas con alto riesgo de mala consolidación —como adultos mayores, fumadores o quienes padecen enfermedad vascular— a regenerar hueso resistente en lugar de tejido cicatricial frágil.
Cita: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
Palabras clave: curación de fracturas óseas, isquemia, inhibidor de CDK8, células estromales mesenquimales, fibrosis