Clear Sky Science · es
Injerto de células epiteliales alveolares tipo II de tipo salvaje en ratones deficientes en la proteína surfactante C
Por qué importa reparar los diminutos sacos de aire
Respirar puede parecer un acto sin esfuerzo, pero depende de una película delicada llamada surfactante que recubre los millones de diminutos sacos de aire en nuestros pulmones. Cuando el surfactante falta o es defectuoso, como ocurre en algunas enfermedades pulmonares infantiles raras, los niños pueden sufrir problemas respiratorios persistentes y cicatrización del tejido pulmonar. Hoy por hoy, la única cura real es el trasplante de pulmón, una opción limitada por la escasez de donantes y riesgos importantes. Este estudio explora una idea diferente: reparar los pulmones dañados trasplantando células sanas que producen surfactante, lo que podría abrir la puerta a tratamientos más suaves y dirigidos.
Cuando los cuidadores del pulmón fallan
Dentro de cada saco de aire (alvéolo) viven células especializadas “cuidadores” llamadas células alveolares tipo II. Producen y reciclan el surfactante, que evita que los alvéolos colapsen y facilita la respiración. En algunos niños, las mutaciones en genes necesarios para producir surfactante, incluido el gen de la proteína surfactante C (SFTPC), alteran estas células. El resultado es la enfermedad pulmonar intersticial infantil (chILD), caracterizada por inflamación, engrosamiento del tejido pulmonar, cicatrización y, a veces, insuficiencia respiratoria. Los médicos solo pueden ofrecer tratamientos de apoyo y oxígeno; para los casos más graves, el trasplante pulmonar es el último recurso. Los autores se propusieron probar si reemplazar algunas de las células defectuosas por células sanas podría frenar o revertir el daño pulmonar.
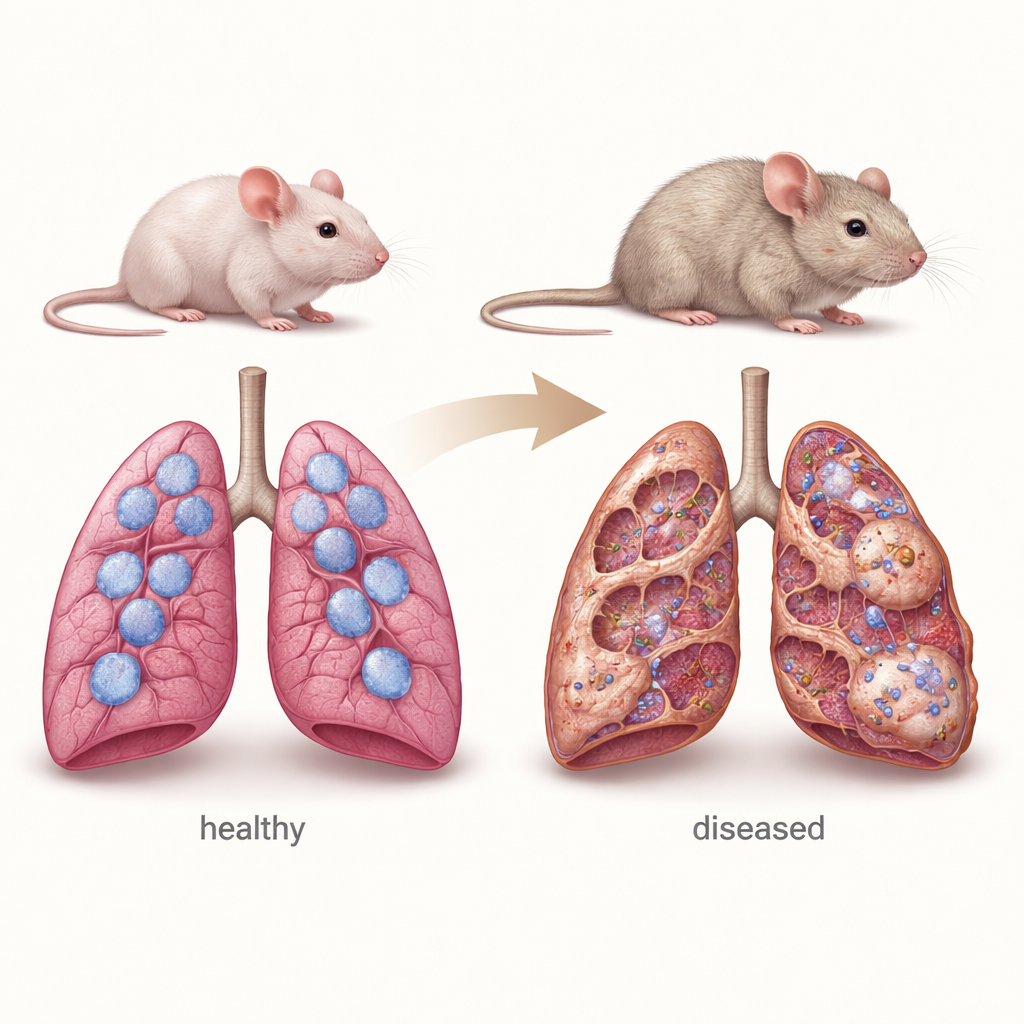
Un modelo de ratón para la enfermedad pulmonar infantil
Para imitar rasgos clave de la chILD, los investigadores usaron ratones que carecen por completo del gen Sftpc. Estos animales nacen con pulmones aparentemente normales, pero al envejecer desarrollan los signos característicos de enfermedad pulmonar crónica: paredes engrosadas entre los alvéolos, tejido cicatricial adicional rico en colágeno, sobrecrecimiento de las células tipo II y acumulación de células inmunitarias. Mediciones detalladas mostraron que la arquitectura pulmonar empeora de forma continua entre los 4 y los 12 meses de edad, asemejándose a la progresión lenta observada en muchos pacientes humanos. El equipo también encontró que estos ratones son inusualmente sensibles al fármaco quimioterápico bleomicina, que se usa a menudo en laboratorios para inducir lesión pulmonar y fibrosis, lo que subraya aún más la vulnerabilidad de sus pulmones deficientes en surfactante.
Preparar pulmones dañados para aceptar nuevas células
Trasplantar células nuevas en un órgano ya saturado no es trivial. Los autores probaron si una dosis cuidadosamente elegida y baja de bleomicina podía actuar como una especie de tratamiento de “acondicionamiento”: dañar algunas de las células residentes defectuosas y crear espacio para las recién llegadas sin destruir el pulmón. En ratones deficientes en Sftpc, incluso pequeñas cantidades de bleomicina agravaron la cicatrización y redujeron los niveles de varios marcadores clave de las células tipo II, confirmando la lesión. Sin embargo, en la dosis más baja el daño fue limitado y la respuesta reparadora propia del pulmón permaneció activa. Este equilibrio sugirió una ventana en la que las células trasplantadas podrían tener la mejor oportunidad de adherirse, sobrevivir y contribuir a la curación.
Células de surfactante sanas se instalan y actúan
El equipo aisló entonces células tipo II sanas de ratones normales y administró un millón de estas células directamente en las vías respiratorias de ratones deficientes en Sftpc diez días después de la bleomicina de baja dosis. Mediante una combinación de tinción proteica y pruebas genéticas, mostraron que las células donantes se injertaron con eficacia, especialmente en animales jóvenes. Estas células trasplantadas produjeron proteína surfactante C madura—completamente ausente en el huésped—lo que indica que no solo estaban presentes sino funcionalmente activas. Las nuevas células persistieron al menos durante dos meses. De forma importante, los ratones que recibieron trasplantes celulares presentaron menos lesión pulmonar y menos regiones gravemente dañadas en comparación con los ratones tratados solo con bleomicina, lo que sugiere que incluso el reemplazo parcial de células enfermas puede amortiguar el daño en curso.
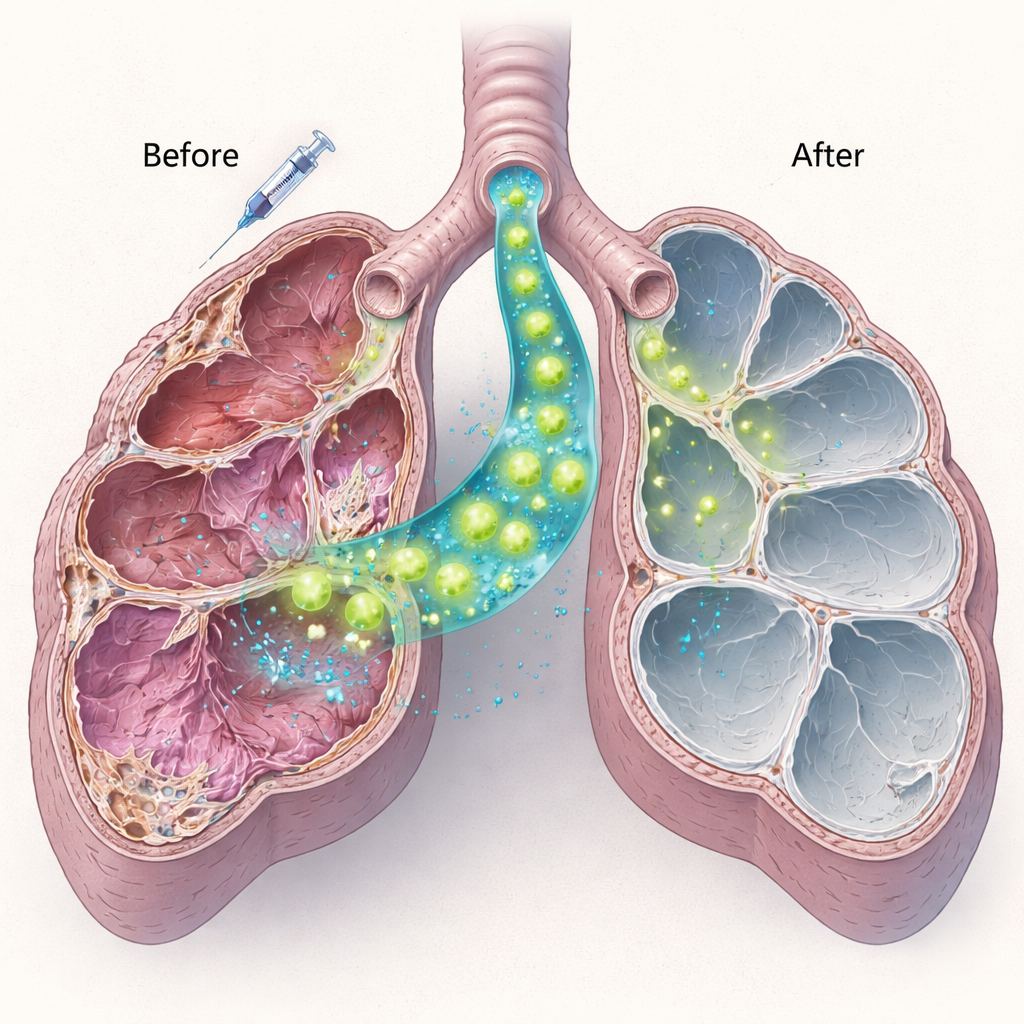
Del ensayo de concepto a futuras terapias
Para los no especialistas, el mensaje clave es que este estudio demuestra una vía realista para reparar, en lugar de reemplazar, los pulmones en ciertas enfermedades genéticas infantiles. Al mostrar que un número modesto de células productoras de surfactante sanas puede echar raíces en un pulmón crónicamente enfermo, producir la proteína que falta y aliviar la lesión, el trabajo ofrece una base para futuras terapias basadas en células pulmonares derivadas de corrección genética o de células madre. Quedan muchos obstáculos, incluida la búsqueda de formas más seguras de preparar pulmones humanos para este tratamiento y garantizar un beneficio duradero. Aun así, esta investigación cambia la conversación de manejar los síntomas a, potencialmente, reconstruir la propia maquinaria pulmonar para una respiración saludable.
Cita: Predella, C., Lapsley, L., Ni, K. et al. Engraftment of wild-type alveolar type II epithelial cells in surfactant protein C deficient mice. npj Regen Med 11, 11 (2026). https://doi.org/10.1038/s41536-026-00455-0
Palabras clave: enfermedad pulmonar intersticial infantil, proteína surfactante C, células alveolares tipo II, terapia celular, fibrosis pulmonar