Clear Sky Science · es
El mapa sensorial olfativo se ve perturbado en un modelo transgénico de ratón con sobreexpresión de α-sinucleína humana de tipo salvaje de la enfermedad de Parkinson
Por qué importa la pérdida del olfato en el Parkinson
Mucha gente asocia la enfermedad de Parkinson con un trastorno del movimiento, pero para la mayoría de los pacientes lo primero que falla es el sentido del olfato. Esta pérdida puede aparecer décadas antes del temblor o la rigidez, por lo que constituye una potente señal de aviso temprana. El estudio que se describe aquí plantea una pregunta básica pero aún no resuelta: ¿qué sucede exactamente en el circuito cerebral del olfato cuando comienzan los cambios relacionados con el Parkinson? Al investigar esta cuestión en un modelo de ratón cuidadosamente diseñado, los investigadores revelan cómo una proteína clave del Parkinson altera el “mapa olfativo” interno del cerebro y señalan una nueva y fácilmente accesible fuente de pistas tempranas de la enfermedad.
El mapa olfativo del cerebro
Nuestras narices contienen millones de células especializadas en detectar olores, cada una de las cuales responde a determinadas moléculas odoríferas. Estas células envían fibras largas y delgadas hacia la parte anterior del cerebro, donde convergen en pequeños núcleos llamados glomérulos dentro del bulbo olfativo. Cada tipo de olor activa un patrón específico de glomérulos, formando un mapa sensorial preciso que permite al cerebro distinguir café de canela o humo de perfume. En ratones sanos, las células que portan un receptor de olor (denominado M72) y otro (denominado P2) proyectan de forma fiable a solo dos glomérulos bien definidos por bulbo, creando un mapa muy ordenado y reproducible.
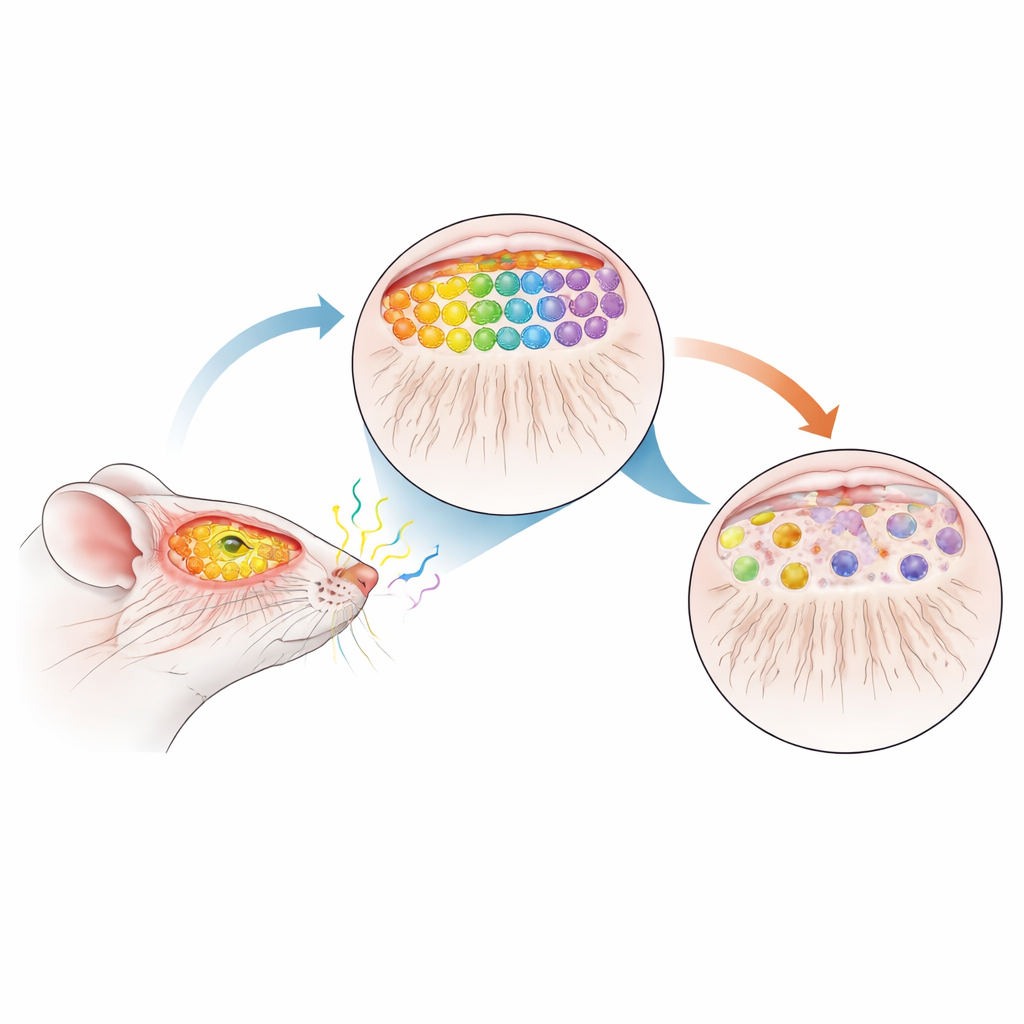
Un ratón que representa las primeras fases del Parkinson
Para ver cómo la enfermedad de Parkinson podría alterar este mapa, el equipo utilizó ratones que sobreproducen α-sinucleína humana normal, la misma proteína que forma agregados en los cerebros de las personas con Parkinson. Después cruzaron estos animales con ratones marcados en M72 y P2 para poder seguir visualmente células olfativas seleccionadas y sus conexiones. Es importante que el exceso de α-sinucleína se active solo después del nacimiento y se acumule gradualmente con la edad, imitando el curso lento y progresivo de la enfermedad humana. A los 12 meses de edad —aproximadamente la mediana de la vida para un ratón y comparable a una fase prodrómica o prediagnóstica en humanos— los investigadores examinaron en detalle los sistemas olfativos de los animales.
Cuando el mapa olfativo se descompone
Mediante el teñido de las neuronas marcadas y el seguimiento de sus trayectos, los científicos hallaron una notable ruptura del mapa olfativo en los ratones con sobreexpresión de α-sinucleína. El número de neuronas M72 y P2 en la nariz cayó drásticamente: aproximadamente una pérdida del 75 % para M72 y casi la mitad para P2, mientras que sus fibras hacia el bulbo se vieron muy reducidas. En lugar de converger ordenadamente en dos glomérulos robustos, las fibras restantes con frecuencia formaron múltiples glomérulos más pequeños de tamaño y posición variables. Estos núcleos “extra” no aparecían en ubicaciones consistentes entre ratones, lo que indica una pérdida de la precisión topográfica normal. Un marcador amplio de las terminales de las células olfativas, VGLUT2, también se redujo en torno a un 44 % en el bulbo, lo que indica que esta degeneración se extendía mucho más allá de los dos tipos de receptores marcados.
Relacionando circuitos dañados con la pérdida de olfato
El daño estructural se tradujo en problemas olfativos medibles. Los ratones mayores con α-sinucleína tardaban más en localizar comida oculta, mostraban peor capacidad para distinguir un olor de otro y no preferían áreas marcadas con su propio olor —pruebas de comportamiento que, en conjunto, revelan hiposmia y deterioro de la discriminación de olores. También necesitaban concentraciones de olor mucho más intensas para responder, lo que pone de manifiesto una sensibilidad reducida. Estos déficit no aparecían en ratones más jóvenes, en los que las neuronas marcadas y sus mapas todavía parecían en gran medida normales, vinculando el momento de la pérdida funcional con la ruptura tardía del mapa sensorial más que con el desarrollo temprano. Es notable que, si bien la proteína problemática era abundante en el bulbo olfativo, no se detectó en el epitelio sensorial de la nariz, lo que señala a cambios dentro del circuito del bulbo —particularmente en las células mitrales que transmiten la información olfativa— como los probables impulsores de la alteración del mapa.
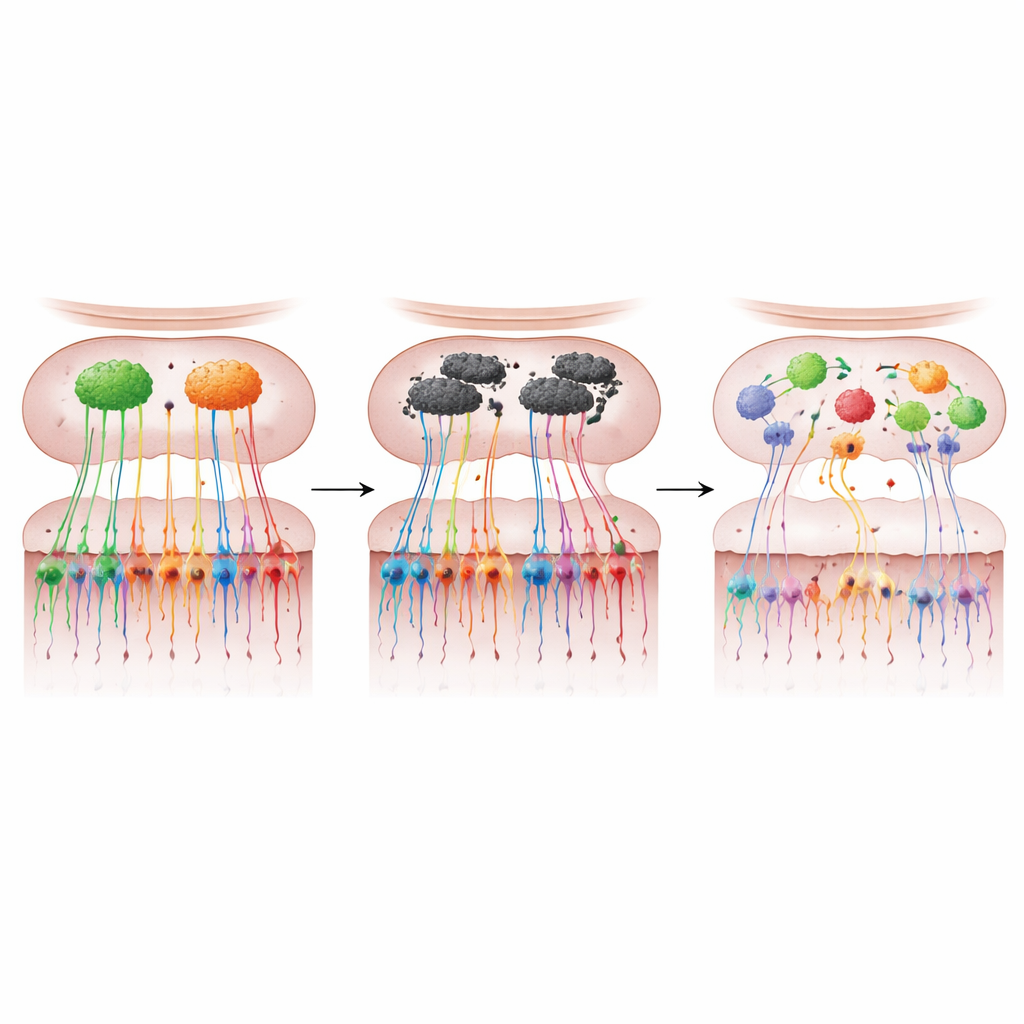
Las células olfativas como ventanas a la enfermedad temprana
En conjunto, el trabajo respalda un mensaje claro para no especialistas: en este modelo de ratón que imita el Parkinson, la sobreproducción de α-sinucleína en el bulbo olfativo conduce tanto a la pérdida como al cableado incorrecto de las neuronas olfativas, deformando el mapa de olores del cerebro y provocando problemas olfativos tempranos. Dado que las células sensoriales de la nariz están emparentadas en su desarrollo con el cerebro y, sin embargo, se pueden muestrear con hisopos o biopsias mínimamente invasivas, los autores sostienen que cambios similares en personas podrían proporcionar un biomarcador temprano potente de la enfermedad de Parkinson. Mapear las huellas moleculares de estas células, sugieren, podría no solo ayudar a identificar a individuos en riesgo años antes de que aparezcan los síntomas motores, sino también ofrecer nuevas perspectivas sobre cómo empieza y se propaga la enfermedad, y cómo podría ralentizarse o prevenirse.
Cita: Biju, K.C., Hernandez, E.T., Stallings, A.M. et al. Olfactory sensory map is perturbed in a human wild-type α-synuclein overexpressing transgenic mouse model of Parkinson’s disease. npj Parkinsons Dis. 12, 70 (2026). https://doi.org/10.1038/s41531-026-01288-w
Palabras clave: Enfermedad de Parkinson, disfunción olfativa, alfa-sinucleína, mapa sensorial, biomarcadores