Clear Sky Science · es
La mutación LRRK2R1627P amplifica la inflamación crónica inducida por factores ambientales y la agregación de α-sinucleína en el intestino de ratas
Por qué el intestino importa en una enfermedad cerebral
La enfermedad de Parkinson es más conocida por los temblores y los problemas de movimiento, pero cada vez hay más pruebas de que sus raíces pueden comenzar lejos del cerebro, en lo profundo del intestino. Este estudio explora cómo un cambio genético específico vinculado al Parkinson en poblaciones asiáticas puede, junto con el envejecimiento y la exposición a toxinas, dañar gradualmente el intestino de las ratas. Al observar lo que sucede en el intestino a lo largo de la vida de los animales, los investigadores trazan cómo las defensas inmunitarias cotidianas pueden derivar hacia una inflamación crónica, preparando el terreno para la acumulación de proteínas relacionadas con la enfermedad que eventualmente podrían amenazar el cerebro.
Un gen de riesgo en el tracto digestivo
Los científicos se centraron en una variante de un gen llamado LRRK2, vinculado desde hace tiempo a la enfermedad de Parkinson y a ciertas afecciones inflamatorias intestinales. Crearon ratas portadoras de la mutación análoga, denominada LRRK2R1627P, y las compararon con ratas normales a lo largo de su vida. Aunque la cantidad de ARN mensajero del gen LRRK2 en el intestino no cambió, la proteína LRRK2 total y uno de sus marcadores de actividad clave disminuyeron, lo que indica que la mutación debilita la función normal de esta proteína en el intestino. Este cambio molecular sutil no provocó un daño temprano y dramático, pero alteró silenciosamente la forma en que las células intestinales se renuevan y se organizan a medida que los animales envejecen.
Un intestino envejecido bajo una tensión lenta y persistente
A medida que pasaron los meses, las ratas con la mutación desarrollaron señales claras de estructura intestinal alterada. Sus intestinos delgados se acortaron, y las finas vellosidades y las criptas que absorben nutrientes redujeron su tamaño. Ciertas células especializadas del epitelio que producen moco protector y sustancias antimicrobianas—células caliciformes y células de Paneth—disminuyeron, mientras que las proteínas que ayudan a las células vecinas a formar uniones estrechas y resistentes a las fugas también cayeron. Al microscopio, estas uniones se volvieron más cortas o más anchas, lo que sugiere una barrera debilitada. Es importante señalar que la arquitectura general no colapsó; en cambio, el intestino mostró un patrón más insidioso de renovación y protección reducidas, lo que puede hacerlo más vulnerable a la irritación y la infección. 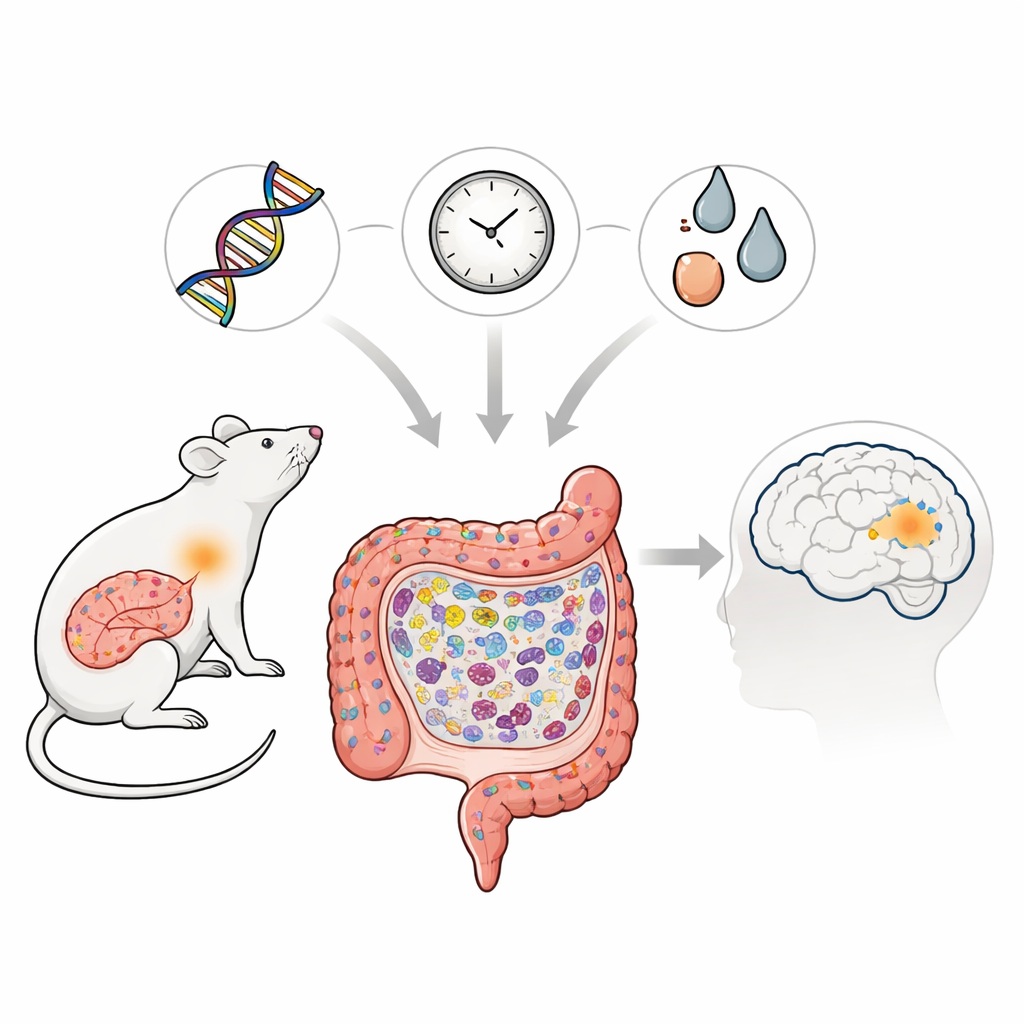
Sistema inmunitario en alerta máxima
Para entender por qué el intestino estaba perdiendo el equilibrio, el equipo examinó la actividad génica y las células inmunitarias en la pared intestinal. Encontraron que las vías vinculadas a un sensor llamado TLR4 y su socio NF-κB estaban sobreactivadas en las ratas mutantes de mayor edad. Estos sensores normalmente ayudan al organismo a detectar microbios nocivos, pero aquí impulsaron la acumulación de células inmunitarias de tipo “pelea primero” conocidas como macrófagos M1. Estas células segregaron moléculas inflamatorias, convirtiendo el intestino en un entorno crónicamente irritado. De forma llamativa, la proteína relacionada con el Parkinson, α-sinucleína, en su forma fosforilada asociada a la enfermedad, comenzó a acumularse no en las neuronas intestinales sino dentro de estos macrófagos activados en el intestino delgado, especialmente en los animales de mayor edad.
Más sensibles a agresiones ambientales
La mutación genética por sí sola no explicó todo. Cuando ratas jóvenes fueron expuestas brevemente a toxinas bacterianas (LPS), que estimulan TLR4, los animales con la mutación LRRK2 desarrollaron una inflamación intestinal mucho más severa que sus contrapartes normales. Su epitelio intestinal perdió más células, las proteínas de la barrera disminuyeron aún más y los macrófagos proinflamatorios se dispararon, acumulando de nuevo α-sinucleína anómala. Esto sugiere que las personas que portan mutaciones similares pueden ser especialmente sensibles a agresiones ambientales que alteran el intestino, como ciertas infecciones o toxinas, amplificando su riesgo a largo plazo.
Bajando la señal de alarma
Puesto que TLR4 ocupaba el centro de esta tormenta inflamatoria, el equipo probó un fármaco, TAK-242, que atenúa específicamente la señalización de TLR4. Administrado durante varios meses a ratas de mediana edad, el inhibidor restauró en gran medida la longitud del intestino delgado, el tamaño de vellosidades y criptas, las células productoras de moco y las proteínas de la barrera. Redujo los macrófagos sobreactivos, disminuyó las moléculas inflamatorias y redujo drásticamente la acumulación de α-sinucleína anómala en el intestino. Al mismo tiempo, corrigió una comunidad microbiana alterada: aumentó la diversidad, la sobrepoblación de Lactobacillus disminuyó y varios grupos bacterianos beneficiosos repuntaron, mientras que las funciones microbianas predichas se desviaron de patrones asociados a la enfermedad. 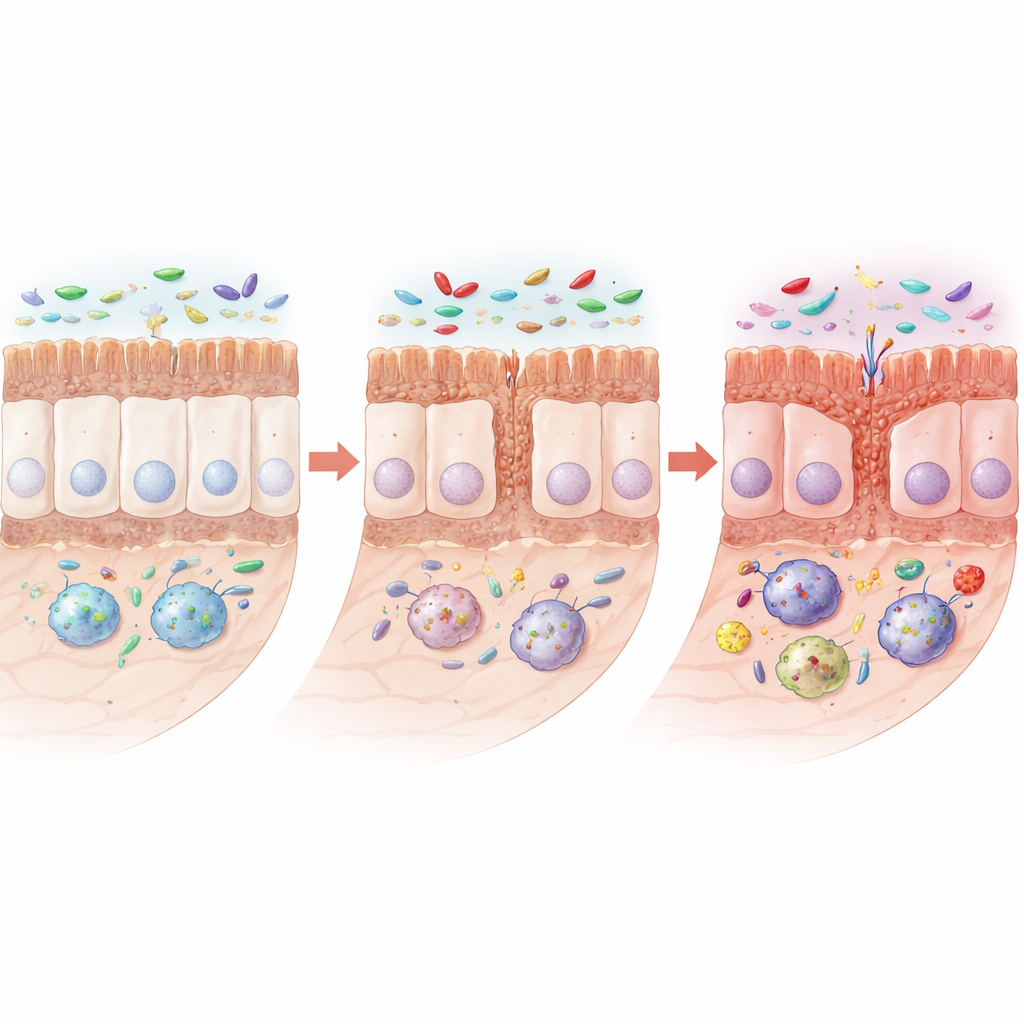
Qué significa esto para el riesgo de Parkinson
Para un público no especializado, el mensaje es que un “gen de Parkinson” puede remodelar silenciosamente las defensas inmunitarias del intestino con el tiempo, sobre todo en presencia de envejecimiento y estrés ambiental. En estas ratas, el resultado es una inflamación crónica de bajo grado que debilita la barrera intestinal, altera los microbios residentes y provoca la acumulación de proteínas vinculadas al Parkinson en células inmunitarias: no se trata aún de un Parkinson desarrollado por completo, pero sí de un entorno biológico que podría favorecer una enfermedad cerebral posterior. Al demostrar que bloquear una sola vía inmunitaria intestinal puede revertir muchos de estos cambios, el estudio destaca el intestino como un objetivo práctico temprano: proteger la salud intestinal y controlar la inflamación intestinal podría ayudar a retrasar o prevenir el Parkinson en personas con riesgo genético.
Cita: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
Palabras clave: Enfermedad de Parkinson, inflamación intestinal, mutación LRRK2, microbioma, inmunidad innata