Clear Sky Science · es
Utilidad clínica de los potenciales evocados para programar la estimulación cerebral profunda en el núcleo subtalámico en la enfermedad de Parkinson
Por qué importa esta historia del marcapasos cerebral
Para muchas personas con enfermedad de Parkinson, los fármacos acaban perdiendo eficacia de forma continua. Pueden oscilar entre rigidez y movimientos descontrolados, y el ajuste del tratamiento se convierte en un ciclo frustrante de visitas clínicas. Este artículo de revisión examina cómo los médicos pueden usar los ecos eléctricos del propio cerebro —llamados potenciales evocados— para programar la estimulación cerebral profunda (ECP) de forma más rápida y objetiva. En esencia, plantea si podemos transformar la programación de la ECP de un proceso de ensayo y error cuidadoso a un marcapasos cerebral más guiado por datos y personalizado.
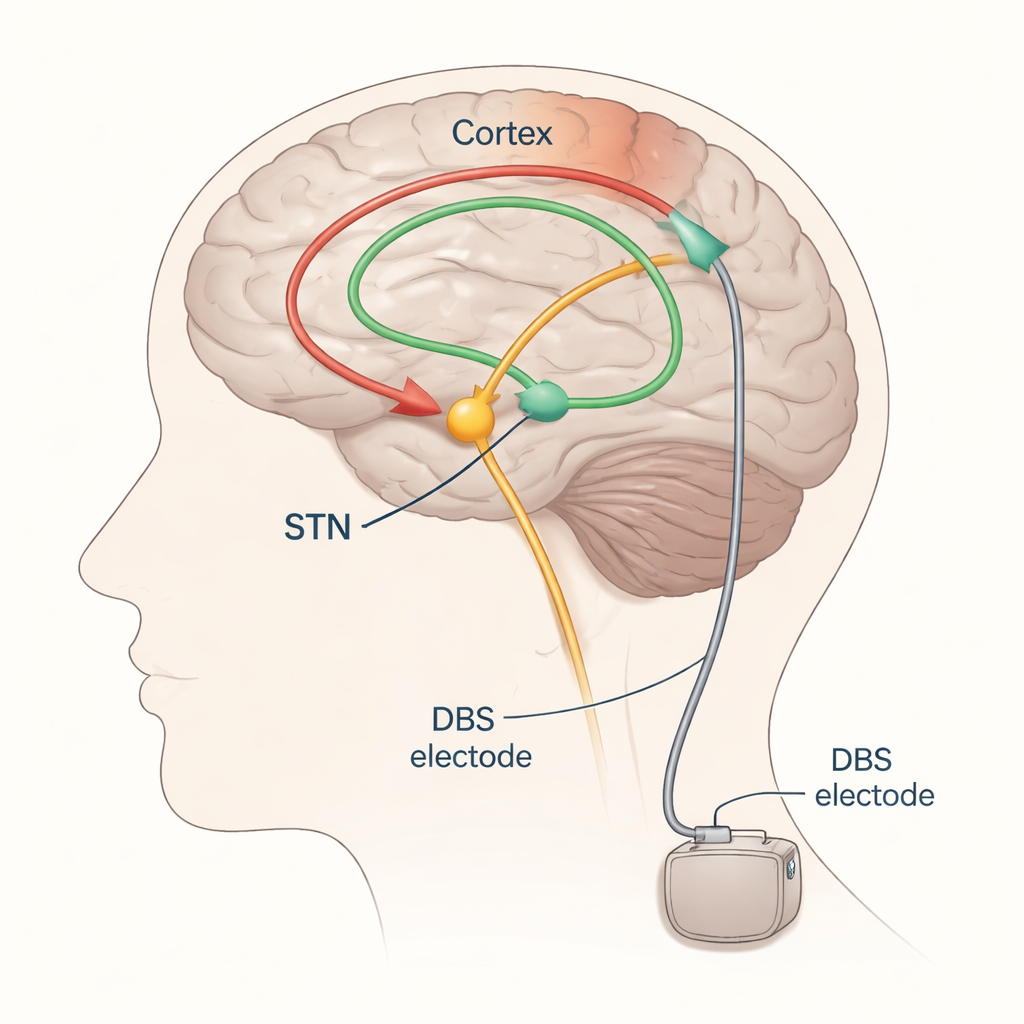
De prueba y error a ajuste guiado
La ECP en la enfermedad de Parkinson suele dirigirse a una estructura pequeña y profunda del cerebro llamada núcleo subtalámico (NST). Se implantan electrodos aquí y se conectan a un generador de pulsos debajo de la piel del pecho. Bien ajustada, la ECP en el NST puede aliviar el temblor, la bradicinesia y la rigidez, pero si el campo eléctrico se extiende demasiado puede estimular por error vías cercanas que controlan músculos o la sensibilidad, provocando efectos secundarios como tirones musculares u hormigueo. Hoy en día, los neurólogos suelen ajustar la ECP cambiando lentamente los parámetros y observando los movimientos y los efectos adversos del paciente: un enfoque que consume tiempo, depende de cómo se encuentre el paciente ese día y a menudo requiere varias visitas de seguimiento.
Escuchar los ecos eléctricos del cerebro
Los autores se centran en los potenciales evocados —pequeñas respuestas eléctricas sincronizadas en el cerebro o los músculos tras un estímulo— como posibles señales para distinguir ajustes buenos de malos en la ECP. Cuando se estimula el NST, ondas de actividad viajan por vías nerviosas y pueden captarse en el cuero cabelludo con EEG, en la actividad muscular con EMG, o en ocasiones con tiras de registro colocadas directamente sobre la superficie cerebral. Estimulando repetidamente a bajas frecuencias y promediando las respuestas, los investigadores pueden ver de forma fiable ondas distintas que aparecen con distintos retrasos (milisegundos) tras cada pulso. Las ondas tempranas, que llegan en aproximadamente dos milésimas de segundo, reflejan sobre todo la activación de vías motoras rápidas próximas al electrodo. Ondas algo más tardías, alrededor de tres milisegundos (a menudo llamadas componente “P3”), se cree que provienen de un vínculo directo entre la corteza frontal y el NST conocido como vía hiper directa. Ondas todavía más tardías probablemente viajan por circuitos más largos y en bucle que incluyen el tálamo y otros núcleos profundos.
Encontrar el punto óptimo y evitar problemas
En numerosos estudios surge una imagen consistente: los contactos del electrodo que generan una P3 fuerte y de latencia corta tienden a ubicarse en la zona más beneficiosa del NST y se asocian con mejoría de los síntomas motores parkinsonianos y con una “ventana terapéutica” más amplia antes de que aparezcan efectos secundarios. En contraste, ondas muy tempranas vinculadas a vías motoras y ciertas respuestas de 8–10 milisegundos suelen señalar que la estimulación se está propagando a estructuras vecinas, aumentando el riesgo de contracciones musculares u otros efectos indeseados. Mediciones separadas de potenciales motores evocados (respuestas EMG en músculos faciales y de las extremidades) y de potenciales evocados somatosensoriales (patrones EEG relacionados con vías táctiles) pueden revelar activación sutil de la cápsula interna o del lemnisco medial, haces de fibras que transmiten comandos motores e información sensorial. Detectar estos cambios pronto permite a los clínicos desviar la corriente de zonas de riesgo eligiendo contactos distintos o ajustando la forma de pulso y la polaridad.
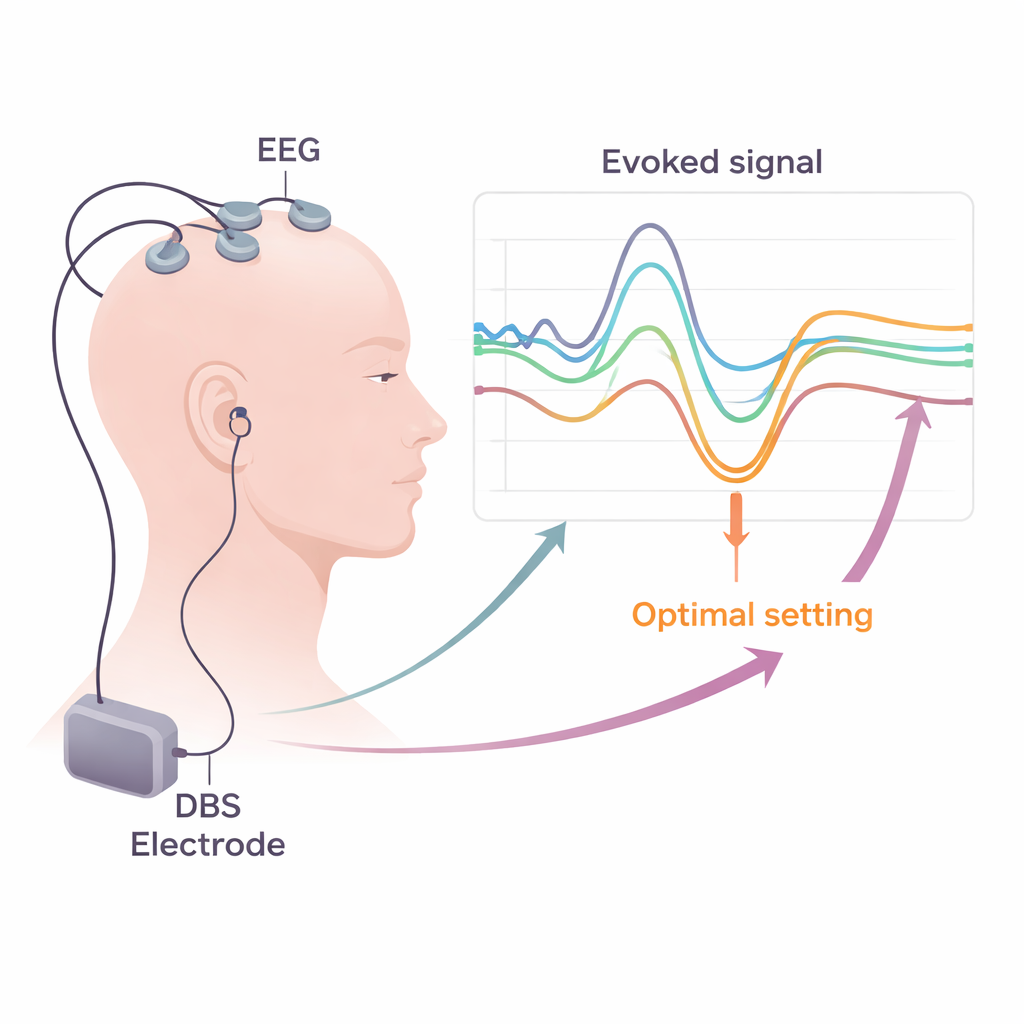
Hacer que las herramientas de laboratorio sean prácticas en la clínica
Convertir estos hallazgos en práctica rutinaria requiere soluciones prácticas. La revisión explica cómo los sistemas de EEG y EMG estándar de los hospitales ya pueden registrar la mayoría de las señales necesarias, siempre que usen tasas de muestreo altas y métodos cuidadosos para eliminar el “ruido” eléctrico de los pulsos de la ECP. Los autores abordan estrategias para reducir artefactos, como referencia ingeniosa, sustracción de plantillas y algoritmos informáticos avanzados que separan la actividad cerebral real de los residuos de estimulación. Sostienen que sesiones de prueba breves y estructuradas —combinando periodos cortos de ECP a baja frecuencia, registros en cuero cabelludo y monitorización muscular durante reposo y ligera contracción— podrían integrarse en la semana habitual de programación postoperatoria. Los mapas de potenciales evocados de cada contacto podrían entonces combinarse con imágenes y otros biomarcadores para guiar qué contactos y ajustes utilizar a largo plazo.
Lo que esto significa para las personas con Parkinson
El artículo concluye que los potenciales evocados son candidatos prometedores para hacer la programación de la ECP más precisa, eficiente y predecible. En particular, la onda P3 de latencia corta parece ser un marcador sólido de que la estimulación está alcanzando el circuito correcto para aliviar los síntomas motores del Parkinson, mientras que las respuestas motoras y sensoriales evocas pueden alertar cuando la corriente se filtra a vías que causan efectos secundarios. Aunque hace falta más trabajo para estandarizar las técnicas y demostrar beneficios en la práctica cotidiana, este enfoque apunta hacia un futuro en el que los médicos puedan “escuchar” el cerebro durante la programación, localizar rápidamente el punto óptimo de cada paciente y reducir la carga de prueba y error para las personas que viven con la enfermedad de Parkinson.
Cita: Hale, B., Latorre, A., Rocchi, L. et al. Clinical utility of evoked potentials for programming subthalamic deep brain stimulation in Parkinsons disease. npj Parkinsons Dis. 12, 54 (2026). https://doi.org/10.1038/s41531-026-01274-2
Palabras clave: Enfermedad de Parkinson, estimulación cerebral profunda, potenciales evocados, mapeo cerebral, neurofisiología