Clear Sky Science · es
Lograr una aleación Mg‑Ca resistente a la corrosión mediante el control de la solidificación para secuestrar impurezas de Fe a nivel de partes por millón
Por qué importa proteger los metales ligeros
El magnesio es uno de los metales estructurales más livianos que tenemos, lo que lo hace atractivo para automóviles, aviones, electrónica portátil e incluso implantes médicos. Pero hay una pega: el magnesio se disuelve en entornos salinos y húmedos mucho más rápido que metales comunes como el acero o el aluminio. Este estudio explora una forma ingeniosa de lograr que una mezcla muy simple de magnesio y calcio resista la corrosión mejor que incluso el magnesio ultra‑puro, no eliminando impurezas, sino atrapándolas en el tipo adecuado de jaulas microscópicas durante la solidificación.
Una impureza minúscula con un gran impacto
Incluso cuando el magnesio se produce con altos estándares de pureza, todavía contiene trazas de hierro —solo unos pocos partes por millón. Eso suena insignificante, pero es suficiente para formar diminutas partículas ricas en hierro que actúan como pilas en miniatura cuando el metal se expone al agua salada. Esas partículas extraen electrones del magnesio circundante, acelerando la pérdida de metal y fomentando la producción de burbujas de hidrógeno. La sabiduría convencional ha sido eliminar el hierro tanto como sea posible o comprar magnesio de ultra‑alta pureza, lo cual es caro y difícil de escalar en la industria.
Usar calcio para construir jaulas microscópicas
Trabajos previos mostraron que añadir una pizca de calcio al magnesio (alrededor de una décima parte de porcentaje en peso) ralentiza drásticamente la corrosión, porque dentro del metal se forman nuevos compuestos microscópicos que contienen calcio, magnesio y silicio. En este estudio, los investigadores se centraron en una aleación específica de magnesio con 0,1 % de calcio y plantearon una pregunta más profunda: ¿cómo afecta la velocidad a la que se enfría y solidifica la aleación fundida al lugar donde termina el hierro y, por tanto, a la velocidad de corrosión? Para responderla, colaron la misma aleación usando cuatro velocidades de enfriamiento distintas, desde muy lentas hasta muy rápidas, y examinaron las microestructuras resultantes en detalle mediante microscopía electrónica y técnicas de mapeo.
Enfriamiento lento y hierro oculto
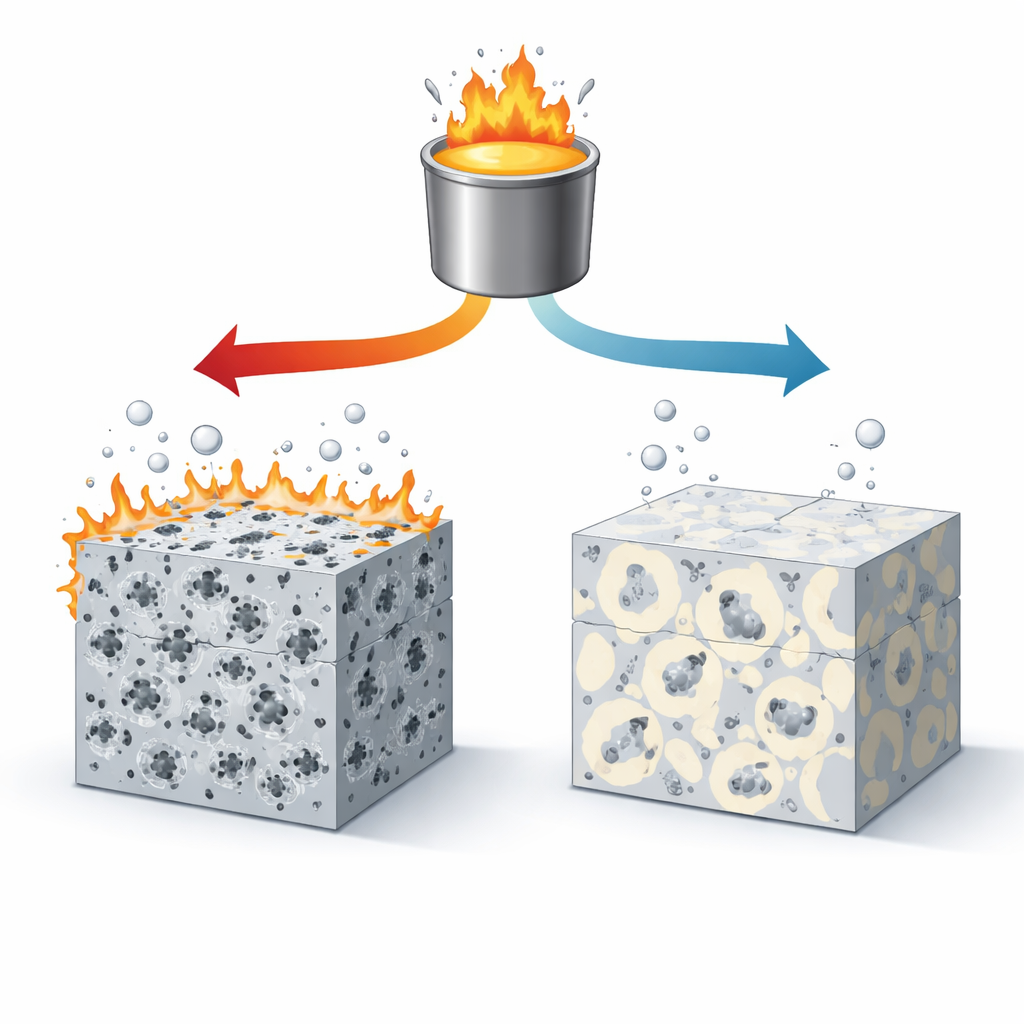
Cuando la aleación se enfrió lentamente, el equipo encontró partículas relativamente grandes del compuesto calcio‑magnesio‑silicio repartidas por el metal. Crucialmente, muchas de las partículas ricas en hierro estaban completamente encerradas dentro de estas partículas mayores, como semillas atrapadas en una fruta. Ese encapsulado implicaba que el hierro tenía poco contacto directo con el magnesio circundante. En ensayos de corrosión con agua salada similar al agua de mar, estas muestras enfriadas lentamente produjeron muy poco hidrógeno y perdieron metal a tasas miles de veces inferiores a las del magnesio de alta pureza ordinario. La corrosión fue suave y bastante uniforme, con solo picaduras superficiales y una película protectora en la superficie que se volvía más resistente con el tiempo.
Enfriamiento rápido y puntos problemáticos expuestos
A medida que la misma aleación se enfrió cada vez más rápido, los compuestos ricos en calcio se volvieron más pequeños y finamente divididos. Ya no crecían lo bastante para envolver muchas de las partículas ricas en hierro. La microscopía mostró numerosas motas ricas en hierro en contacto directo con el magnesio, o solo parcialmente cubiertas. En la exposición a agua salada, esos puntos descubiertos se convirtieron en sitios altamente activos donde la corrosión arrancaba rápidamente, excavando cavidades profundas y trayectos de ataque en forma de filamentos a lo largo de la superficie. Se generó hidrógeno mucho más rápido, y las medidas electroquímicas mostraron una actividad catódica más fuerte y películas superficiales menos protectoras.
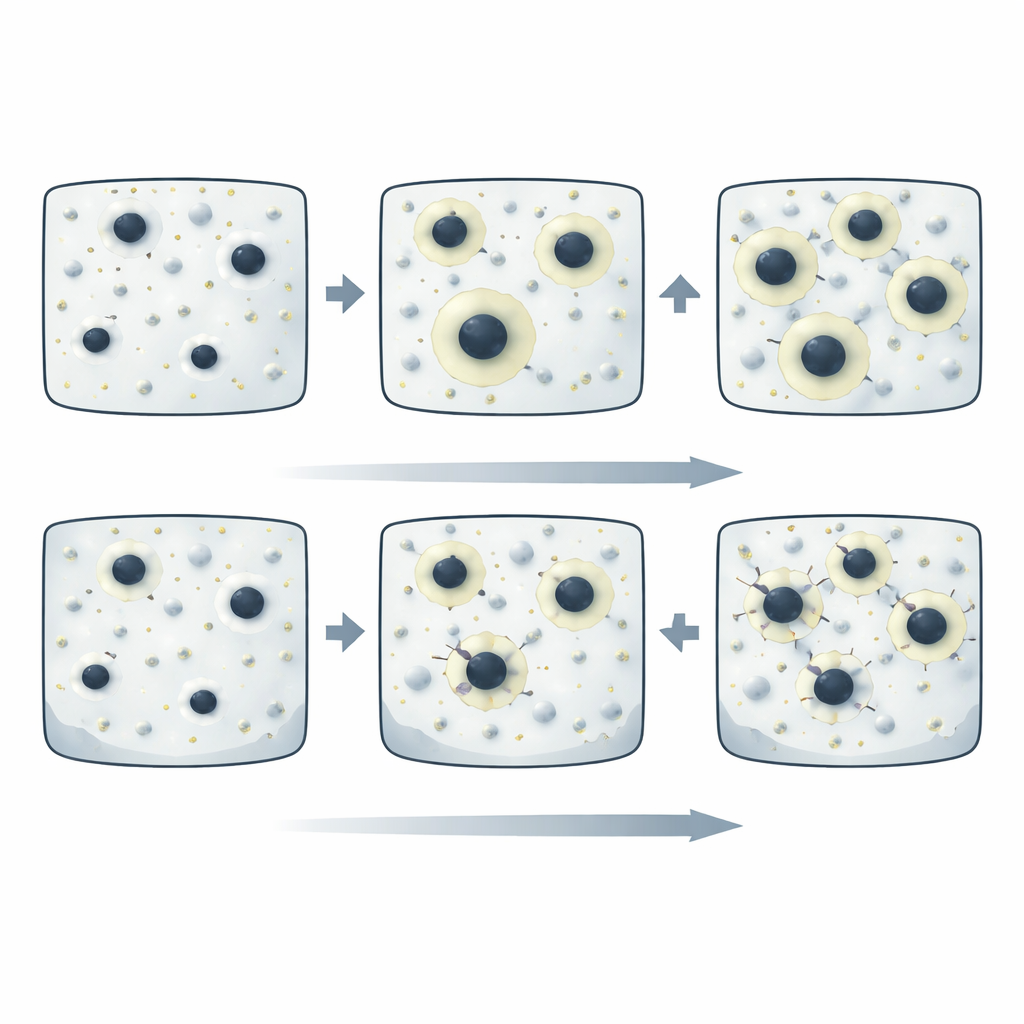
Cómo el control del enfriamiento supera al metal ultra‑puro
La idea clave de este trabajo es que el comportamiento frente a la corrosión está dictado menos por la cantidad de hierro presente y más por cómo se dispone ese hierro dentro del metal. Con una pequeña adición de calcio y un enfriamiento lo bastante lento —más lento que aproximadamente 5 kelvin por segundo—, la estructura interna del metal encierra de forma natural el hierro dentro de compuestos benignos. Estas jaulas bloquean los pequeños “cortocircuitos” electroquímicos que de otro modo provocarían un ataque rápido. En estas condiciones, la simple aleación magnesio‑calcio supera incluso al magnesio de ultra‑alta pureza en soluciones salinas agresivas, partiendo de materias primas comerciales más baratas.
Qué significa esto para usos en el mundo real
Para ingenieros y fabricantes, el estudio ofrece una receta práctica: en lugar de depender únicamente de magnesio crudo extremadamente limpio y caro, pueden ajustar tanto la composición de la aleación como las condiciones de colada para neutralizar impurezas dañinas. Añadiendo una traza de calcio y usando procesos de colada que mantengan las velocidades de enfriamiento lo bastante bajas para formar partículas encapsulantes, es posible producir componentes de magnesio ligeros que duran mucho más en entornos corrosivos. Esta estrategia podría beneficiar desde piezas automotrices y ánodos para almacenamiento de energía hasta dispositivos médicos biodegradables, donde una corrosión controlada y predecible es esencial.
Cita: Qi, Y., Deng, M., Rong, J. et al. Achieving a corrosion-resistant Mg-Ca lean alloy by solidification control to sequester parts-per-million-level Fe impurity. npj Mater Degrad 10, 41 (2026). https://doi.org/10.1038/s41529-026-00755-2
Palabras clave: aleaciones de magnesio, resistencia a la corrosión, microaleación, velocidad de enfriamiento de la solidificación, materiales ligeros