Clear Sky Science · es
Inhibición de la corrosión por picaduras en acero inoxidable mediante NaNO3: perspectivas mecanísticas sobre la disolución de sulfuros, despasivación y disolución activa
Por qué importan las pequeñas manchas de óxido
Desde puentes y rascacielos hasta automóviles y plantas químicas, el acero inoxidable se elige porque normalmente resiste el óxido. Sin embargo, bajo ciertas condiciones puede aparecer de forma abrupta pequeños orificios profundos llamados picaduras que pueden propagarse hasta convertirse en grietas peligrosas. Este estudio plantea una pregunta práctica para la industria: ¿puede un químico común y relativamente seguro —el nitrato de sodio— impedir que esas picaduras se inicien, y si es así, cómo lo hace? La respuesta podría ayudar a mantener la infraestructura crítica más segura durante más tiempo empleando aditivos asequibles y menos dañinos para el medio ambiente. 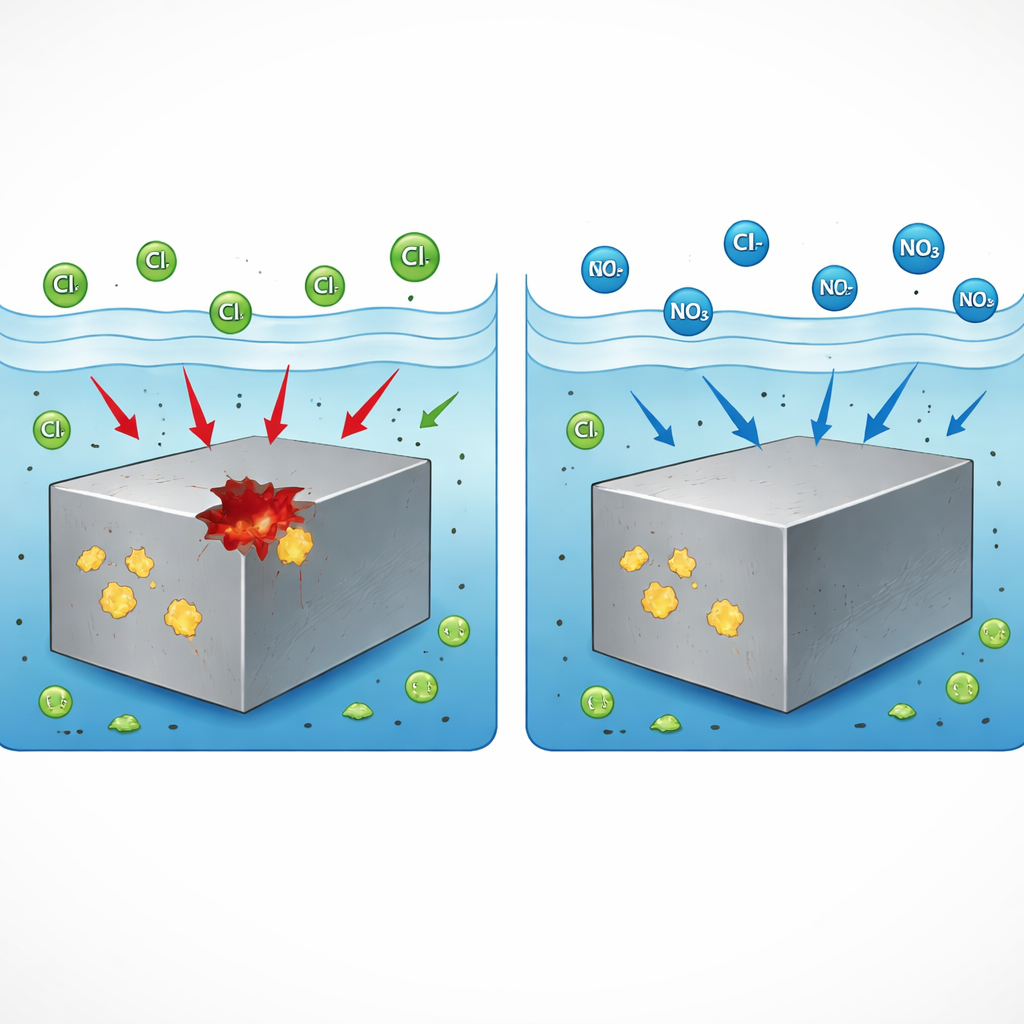
Puntos débiles ocultos dentro del acero inoxidable
Incluso los mejores aceros inoxidables no son perfectamente homogéneos. Diseminadas en su interior hay partículas microscópicas ricas en azufre, conocidas como inclusiones de sulfuro. Dos tipos importantes se basan en manganeso (MnS) y calcio (CaS). Estas inclusiones actúan como puntos débiles incorporados donde las picaduras tienden a iniciarse cuando el metal entra en contacto con agua que contiene cloruros, como la niebla salina o el agua de refrigeración. Trabajos previos mostraron que la formación de picaduras sigue un guion consistente: la partícula de sulfuro comienza a disolverse, la película protectora del acero cercana se rompe y entonces el metal circundante empieza a disolverse rápidamente, excavando una picadura. El estudio actual compara dos aceros inoxidables comerciales del tipo 304 —uno dominado por inclusiones ricas en MnS y otro por inclusiones basadas en CaS— para entender si el nitrato puede interrumpir este proceso en uno o ambos tipos de puntos débiles.
Evaluando aditivos comunes en agua salada
Los investigadores sumergieron los aceros en una solución salina simple y forzaron lentamente al metal hacia condiciones más corrosivas mientras observaban cuándo se formaban picaduras estables. Compararon tres aditivos a concentraciones realistas: amonio, nitrito y nitrato, todos como sales sódicas o amoniacales. Solo el nitrato tuvo un efecto notable. En ambos aceros, rico en MnS y rico en CaS, la adición de una cantidad modesta de nitrato de sodio impidió completamente la formación de picaduras estables en el rango probado, mientras que los otros dos aditivos no ofrecieron mejora. La microscopía confirmó que, sin nitrato, las picaduras efectivamente se iniciaban en inclusiones de sulfuro, mientras que con nitrato esas inclusiones dejaron de provocar orificios dañinos. Esto mostró que el nitrato es un inhibidor de picaduras eficaz de forma general para distintos tipos de sulfuros, no solo un caso particular. 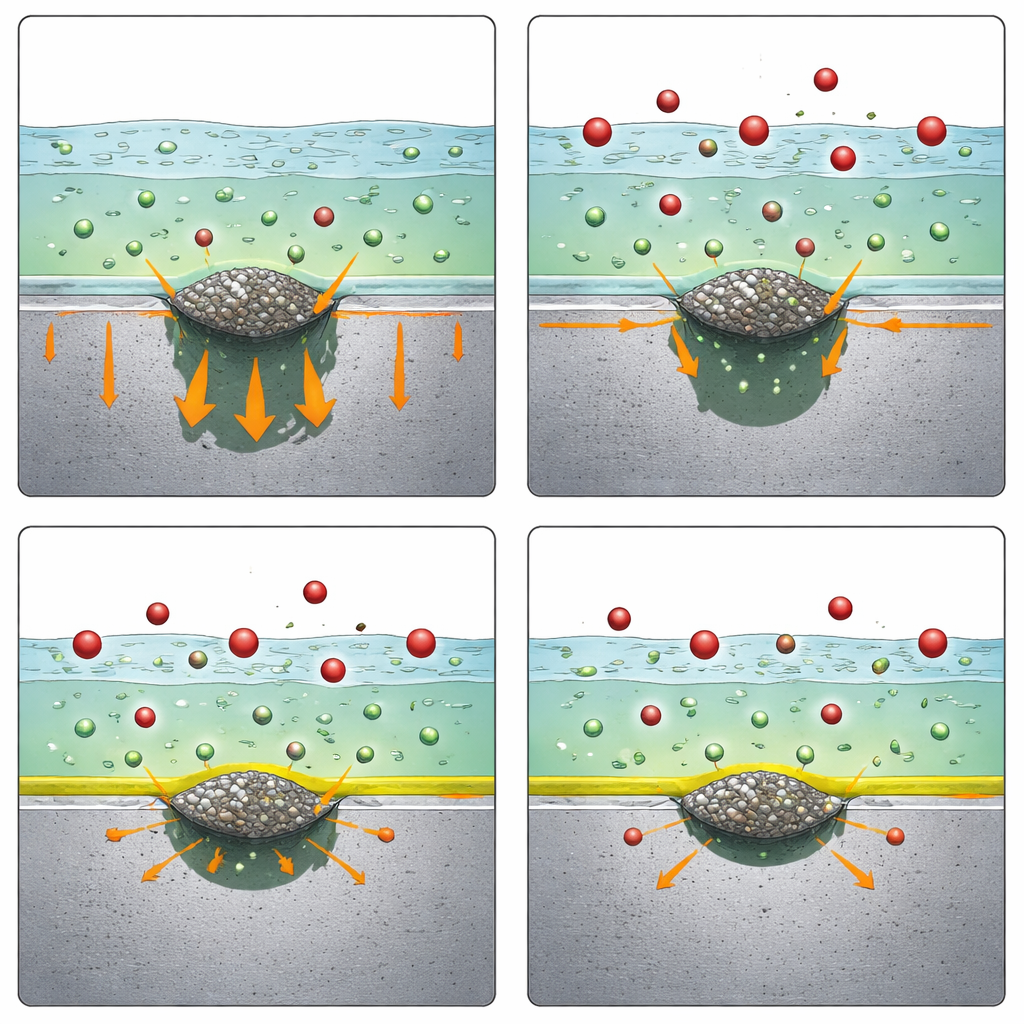
Observando en detalle lo que el nitrato cambia —y lo que no
Para precisar cómo actúa el nitrato, el equipo examinó las etapas iniciales de la formación de picaduras alrededor de partículas individuales de MnS usando microelectrodos e imágenes de alta resolución. Observaron que el nitrato no impedía que las partículas de MnS se disolvieran, ni alteraba las pequeñas zanjuelas que se forman en la interfaz entre la inclusión y el acero circundante. Tampoco cambió el nivel de acidez al que la película protectora del acero falla en solución clorurada. Todo ello indicó que los primeros pasos de la iniciación de la picadura —el debilitamiento y la alteración alrededor de la inclusión— continúan de forma muy similar en presencia de nitrato.
Ralentando la fase final de pérdida de metal
La diferencia crucial apareció cuando los investigadores recrearon el ambiente agresivo dentro de una picadura ya formada: condiciones muy ácidas y ricas en cloruros. Usando soluciones de ácido concentrado que imitan la química en el fondo de las picaduras, encontraron que el acero normalmente presenta dos oleadas distintas de disolución rápida del metal al aumentar el potencial. La adición de nitrato redujo de forma consistente la primera oleada de disolución, tanto en ácido simple como en ácido que también contenía especies de azufre similares a las liberadas por la disolución de MnS. Las observaciones de superficie mostraron un ataque más uniforme pero a una tasa claramente menor. Pruebas adicionales, variando la acidez y los niveles de cloruro, sugirieron que el efecto del nitrato no puede explicarse simplemente por diluir la acidez, desplazar cloruros o estabilizar costras salinas. En cambio, los resultados apuntan a que el nitrato ayuda al cromo del aleado a formar una capa superficial estabilizadora que, a su vez, ralentiza la fase temprana y más crítica de pérdida activa de metal.
Qué significa esto para los aceros en el mundo real
En pocas palabras, el nitrato no impide las primeras muescas químicas en pequeñas partículas de sulfuro dentro del acero inoxidable, pero sí ralentiza la fase final descontrolada en la que una imperfección inocua se transforma en una picadura peligrosa. Al amortiguar ese estallido de pérdida de metal en microambientes ácidos y salinos, el nitrato de sodio mantiene el acero más cercano a un estado pasivo y auto-protector, incluso cuando están presentes inclusiones de sulfuro e iones cloruro. Dado que el nitrato es relativamente económico, menos tóxico que muchas alternativas y ya se utiliza en sistemas industriales de agua, entender este mecanismo refuerza el argumento para su uso cuidadoso como aditivo de control de la corrosión para prolongar la vida útil de estructuras y equipos de acero inoxidable.
Cita: Amatsuka, S., Nishimoto, M. & Muto, I. Pitting-corrosion inhibition in stainless steel by NaNO3: mechanistic insights on sulfide dissolution, depassivation, and active dissolution. npj Mater Degrad 10, 40 (2026). https://doi.org/10.1038/s41529-026-00753-4
Palabras clave: corrosión del acero inoxidable, inhibición de picaduras, nitrato de sodio, inclusiones de sulfuro, soluciones cloruradas