Clear Sky Science · es
Efecto de los procesos electroquímicos de tratamiento del agua sobre la corrosión del acero al carbono en el sistema de abastecimiento urbano
Por qué importan las tuberías de su grifo
Los sistemas de tratamiento electroquímico del agua son cada vez más comunes en las ciudades porque eliminan contaminantes con eficacia, ablandan el agua y eliminan gérmenes. Pero las mismas reacciones eléctricas que limpian el agua también pueden corroer de forma silenciosa los metales de las tuberías que llevan esa agua a nuestros hogares. Este estudio examina cómo ese tratamiento afecta al acero al carbono, un material de tubería habitual, y explica por qué la corrosión puede acelerarse notablemente cuando la electricidad interactúa con la química cotidiana del agua del grifo.
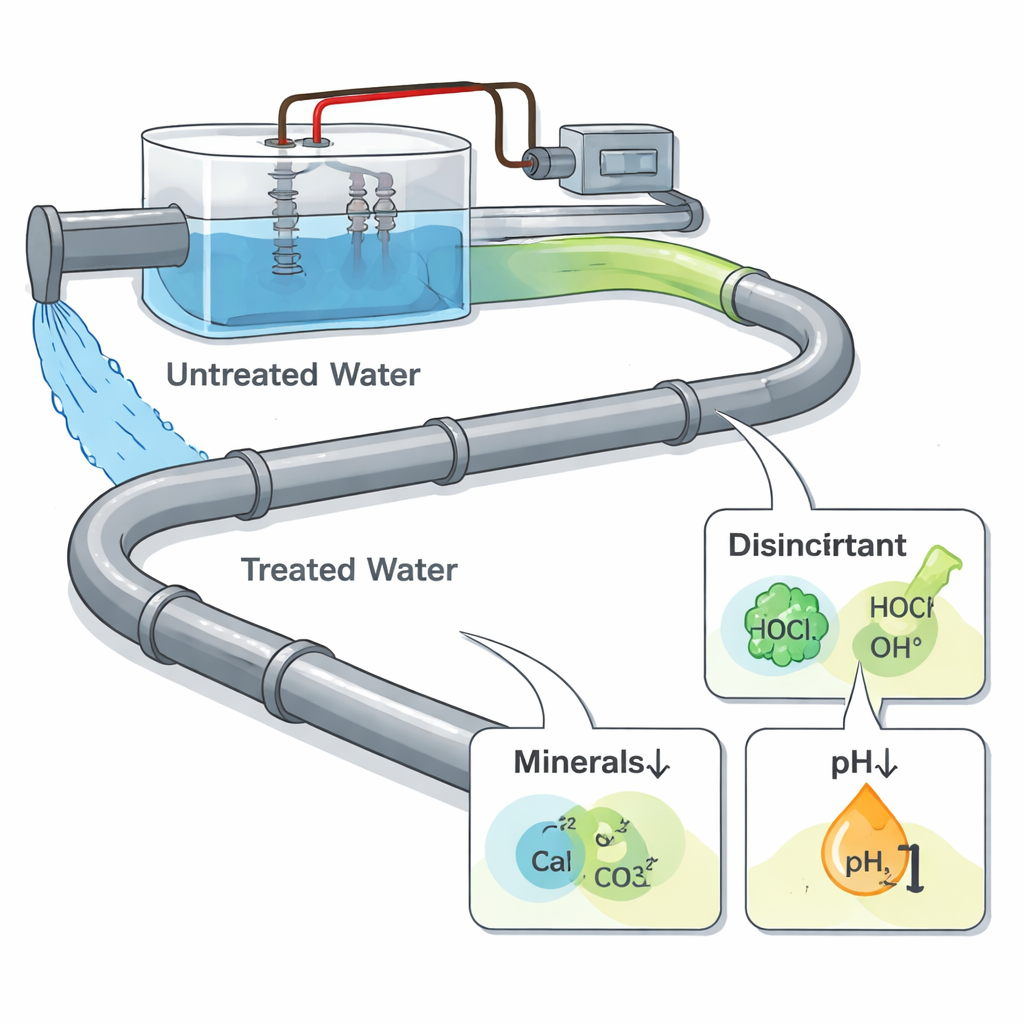
Limpiar el agua con electricidad
El tratamiento electroquímico del agua hace pasar una corriente eléctrica por el agua utilizando placas metálicas llamadas electrodos. Esto puede eliminar iones indeseados, descomponer contaminantes orgánicos y generar desinfectantes, lo que hace que el proceso sea atractivo para sistemas urbanos e industriales. A diferencia del tratamiento tradicional, sin embargo, las tuberías en sí no están conectadas al sistema eléctrico: solo reciben el agua tratada que sale de la unidad. Eso significa que cualquier corrosión adicional no se debe a la electricidad golpeando directamente la tubería, sino a cambios en la química del agua: nuevos agentes oxidantes para la desinfección, variaciones de acidez y movimiento de iones minerales que normalmente ayudan a formar capas protectoras en el interior de las tuberías.
Pérdida de metal más rápida y daños ocultos más profundos
Los investigadores realizaron un experimento de 90 días con agua real de ciudad, exponiendo muestras de acero al carbono a diferentes voltajes de 0 a 9 voltios, y luego siguieron la pérdida de masa, el daño superficial y el comportamiento electroquímico. Encontraron que incluso en los primeros tres días, activar la electrólisis empeoraba la corrosión, y a mayor voltaje siempre había más daño. A 9 voltios, la tasa de corrosión general aumentó más de 25 veces en comparación con el agua que no pasó por el proceso eléctrico. Usando escaneos superficiales 3D, también mostraron que las pequeñas picaduras en el metal crecían mucho más en profundidad conforme aumentaba el voltaje. Bajo el voltaje más alto, las picaduras más profundas eran casi cinco veces más profundas que en agua no tratada, reduciendo drásticamente la vida útil esperada del acero incluso si la pérdida media de metal no parecía extrema.
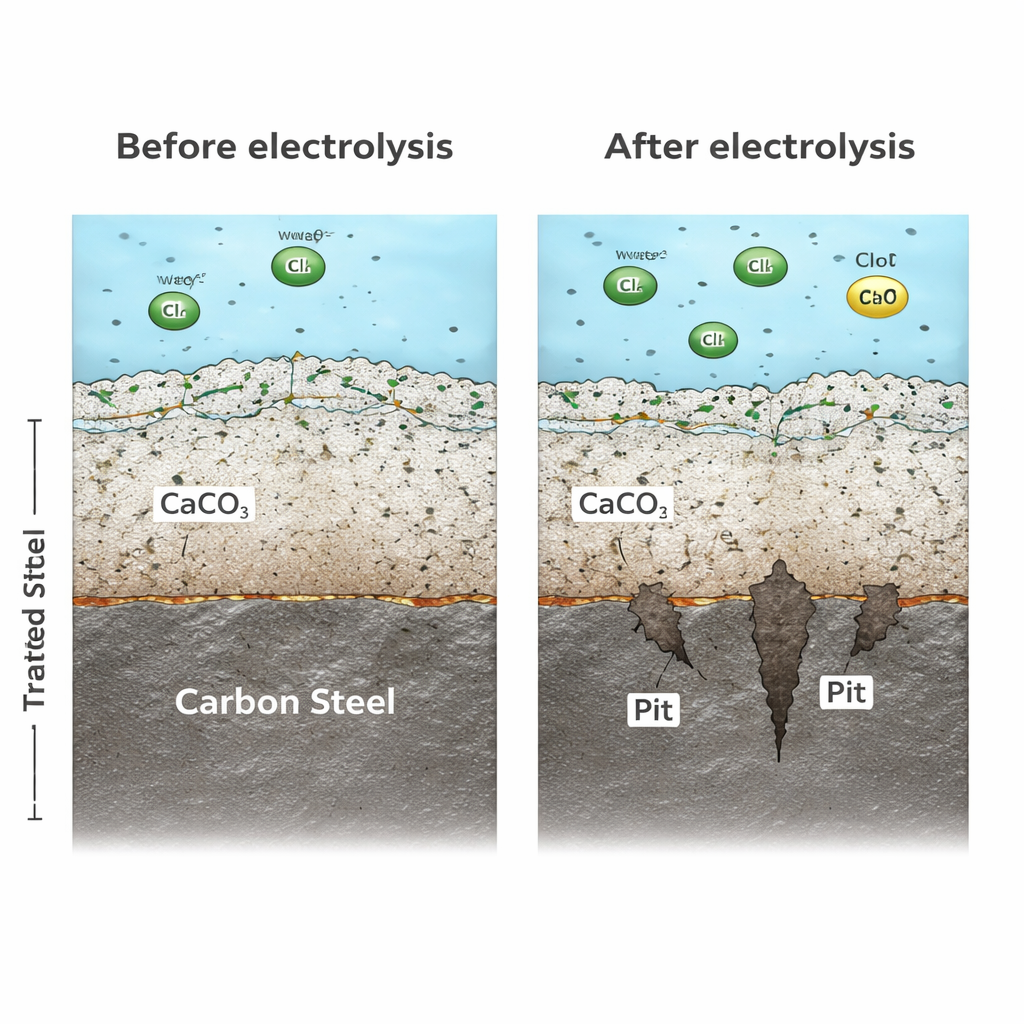
Por qué fallan las capas protectoras
En el interior de muchas tuberías, los minerales presentes en el agua forman de manera natural una capa delgada y densa que ayuda a proteger el metal. En el agua sin tratar, el carbonato de calcio cumple ese papel protector. Sin embargo, en el agua tratada electroquímicamente, esa protección mineral desaparece en gran medida. Porque el cátodo en la unidad de tratamiento atrae iones de calcio y carbonato y favorece su deposición allí, quedan menos de esos iones disponibles para formar un escudo sólido en las paredes de la tubería. Pruebas con microscopía y difracción revelaron que, en lugar de una barrera densa rica en minerales, el acero en agua tratada desarrolló una capa de óxido suelta y porosa con cristales pequeños e inestables. Este recubrimiento débil permitió que especies corrosivas y electrones se movieran con facilidad, de modo que la corrosión se mantuvo rápida en lugar de ralentizarse con el tiempo.
Un ataque químico más agresivo en el agua
Para identificar qué impulsaba el ataque adicional, el equipo separó distintos factores. Cuando hicieron electrólisis en una solución sulfática sin cloruro, los subproductos de la disociación del agua —como oxígeno, hidrógeno y radicales de corta vida— apenas cambiaron el comportamiento de corrosión del acero. Pero cuando estaba presente el cloruro, el ion común en las sales y muchas aguas, la situación cambió. La electrólisis convirtió parte del cloruro en hipoclorito, un desinfectante más reactivo. Pruebas electroquímicas mostraron que a medida que aumentaba la corriente, el acero se volvía mucho más fácil de corroer en soluciones con cloruro. Simulaciones por ordenador respaldaron esto: el hipoclorito redujo la barrera energética para que los átomos de hierro abandonen la superficie metálica, facilitando la progresión de la corrosión más que con cloruro solo. Al mismo tiempo, la rápida formación de productos de óxido consumió iones hidroxilo, empujando el agua hacia un pH más bajo, es decir, condiciones más ácidas, que favorecen aún más la corrosión.
Qué significa esto para los sistemas de agua
Para quienes no son especialistas, la conclusión es que limpiar y desinfectar el agua con electricidad no es automáticamente benigno para las tuberías que la transportan. En sistemas donde el agua contiene cloruro, el tratamiento electroquímico puede transformar parte de ese cloruro en un desinfectante más fuerte y corrosivo mientras elimina los ingredientes minerales necesarios para formar protección natural. El resultado es un adelgazamiento más rápido del metal y picaduras más profundas que pueden acortar la vida útil de las tuberías y aumentar el riesgo de fugas o contaminación. Los autores sugieren que los diseñadores y operadores de estos sistemas consideren la corrosión como una preocupación central de diseño: limitar el voltaje, reducir el cloruro antes del tratamiento, elegir electrodos que generen menos subproductos agresivos y monitorizar la picadura y la química del agua a largo plazo, para garantizar que un agua más limpia no suponga el coste de una infraestructura que falle.
Cita: Zhao, S., Jing, Y., He, X. et al. Effect of electrochemical water treatment processes on carbon steel corrosion in urban water supply system. npj Mater Degrad 10, 23 (2026). https://doi.org/10.1038/s41529-026-00736-5
Palabras clave: tratamiento electroquímico del agua, corrosión del acero al carbono, tuberías de agua urbanas, cloruro e hipoclorito, durabilidad de la infraestructura hídrica