Clear Sky Science · es
La expresión de genes diana del receptor de estrógenos β revela nuevas funciones represoras en el cáncer de mama agresivo
Por qué importa esta investigación
El cáncer inflamatorio de mama es una de las formas más agresivas y letales de cáncer de mama, que a menudo se disemina rápidamente y deja a las pacientes con pocas opciones de tratamiento dirigidas. Este estudio explora un sensor hormonal menos conocido en las células mamarias, denominado receptor de estrógenos beta, y muestra cómo puede actuar como un freno natural a la diseminación tumoral. Comprender cómo funciona este freno integrado podría abrir la puerta a nuevos fármacos que ralenticen o prevengan la metástasis en pacientes que actualmente tienen muy pocas alternativas.
Una cara distinta del cáncer inflamatorio de mama
A diferencia de muchos cánceres de mama que dependen del receptor de estrógenos clásico alfa, el cáncer inflamatorio de mama suele carecer de esta molécula y, por tanto, no responde bien a las terapias hormonales estándar. Los autores se centran en cambio en un segundo receptor de estrógenos, el receptor de estrógenos beta (ERβ), que previamente habían vinculado a menos metástasis tanto en pacientes como en modelos murinos. Trabajos anteriores sugerían que ERβ frena el andamiaje interno y la maquinaria de movimiento celular. En este estudio, el equipo se propuso mapear, a lo largo del genoma, cómo ERβ modifica la actividad génica y qué moléculas downstream podrían explicar su papel protector y anti‑metastásico.
Leyendo el manual de instrucciones de la célula cancerosa
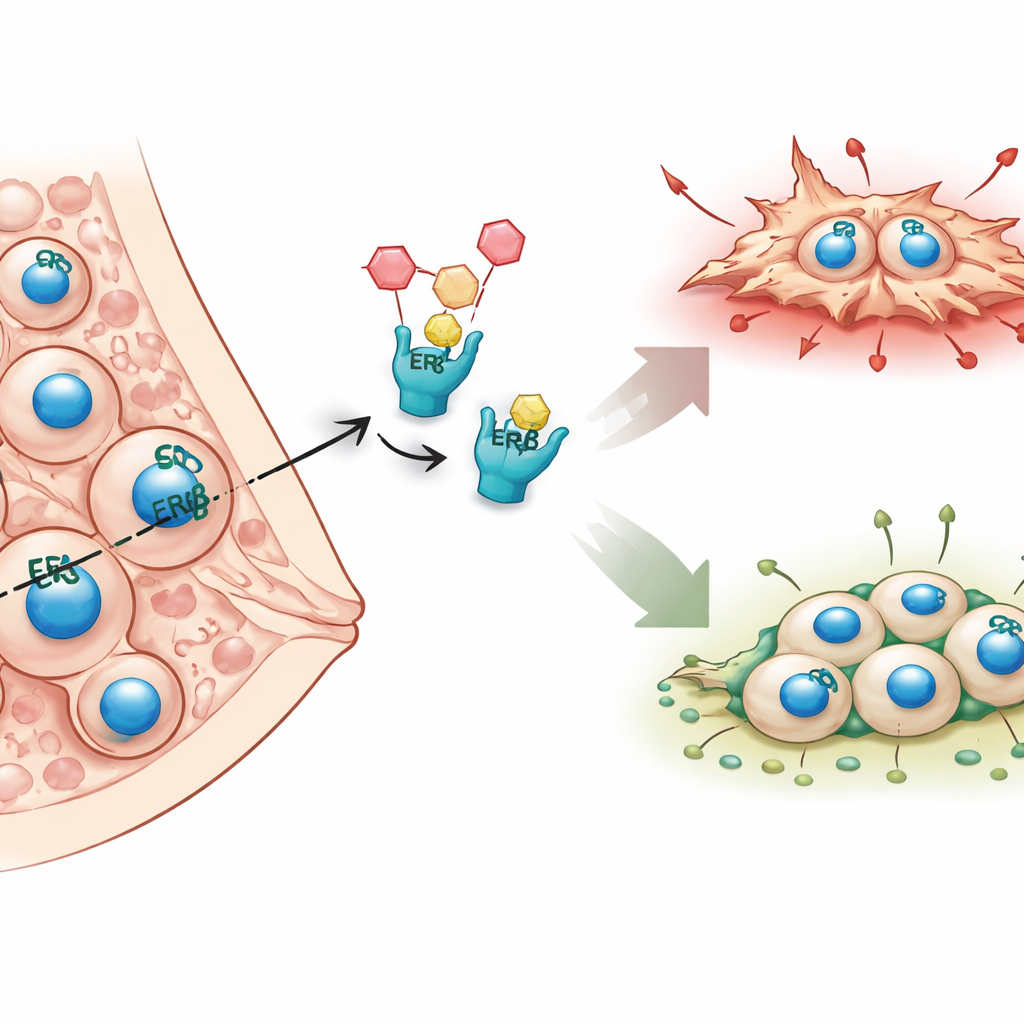
Para desvelar la influencia de ERβ, los investigadores emplearon dos potentes enfoques de secuenciación en líneas celulares de cáncer inflamatorio de mama. Un método, ChIP‑seq, señala exactamente dónde se fija ERβ en el ADN, como marcando páginas y líneas específicas del manual de instrucciones celular. El otro método, RNA‑seq, mide qué genes se activan o reprimen cuando ERβ está presente, ausente o activado por un fármaco selectivo. Al comparar estos conjuntos de datos, hallaron miles de sitios de ADN unidos por ERβ, la mayoría no sólo en los interruptores de encendido y apagado génico sino dentro o entre genes, lo que sugiere un control de amplio alcance. También descubrieron que ERβ frecuentemente actúa junto a familias de otros factores de transcripción, formando complejos que colectivamente deciden qué genes se silencian o activan.
Reconfigurando crecimiento, movimiento y metabolismo
El análisis integrado mostró que ERβ tiende a atenuar genes que promueven el movimiento celular, los cambios de forma y la invasión, especialmente aquellos vinculados al citoesqueleto de actina y a la señalización de las GTPasas Rho, vías conocidas por impulsar la metástasis. Al mismo tiempo, ERβ apoya programas génicos relacionados con el desarrollo tisular y la diferenciación celular, empujando a las células cancerosas hacia un estado más asentado y menos agresivo. El estudio también reveló un papel sorprendente de ERβ en la modulación de vías metabólicas, particularmente las que implican ácidos grasos y fosfolípidos, componentes clave como combustible y bloques de construcción para tumores de rápido crecimiento. Es importante que estos efectos se observaron no sólo en células modificadas para sobreexpresar ERβ sino también en células con niveles naturales del receptor, lo que subraya su relevancia en el mundo real.
Pequeños mensajeros de ARN y repercusión clínica
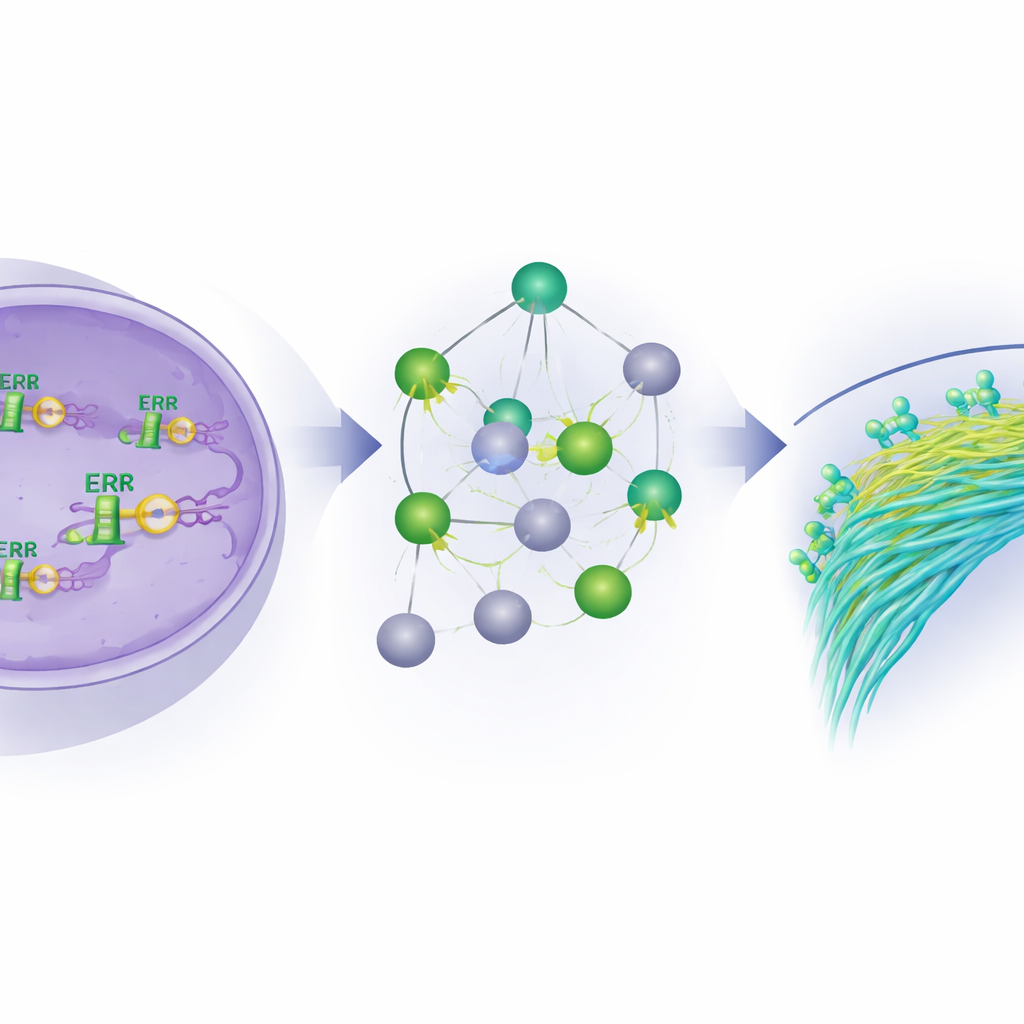
Más allá de los genes codificadores de proteínas, el equipo examinó microARNs —pequeñas moléculas de ARN que afinan la expresión génica. Encontraron docenas de microARNs cuyos niveles cambiaron cuando ERβ fue eliminado o restaurado, muchos de los cuales se han vinculado a la supresión tumoral en el cáncer de mama. Al conectar estos microARNs con sus genes diana, los autores mostraron que ERβ controla indirectamente a algunos conductores del cáncer a través de una red reguladora por capas. A continuación, analizaron datos de pacientes, examinando tumores de individuos con cáncer de mama inflamatorio y no inflamatorio. Varios genes controlados por ERβ se asociaron fuertemente con la supervivencia de las pacientes: niveles altos de algunos (como SERPINA1 y HSPB8) predijeron mejores resultados, mientras que niveles elevados de otros (como PITX1 y HOMER3) se vincularon a una peor supervivencia. Esto sitúa a estas moléculas downstream como posibles marcadores pronósticos y como futuros dianas terapéuticas.
Del freno molecular a futuras terapias
En conjunto, el estudio presenta a ERβ como un freno central sobre el comportamiento invasivo de las células del cáncer inflamatorio de mama. Al unirse al ADN, asociarse con otros reguladores y moldear tanto las redes de genes como las de microARNs, ERβ silencía programas que impulsan la migración celular y la metástasis, al tiempo que promueve estados más estables y diferenciados y reorienta el metabolismo del cáncer. Para las pacientes, esto sugiere que fármacos que activen ERβ o inhiban sus principales dianas downstream —especialmente las implicadas en el movimiento celular y el uso de ácidos grasos— podrían servir como base para nuevos tratamientos más precisos contra esta enfermedad de difícil manejo.
Cita: Tastsoglou, S., Karagounis, I.V., Miliotis, M. et al. Estrogen receptor β target gene expression reveals novel repressive functions in aggressive breast cancer. npj Breast Cancer 12, 38 (2026). https://doi.org/10.1038/s41523-026-00905-4
Palabras clave: cáncer inflamatorio de mama, receptor de estrógenos beta, metástasis, regulación génica, metabolismo del cáncer