Clear Sky Science · es
La señalización de CD52 a través de Siglec‑G de los macrófagos representa un objetivo terapéutico para la inmunoterapia del cáncer
Por qué algunos cánceres de mama se ocultan del sistema inmunitario
El cáncer de mama triple negativo es una de las formas más peligrosas de cáncer de mama porque se disemina con rapidez y carece de muchos de los blancos terapéuticos habituales. Este estudio explora una vía recién descubierta por la que estos tumores pueden eludir las defensas del organismo y muestra cómo bloquear esa ruta de escape podría mejorar la eficacia de las terapias basadas en el sistema inmune.
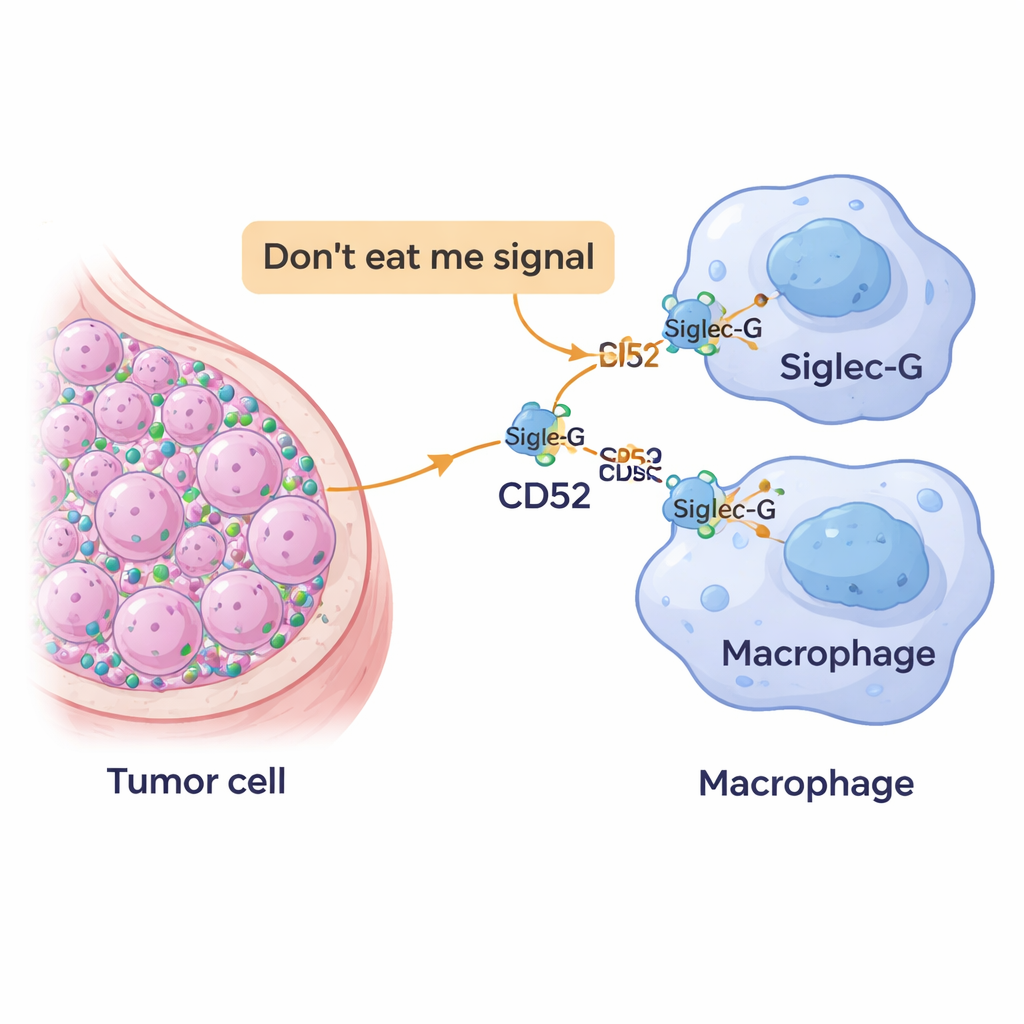
Una nueva bandera de “no me comas” en las células cancerosas
Nuestro sistema inmunitario depende de células fagocíticas llamadas macrófagos que patrullan los tejidos y se tragan células peligrosas o anormales. Para evitar ser destruidas por error, las células sanas muestran marcadores en su superficie que señalan, en esencia, “pertenezco aquí”. Las células cancerosas con frecuencia secuestran este sistema sobreexpresando esas señales protectoras, convirtiéndolas en potentes banderas de “no me comas”. Los investigadores se centraron en una molécula llamada CD52, ya conocida en cánceres hematológicos y enfermedades autoinmunes, y se preguntaron si las células tumorales mamarias también la usan para escapar del ataque de los macrófagos.
Detección de CD52 en tumores mamarios agresivos
El equipo analizó grandes bases de datos públicas de cáncer y muestras de tejido de pacientes. Encontraron que los tumores mamarios, especialmente los triple negativos, producían más CD52 que el tejido mamario normal. Además, los tumores con mayor CD52 tendían a estar menos diferenciados, una característica a menudo asociada con una enfermedad más agresiva. Al mismo tiempo, las células inmunitarias dentro y alrededor de los tumores presentaban altos niveles de una molécula compañera llamada Siglec‑10 (y su contraparte en ratón Siglec‑G), que se expresa en los macrófagos y puede enviar señales calmantes al interior de estas células. En conjunto, estos patrones sugerían que CD52 en las células tumorales podría estar comunicándose directamente con Siglec‑G en los macrófagos para impedir que cumplieran su función.
Apagar CD52 para liberar a los macrófagos
Para probar esta hipótesis, los científicos utilizaron herramientas de edición genética para eliminar CD52 de células de cáncer de mama triple negativo de ratón. Cuando estas células modificadas se mezclaron con macrófagos en el laboratorio, los macrófagos fagocitaron significativamente más células tumorales que cuando se enfrentaban a células cancerosas no modificadas. Es importante destacar que las propias células cancerosas no crecieron ni murieron de forma diferente tras perder CD52, lo que indica que el efecto clave estaba en el reconocimiento inmunitario más que en la biología intrínseca del tumor. Cuando las mismas células tumorales se implantaron en ratones, las que carecían de CD52 formaron tumores más pequeños y estaban rodeadas por macrófagos que mostraban más evidencia de haber ingerido células cancerosas. Si se depletaban los macrófagos de los ratones, esta ventaja en el crecimiento desaparecía, confirmando que el papel principal de CD52 era proteger a los tumores de ser devorados.
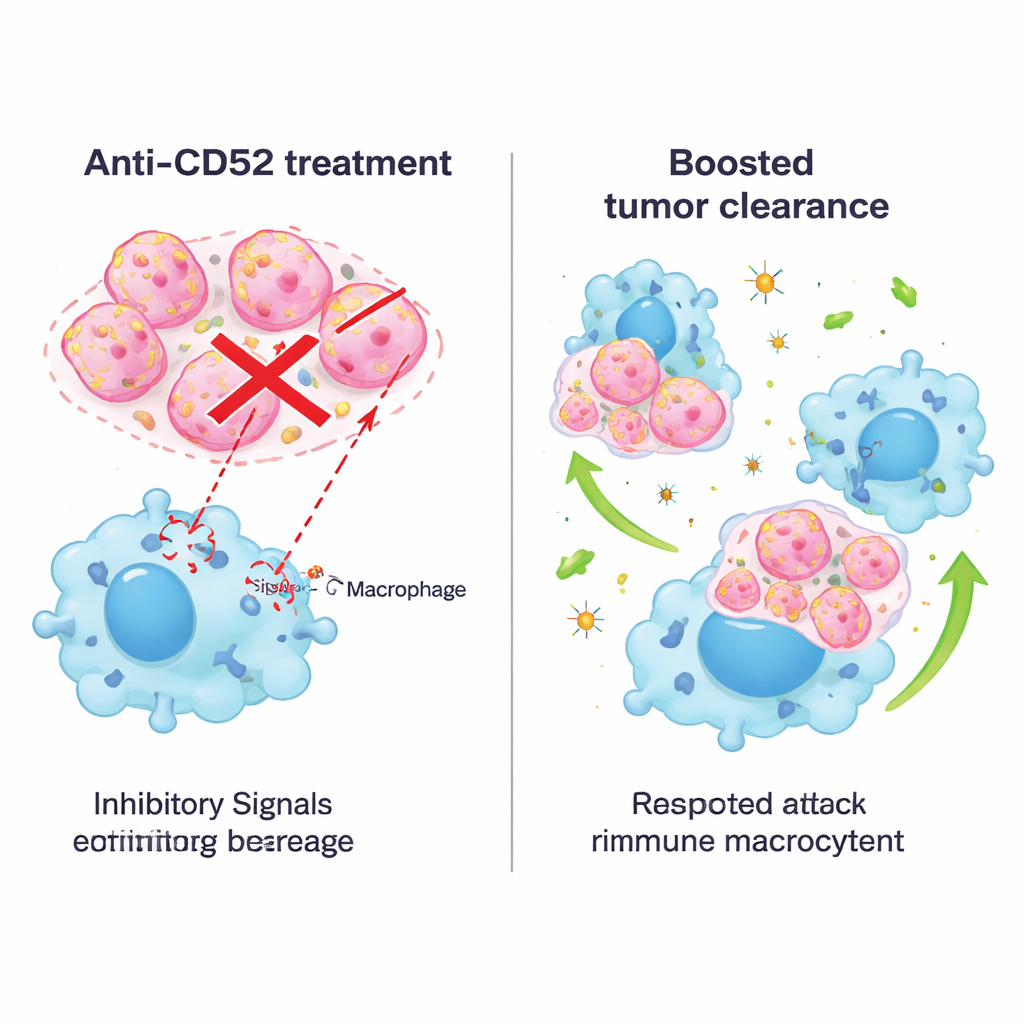
Bloquear la señal con anticuerpos y combinar tratamientos
Dado que ya existen fármacos dirigidos contra CD52 en otras enfermedades, los investigadores probaron a continuación un anticuerpo bloqueante en modelos murinos. El tratamiento de ratones portadores de tumores con un anticuerpo anti‑CD52 redujo el crecimiento tumoral, prolongó la supervivencia y no causó daños orgánicos evidentes ni pérdida de peso. En cultivos, anticuerpos similares aumentaron la capacidad tanto de macrófagos de ratón como de humanos para engullir células de cáncer de mama de varios subtipos, no solo triple negativo. El equipo combinó entonces el bloqueo de CD52 con terapia anti‑PD‑1, un fármaco de punto de control ampliamente usado dirigido a las células T. En un modelo murino espontáneo de cáncer de mama triple negativo, la combinación funcionó mejor que cada tratamiento por separado: los tumores se redujeron más, los macrófagos se volvieron más inflamatorios y activos, y más células T con alto potencial citotóxico penetraron en el tumor mientras que disminuía la proporción de células T agotadas.
Qué supone esto para el tratamiento futuro del cáncer de mama
Este trabajo descubre a CD52 como una señal de “no me comas” hasta ahora no reconocida que las células de cáncer de mama triple negativo usan para repeler a los macrófagos. Al interrumpir la conversación entre CD52 en las células tumorales y Siglec‑G en los macrófagos, los investigadores consiguieron reactivar tanto a las células del sistema inmune innato como, de forma indirecta, a las células T, especialmente al combinarlo con bloqueo de PD‑1. Aunque hacen falta más estudios de seguridad y ensayos clínicos —porque CD52 también aparece en muchas células inmunitarias normales—, los hallazgos apuntan a una estrategia prometedora de doble punto de control que podría ayudar a convertir tumores mamarios difíciles de tratar y resistentes al sistema inmune en otros que respondan mejor a la inmunoterapia.
Cita: Qin, X., Chang, Y., Qiu, Y. et al. CD52 signaling via macrophage Siglec-G represents a therapeutic target for cancer immunotherapy. npj Breast Cancer 12, 29 (2026). https://doi.org/10.1038/s41523-026-00895-3
Palabras clave: cáncer de mama triple negativo, macrófagos, inmunoterapia, CD52, bloqueo de puntos de control