Clear Sky Science · es
Coentrega de la quimiocina CXCL9 y del ligando cosimulador TNFSF9 por células madre mesenquimales reprograma el microambiente inmune contra el cáncer de mama triple negativo
Por qué importa este nuevo enfoque contra el cáncer de mama
El cáncer de mama triple negativo es una de las formas más peligrosas de este tumor porque crece rápido, se disemina pronto y carece de los dianas hormonales habituales en las que confían muchos fármacos. La inmunoterapia ha levantado esperanzas, pero en muchos pacientes las células defensoras del organismo simplemente no penetran en el tumor en número suficiente para marcar la diferencia. Este estudio explora una estrategia ingeniosa: usar células vivas como “camiones de reparto” guiados que llevan señales que estimulan la respuesta inmune directamente a tumores difíciles de tratar, lo que podría permitir que más pacientes sean candidatos a tratamientos inmunológicos potentes.
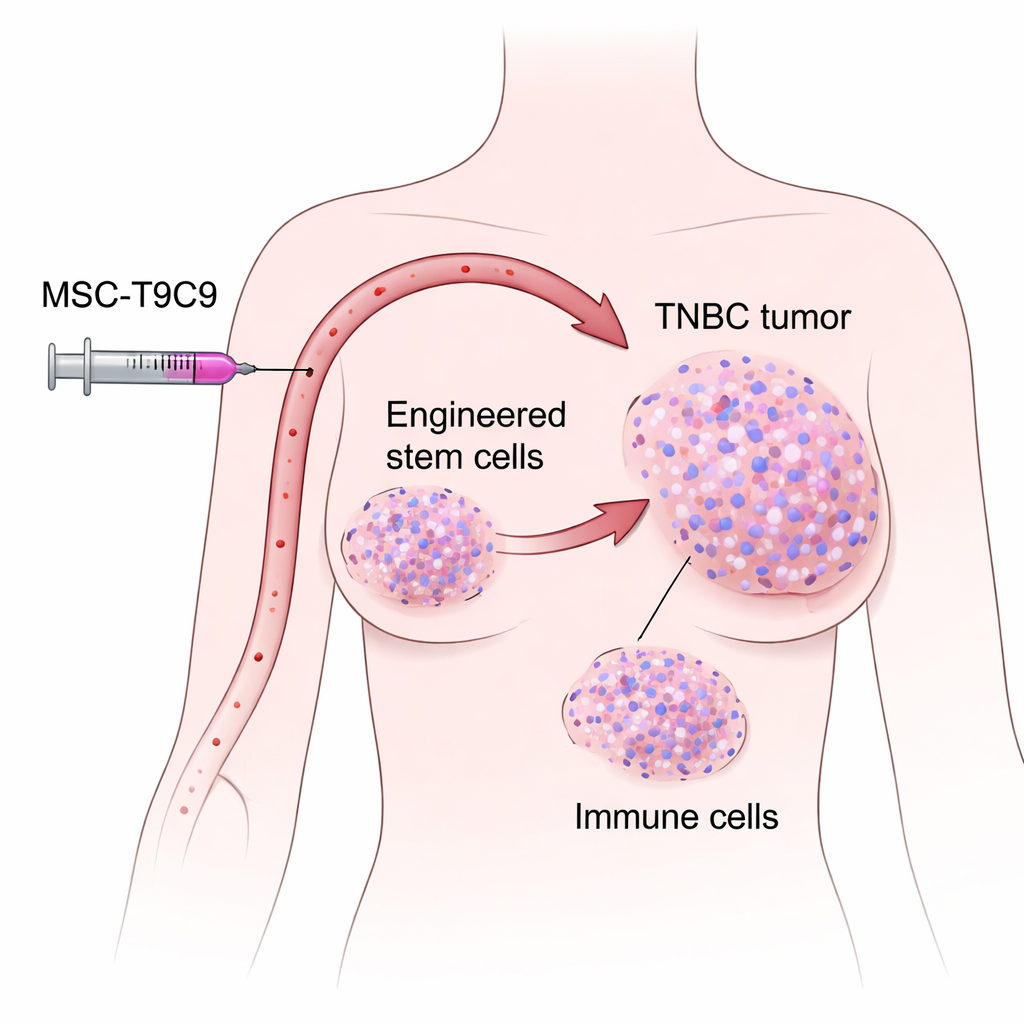
Un cáncer difícil con poca ayuda inmune
Los tratamientos estándar para el cáncer de mama triple negativo —cirugía, quimioterapia y radiación— a menudo no evitan la recaída, y la supervivencia media en enfermedad avanzada sigue siendo inferior a dos años. Una razón clave es que muchos de estos tumores son “fríos”, es decir, contienen pocas células inmunitarias que combatan el cáncer. Grandes bases de datos de pacientes mostraron que las personas cuyos tumores producen de forma natural mayores cantidades de dos moléculas relacionadas con la inmunidad, CXCL9 y TNFSF9, tienden a vivir más y a tener más células T y células asesinas naturales (NK) dentro de sus tumores. CXCL9 es una señal química que atrae células inmunitarias al tejido, mientras que TNFSF9 actúa como un interruptor adicional que ayuda a que esas células ataquen con más fuerza. El patrón sugería que elevar ambas señales directamente dentro de los tumores podría inclinar la balanza a favor del sistema inmune.
Convertir células madre en camiones de reparto inteligentes
Los investigadores se centraron en células madre mesenquimales extraídas de cordones umbilicales humanos donados. Estas células tienen una propiedad útil: cuando se inyectan en el torrente sanguíneo de ratones con tumores mamarios, se dirigen de forma natural a los sitios tumorales y permanecen allí durante días, evitando en gran medida órganos normales. El equipo modificó genéticamente estas células madre para que liberaran CXCL9 y mostraran TNFSF9 en su superficie, creando una terapia celular de doble función que denominaron MSC‑T9C9. Las pruebas de laboratorio mostraron que las células modificadas secretaban altos niveles de CXCL9 y activaban con fuerza las células T y NK de ratón, sin cambiar su propio comportamiento proliferativo ni provocar tumores por sí mismas. Esto las convirtió en candidatas prometedoras como potenciadores inmunitarios dirigidos.
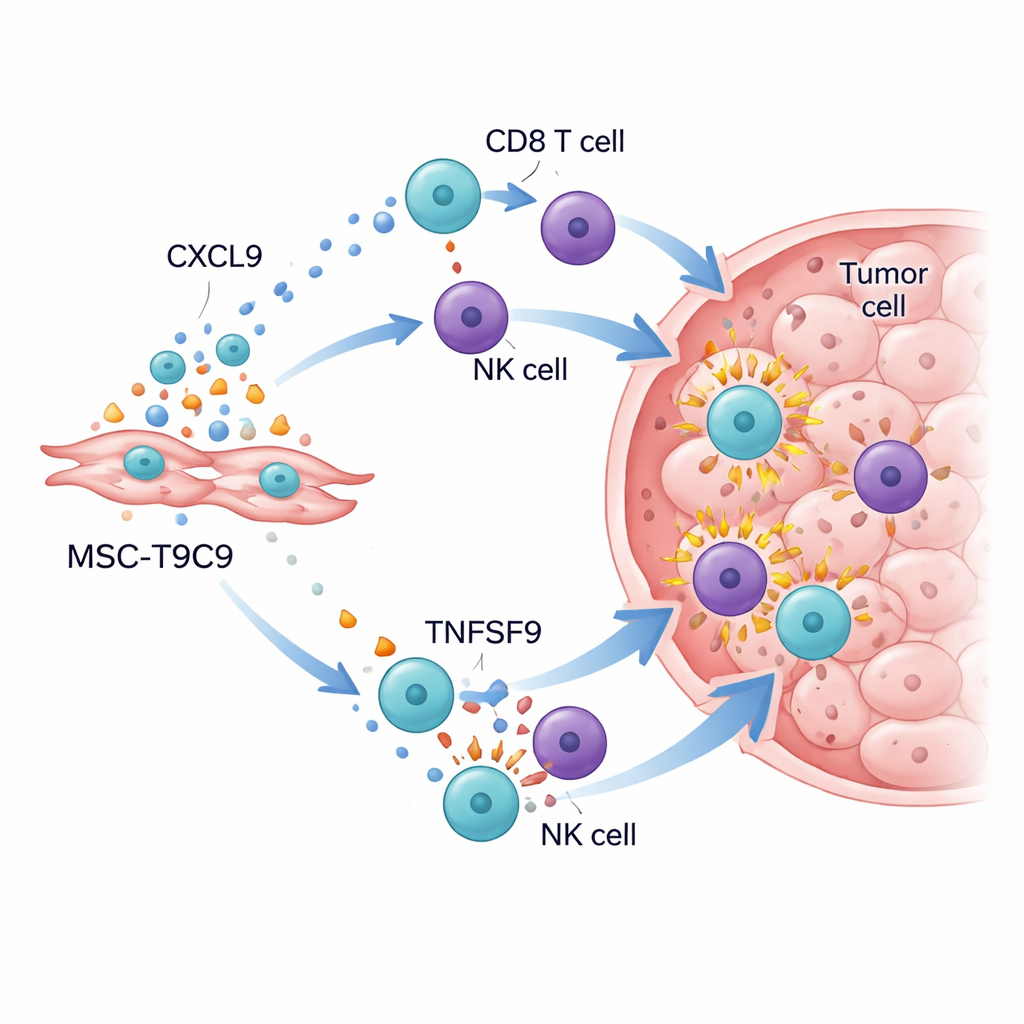
Despertar el campo de batalla inmune del tumor
Cuando las células modificadas se administraron a ratones portadores de tumores de mama triple negativo, los resultados fueron llamativos. En ratones con un sistema inmune funcional, inyecciones repetidas de MSC‑T9C9 frenaron mucho el crecimiento tumoral e incrementaron la muerte de células cancerosas, mientras que las células madre de control tuvieron poco efecto. El análisis detallado de los tumores mostró un aumento dramático en el número de células T CD8 “asesinas” y de células NK, junto con niveles más altos de moléculas de ataque potentes como la granzima B, el interferón‑γ, el factor de necrosis tumoral‑α y la interleucina‑2. Al mismo tiempo, el entorno tumoral se desplazó lejos de un estado supresor: aumentaron los macrófagos inflamatorios beneficiosos y, aunque las células T reguladoras seguían presentes, quedaron superadas en número por la nueva oleada de combatientes. En ratones inmunodeficientes, donde faltan las células T y NK, MSC‑T9C9 no ralentizó el crecimiento tumoral, lo que confirma que su beneficio depende de movilizar las defensas del propio organismo.
Preparar los tumores para la terapia con inhibidores de puntos de control
Los fármacos inmunoterapéuticos modernos, como los anticuerpos anti‑PD‑1, liberan los “frenos” moleculares de las células T, pero funcionan mejor cuando ya hay suficientes células T dentro del tumor. El estudio encontró que MSC‑T9C9 no solo atraía más células T CD8 al tumor, sino que también las empujaba a un estado altamente activo, aunque sensible a los frenos, marcado por el receptor PD‑1. En un modelo murino, la combinación de MSC‑T9C9 con un fármaco anti‑PD‑1 produjo la mayor reducción tumoral y la supervivencia más prolongada en comparación con cualquiera de los tratamientos por separado. Los análisis de conjuntos de datos de cáncer humano respaldaron esta idea: los pacientes con niveles combinados más altos de TNFSF9 y CXCL9 eran más propensos a beneficiarse de terapias que bloquean los puntos de control, lo que sugiere que la misma biología podría aplicarse en personas.
Seguridad y promesa futura
Cualquier tratamiento que potencie la inmunidad suscita preocupaciones sobre efectos secundarios peligrosos, como inflamación generalizada o daño orgánico. De forma alentadora, los ratones que recibieron MSC‑T9C9 mantuvieron peso y comportamiento normales, no mostraron lesiones evidentes en órganos principales y presentaron análisis de sangre y pruebas hepáticas‑renales normales. Es importante que el aumento de la actividad inmune se confinara en gran medida al propio tumor, y las señales inflamatorias en la circulación no se elevaron. Aunque hacen falta más estudios antes de ensayos en humanos —incluyendo pruebas en modelos más realistas y una cuidadosa determinación de dosis—, este trabajo sugiere que guiar células madre modificadas hasta los tumores para atraer y activar células inmunitarias podría ofrecer una forma dirigida y más segura de convertir los cánceres de mama triple negativo “fríos” en “calientes” y más sensibles a la inmunoterapia.
Cita: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Palabras clave: cáncer de mama triple negativo, inmunoterapia, células madre mesenquimales, microambiente tumoral, bloqueo de puntos de control