Clear Sky Science · es
La interleucina-1α de origen hostil impulsa la inmunosupresión tumoral al reprogramar las células mieloides asociadas al tumor
Por qué esta investigación importa para las pacientes con cáncer
La inmunoterapia ha transformado el tratamiento de ciertos cánceres, pero muchos tumores de mama siguen evadiendo al sistema inmune. Este artículo explora a un culpable menos conocido: una molécula de señalización llamada interleucina‑1 alfa (IL‑1α) producida no por las células tumorales, sino por células normales del organismo. Los autores muestran que la IL‑1α de origen hostil puede, de forma silenciosa, convertir a células inmunitarias en aliadas del tumor, y que bloquear esta señal en ratones puede provocar que los tumores mamarios se reduzcan o desaparezcan. Comprender este interruptor podría ayudar a los médicos a diseñar tratamientos que hagan la inmunoterapia más eficaz frente al cáncer de mama.
Un influyente oculto en el vecindario tumoral
Los cánceres no crecen aisladamente; viven en un “vecindario” concurrido de células inmunitarias, vasos sanguíneos y tejido conectivo conocido como microambiente tumoral. Entre los residentes más importantes están las células mieloides, especialmente los macrófagos, que pueden atacar a los tumores o protegerlos. Los manuales clásicos dividen los macrófagos en M1 (combaten el tumor) y M2 (lo apoyan), pero los tumores reales contienen muchos matices intermedios. Los autores se centraron en la IL‑1α, una molécula normalmente producida por tejidos no cancerosos, para preguntar si esta señal del huésped orienta a los mieloides entrantes hacia funciones útiles o dañinas dentro de los tumores de mama.
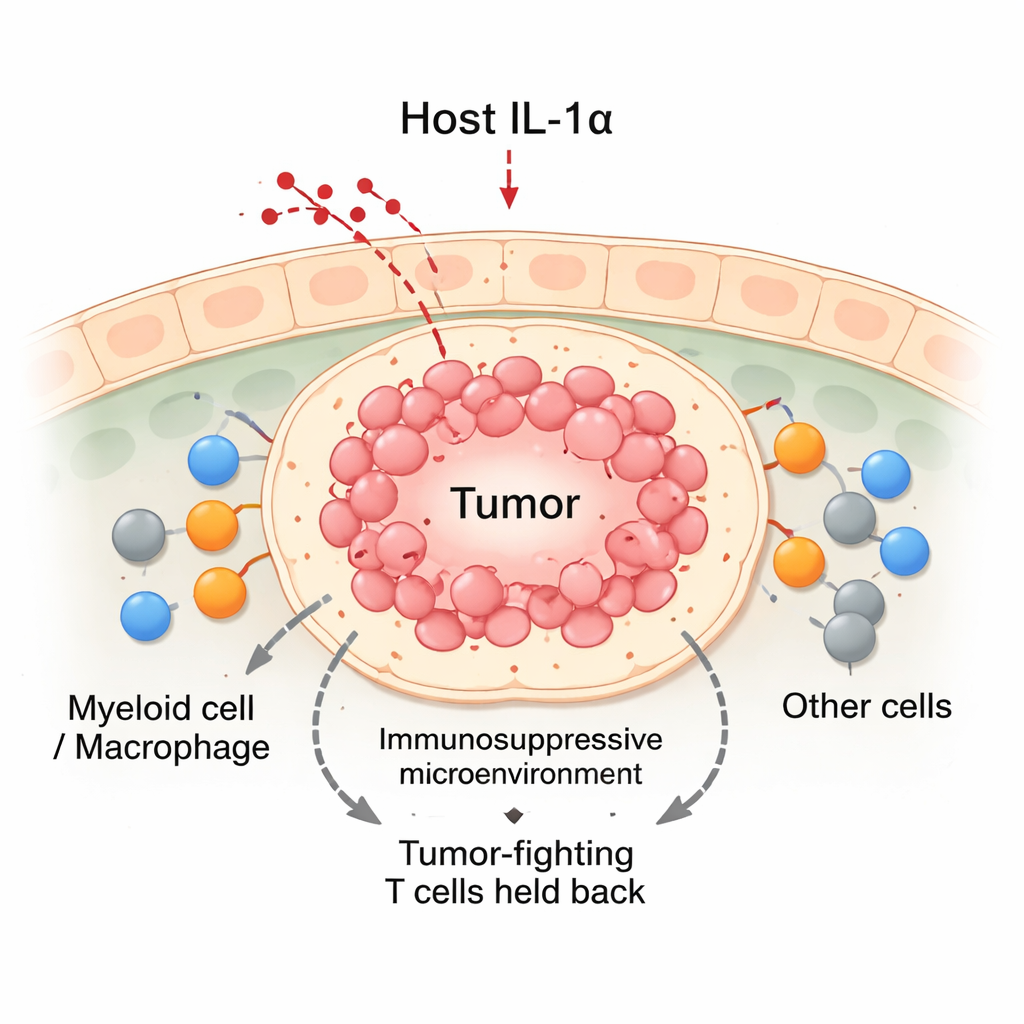
Apagar la IL‑1α inclina la balanza contra los tumores
Usando modelos murinos de cáncer de mama, el equipo comparó animales normales con otros modificados genéticamente para carecer de IL‑1α. Al trasplantar células tumorales mamarias en las glándulas mamarias, los tumores en ratones normales crecieron de forma sostenida. En contraste, los tumores en ratones deficientes en IL‑1α crecieron durante aproximadamente dos semanas y luego con frecuencia regrédieron. Estos tumores en regresión contenían más células inmunitarias en conjunto, incluidos un aumento de células T CD8 “asesinas” y de células mieloides. Aunque los ratones sin IL‑1α tenían menos leucocitos circulantes en sangre, concentraron muchas más células inmunitarias en el sitio tumoral. Los análisis detallados mostraron que las células T CD8 infiltrantes en los tumores sin IL‑1α estaban más activas, producían mayores niveles de moléculas citotóxicas y mostraban menos signos de agotamiento.
Cómo la IL‑1α remodela las células mieloides asociadas al tumor
Para entender qué hacía la IL‑1α a nivel celular, los investigadores emplearon secuenciación de ARN de célula única para examinar miles de células individuales del tumor. Descubrieron que solo un subconjunto pequeño de macrófagos asociados al tumor —aquellos marcados por un receptor llamado CX3CR1— producía IL‑1α. En ratones normales, muchos monocitos entrantes maduraban hasta convertirse en estos macrófagos CX3CR1‑positivos, asociados a un comportamiento inmunosupresor. En ratones carentes de IL‑1α, esta ruta de maduración se vio interrumpida. En su lugar, las células mieloides tendían a convertirse en macrófagos inflamatorios iNOS‑positivos, un perfil ligado a la actividad antitumoral. Funcionalmente, las células mieloides de tumores sin IL‑1α eran menos capaces de inducir frenos como PD‑1 y CTLA‑4 en las células T, y mostraban menor capacidad para amortiguar la proliferación de células T.
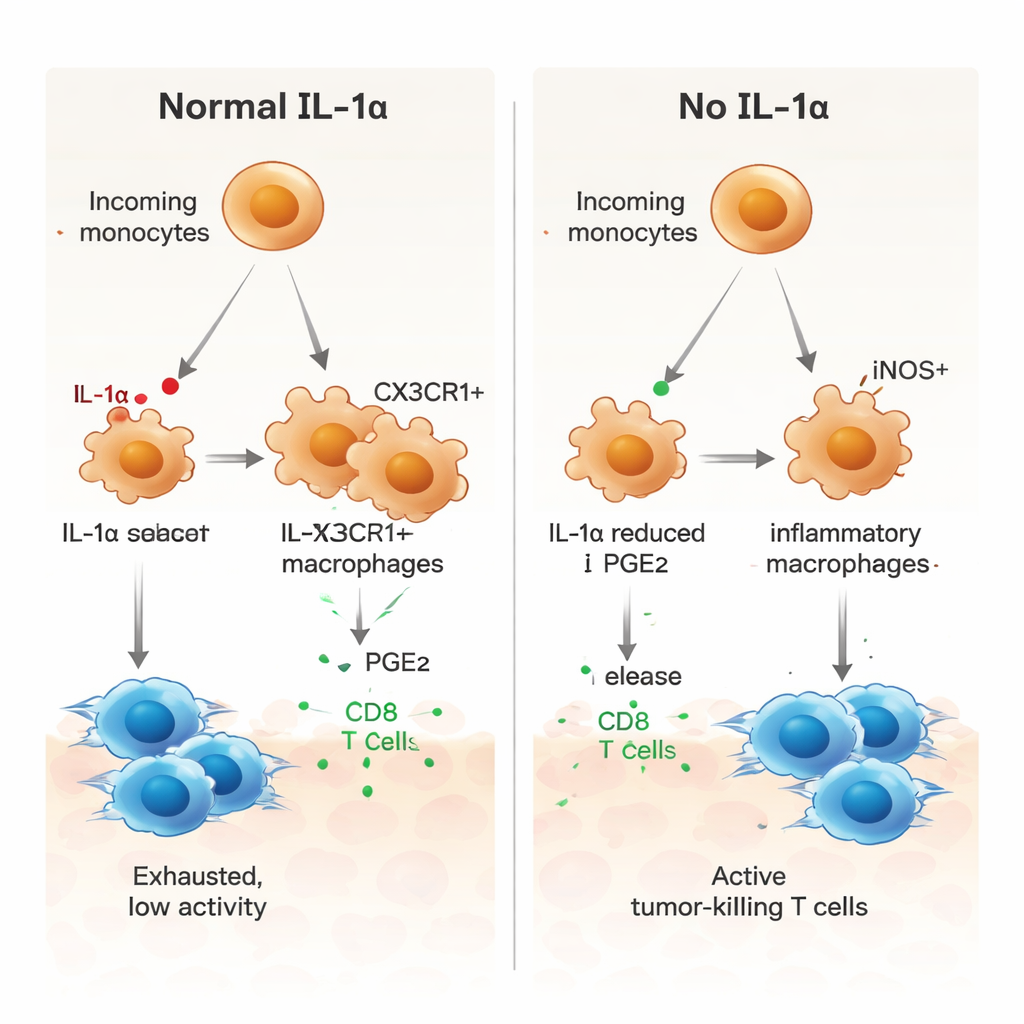
Un papel clave para un mensajero lipídico, la PGE2
Los autores preguntaron entonces cómo impulsa la IL‑1α a las células mieloides hacia un estado que apoya al tumor. El análisis de comunicación de los datos de célula única señaló varias vías de señalización, incluida una que involucra a la prostaglandina E2 (PGE2), un mediador lipídico conocido por promover la supresión inmune. En los tumores carentes de IL‑1α, los macrófagos expresaban niveles más bajos de receptores para el factor de crecimiento de macrófagos (M‑CSF), receptores de TGF‑β y un receptor de PGE2, y las células estromales cercanas producían menos de las enzimas que generan PGE2. En cultivos de laboratorio, los macrófagos derivados de médula ósea de ratones deficientes en IL‑1α mostraron un perfil más inflamatorio, con mayor iNOS y menor CX3CR1. Añadir PGE2 revirtió este cambio y restauró un patrón más supresor, mientras que bloquear PGE2 en macrófagos normales los empujó hacia un estado proinflamatorio. Los macrófagos sin IL‑1α también estimularon con más fuerza la proliferación de células T CD8 específicas del tumor, efecto que se atenuó al reponer PGE2.
Puenteando los hallazgos en ratones con la inmunidad humana
Para determinar si sus datos murinos reflejan la biología humana, el equipo comparó firmas génicas de los distintos subconjuntos de macrófagos de ratón con un amplio panel de células mieloides humanas induci das hacia varios estados en el laboratorio. Los clústeres de macrófagos de tumores en ratones normales se asemejaban a células humanas empujadas hacia estados tipo M2, atenuantes de la inmunidad, por moléculas como IL‑10, IL‑4 y glucocorticoides. Por el contrario, los mismos clústeres procedentes de tumores carentes de IL‑1α coincidían con células humanas en condiciones más inflamatorias y menos supresoras. Notablemente, los patrones génicos ligados a la señalización de PGE2 estaban enriquecidos en macrófagos dependientes de IL‑1α pero ausentes cuando faltaba IL‑1α, reforzando la idea de que IL‑1α y PGE2 actúan juntos para construir un nicho inmunosupresor.
Qué podría significar esto para la futura terapia del cáncer de mama
En términos sencillos, este estudio sugiere que una molécula de origen hostil, la IL‑1α, puede indicarle discretamente a ciertos macrófagos que protejan el tumor y mantengan a raya a las células T asesinas, en parte mediante la señalización por PGE2. Cuando se elimina la IL‑1α en ratones, los macrófagos cambian hacia un estado más inflamatorio y antitumoral, las células T CD8 se activan más y los tumores mamarios trasplantados suelen ser rechazados. Dado que las inmunoterapias actuales ya pretenden reactivar a las células T agotadas, combinarlas con enfoques que bloqueen la IL‑1α o su vía downstream de PGE2 podría inclinar aún más el microambiente tumoral a favor del sistema inmune de la paciente. Aunque hacen falta más estudios para evaluar seguridad y eficacia en humanos, estos hallazgos señalan a la IL‑1α como un prometedor nuevo blanco para hacer que el cáncer de mama sea más vulnerable al ataque inmunitario.
Cita: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Palabras clave: inmunoterapia del cáncer de mama, microambiente tumoral, macrófagos, interleucina-1 alfa, prostaglandina E2