Clear Sky Science · es
Eliminación dirigida de las infecciones de mastitis por Staphylococcus aureus con sistemas sintéticos de entrega CRISPR‑Cas basados en fagos
Luchar contra una infección costosa en la industria láctea
La leche de las vacas y otros animales de granja puede verse comprometida por una dolorosa infección mamaria llamada mastitis, a menudo causada por la bacteria Staphylococcus aureus. El tratamiento de estas infecciones suele requerir cursos largos de antibióticos, que son caros, estresantes para los animales y contribuyen al creciente problema de la resistencia a los antibióticos. Este estudio explora un enfoque radicalmente distinto: convertir un parásito natural similar a un virus de las bacterias en un arma de precisión que puede cortar selectivamente el ADN de la bacteria y eliminar las infecciones sin propagar genes de resistencia.
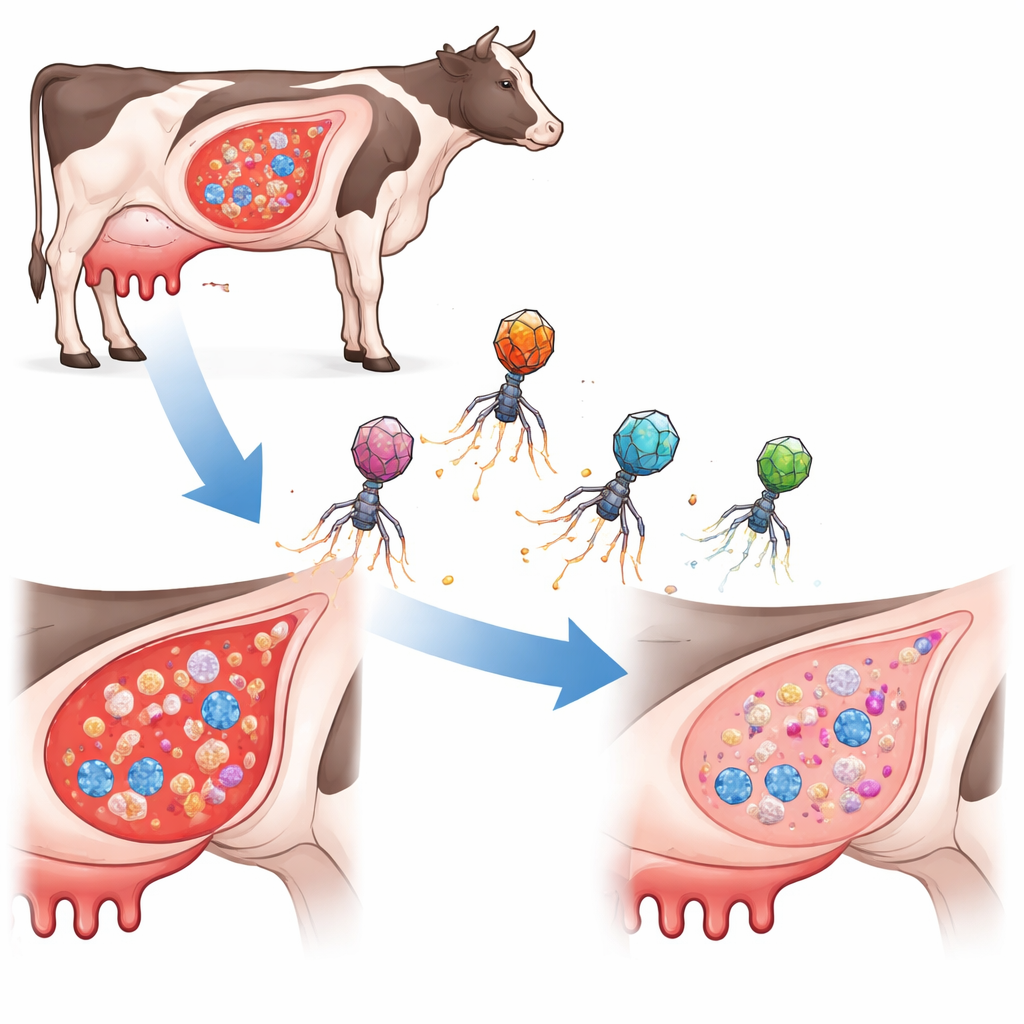
Un nuevo tipo de cazador bacteriano dirigido
En lugar de usar antibióticos tradicionales o bacteriófagos ordinarios (virus que infectan bacterias), los investigadores diseñaron pequeños elementos portadores de ADN conocidos como islas cromosómicas inducibles por fagos. En la naturaleza, estas islas viajan dentro de cápsides fagales para desplazarse entre células bacterianas. Aquí, el equipo las reconstruyó como “ePICIs” que transportan la herramienta de edición genética CRISPR‑Cas9 más secuencias guía cortas dirigidas a tres pequeños pero importantes ARN regulatorios en S. aureus. Cuando un ePICI entra en una célula objetivo, se produce Cas9 y corta el cromosoma bacteriano en el sitio elegido, matando la célula desde dentro. Crucialmente, estas partículas diseñadas no se replican por sí solas, lo que limita su propagación y reduce el riesgo de mover accidentalmente genes nocivos.
Cómo el escudo bacteriano cambia la batalla
S. aureus a menudo sobrevive al tratamiento formando biopelículas: comunidades pegajosas donde las células quedan embebidas en una matriz autogenerada. El equipo comparó dos tipos comunes de matriz: una construida principalmente a partir de una proteína llamada Bap y otra formada por un polisacárido conocido como PIA/PNAG. En pruebas de laboratorio, las biopelículas ricas en Bap protegieron fuertemente a las bacterias contra los ePICIs y contra un fago auxiliar estándar, actuando como una armadura densa que bloqueaba la infección. En contraste, las biopelículas basadas en el polisacárido hicieron que las bacterias fueran más fáciles de matar, probablemente porque las enzimas en las cápsides virales pueden degradar estos azúcares y ayudar a las partículas a alcanzar sus objetivos.
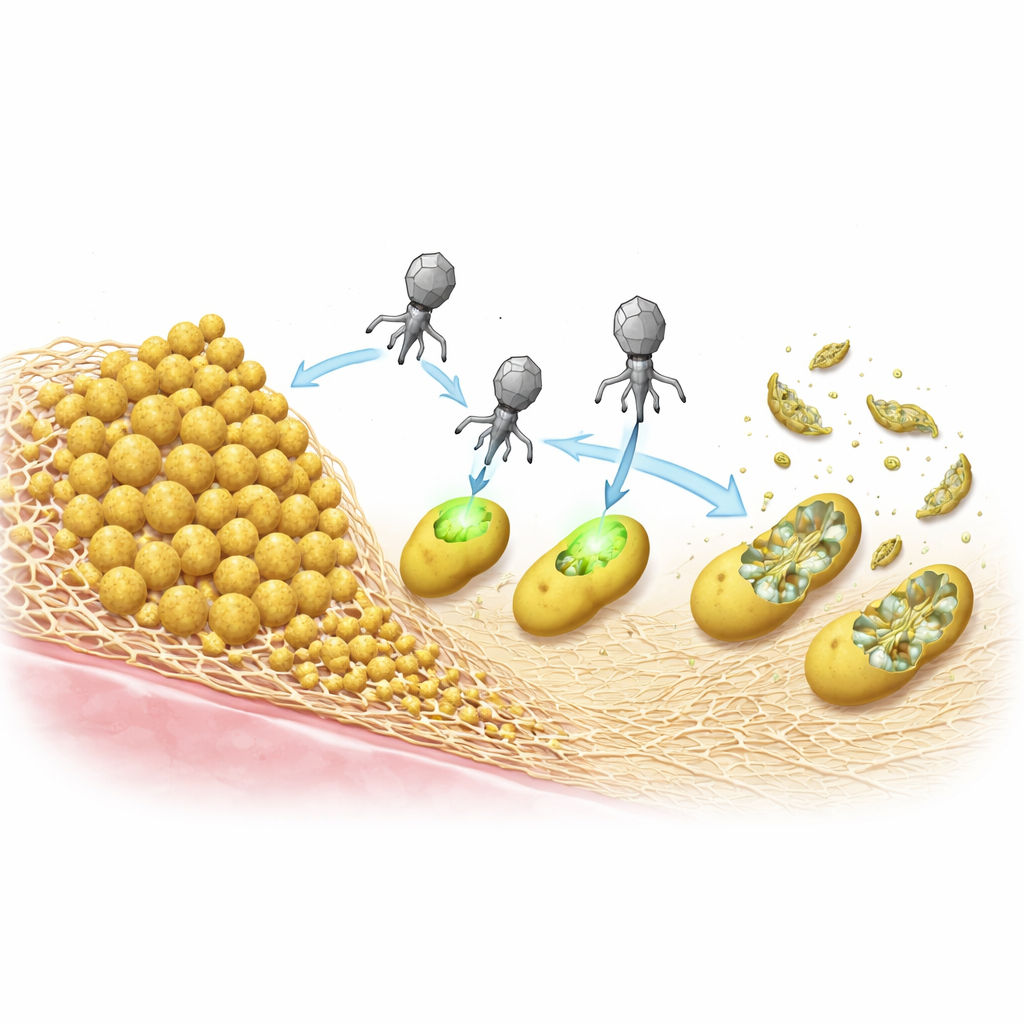
Matar bacterias sin integrarse en su ADN
Una vez dentro de la célula, los ePICIs pueden integrarse en el cromosoma bacteriano, pero los investigadores se preguntaron si ese paso es realmente necesario para matar. Crearon una versión que ya no podía integrarse y demostraron que, siempre que la partícula se produjera correctamente en la cepa origen, era igual de letal para S. aureus que la original. Esto significa que el sistema CRISPR puede expresarse directamente desde el ADN circular entrante, hacer su trabajo y luego perderse a medida que la célula muere. Esa acción sin integración reduce aún más las posibilidades de transferencia genética no deseada y diferencia a estas partículas de la terapia fagal clásica, que depende de la replicación viral y la lisis celular para propagarse.
Del plato de Petri a las glándulas mamarias infectadas
Dado que las cepas productoras de Bap son comunes en la mastitis láctea, el equipo probó su construcción de mejor rendimiento, llamada ePICIrsaE, en un modelo murino que imita la infección de la ubre. En la leche y en cultivos de laboratorio, las biopelículas ricas en Bap claramente atenuaron la actividad del ePICI. Sin embargo, dentro de la glándula mamaria, dosis repetidas de ePICIrsaE redujeron drásticamente el número de bacterias para todas las cepas probadas, incluidas las que producían Bap. Su rendimiento fue comparable al de la vancomicina, un poderoso antibiótico de última línea. Los resultados sugieren que las condiciones en el tejido vivo —como una menor producción de Bap, la presencia de bacterias flotantes o componentes útiles en la leche— permiten que las partículas diseñadas funcionen mucho mejor que en biopelículas estáticas de laboratorio.
Qué podría significar para las granjas y más allá
El estudio muestra que sistemas CRISPR no replicativos empaquetados en fagos pueden eliminar selectivamente S. aureus en una infección difícil ligada a biopelículas sin propagarse ni romper enormes cantidades de células de una vez. Aunque se necesitan dosis elevadas de partículas y la escalada de ratón a vaca será un desafío, estas partículas ofrecen una alternativa prometedora y controlable a los antibióticos para infecciones localizadas como la mastitis. Más ampliamente, el trabajo subraya que tratamientos que parecen decepcionantes en pruebas de laboratorio simples pueden aún tener éxito en el complejo entorno de un animal, y abre la puerta a bibliotecas de ePICIs personalizadas ajustadas a distintas bacterias, cápsides virales y secuencias guía.
Cita: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Palabras clave: mastitis bovina, Staphylococcus aureus, terapia CRISPR, tratamiento basado en fagos, infecciones por biopelícula