Clear Sky Science · es
La microbiota intestinal media comportamientos tipo depresión en ratones con infección crónica por Echinococcus multilocularis
Cuando una infección oculta afecta la mente
La mayoría de la gente piensa en los parásitos como un problema del intestino o del hígado, no de la mente. Sin embargo, muchos pacientes con infecciones persistentes describen ánimo bajo, fatiga y dificultades para disfrutar la vida. Este estudio explora un vínculo sorprendente: cómo una infección crónica por una tenia que se aloja en la cavidad corporal y el hígado podría, a través de cambios en las bacterias y la química intestinal, provocar comportamientos tipo depresión en ratones. Entender esta cadena de eventos podría eventualmente señalar nuevas formas de proteger la salud mental de las personas que conviven con infecciones persistentes.
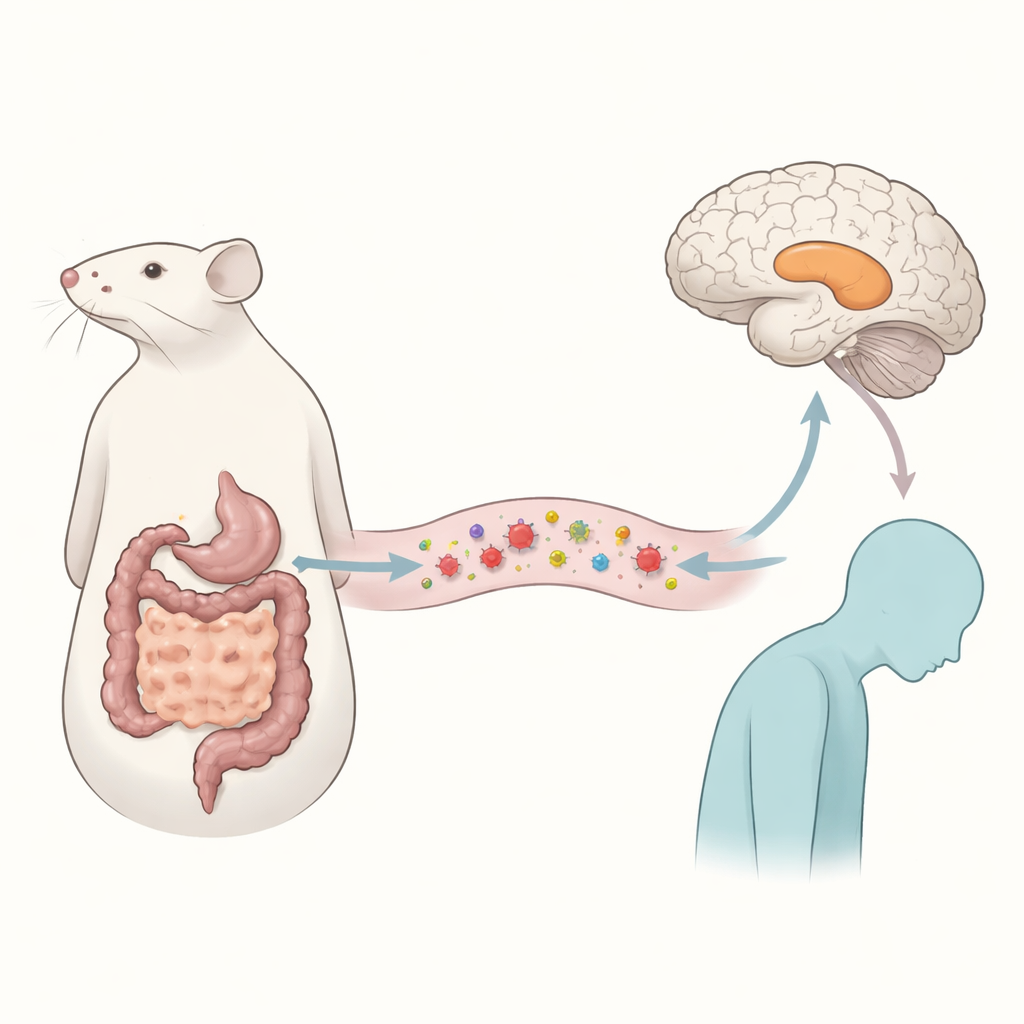
Un pasajero parasitario y cambios en el estado de ánimo
Los investigadores se centraron en Echinococcus multilocularis, el parásito responsable de la equinococosis alveolar, una enfermedad grave que ataca principalmente al hígado. Los pacientes con esta condición con frecuencia refieren malestar mental, pero las razones no estaban claras. Para investigarlo, el equipo infectó ratones con el parásito y esperó dos meses, tiempo suficiente para imitar una infección crónica. Los animales luego realizaron una batería de pruebas conductuales diseñadas para distinguir entre una enfermedad general y cambios de ánimo más específicos. Los ratones infectados se movieron tanto como los sanos y aprendieron y recordaron tareas con normalidad, pero mostraron signos claros de comportamientos tipo depresión: menos interés en recompensas dulces y mayor inmovilidad en pruebas basadas en estrés que se usan ampliamente como indicadores de estados tipo desesperanza en roedores.
Cambios cerebrales sutiles y señales inmunitarias
Al examinar el cerebro, los científicos se fijaron en el hipocampo y la amígdala, regiones profundamente implicadas en la emoción y el estrés. La estructura general de estas áreas permaneció intacta, pero al microscopio algunas neuronas parecían encogidas o de forma anómala, y la membrana externa de sus núcleos mostraba arrugas. Las células inmunitarias residentes del cerebro, las microglías, eran más numerosas en ciertas regiones y presentaban formas más sencillas y menos ramificadas: rasgos característicos de un cambio desde un estado vigilante y en calma hacia un estado activado. Al mismo tiempo, tanto el tejido intestinal como la sangre de los ratones infectados contenían mayores niveles de moléculas proinflamatorias, especialmente las citocinas IL‑6 y MCP‑1, y los genes de algunas de estas señales mostraron mayor actividad en el hipocampo. En conjunto, estos hallazgos apuntan a un estado inflamatorio de bajo grado que se extiende desde el intestino hasta el cerebro y desequilibra a sus células inmunitarias.
Bacterias intestinales y mensajeros químicos perdidos
El equipo preguntó entonces si la comunidad microbiana del intestino podría ser parte de la historia. Mediante secuenciación de ADN, encontraron que la infección remodeló la microbiota intestinal: grupos beneficiosos como Lactobacillus y Bifidobacterium disminuyeron drásticamente, mientras que otros géneros, incluidos Ruminococcus y Prevotella, se expandieron. Los ratones con menos bacterias «amigables» tendían a presentar niveles más altos de citocinas inflamatorias tanto en el intestino como en la sangre. Al mismo tiempo, análisis sanguíneos y un perfil amplio de metabolitos revelaron que componentes clave de la vía triptófano‑serotonina estaban agotados. Los niveles de triptófano (un aminoácido dietario), su intermedio N‑acetilserotonina y el neurotransmisor serotonina (5‑HT) cayeron en los animales infectados. Estos cambios reflejan alteraciones descritas en personas con depresión mayor y se vincularon fuertemente con la abundancia de microbios intestinales específicos.
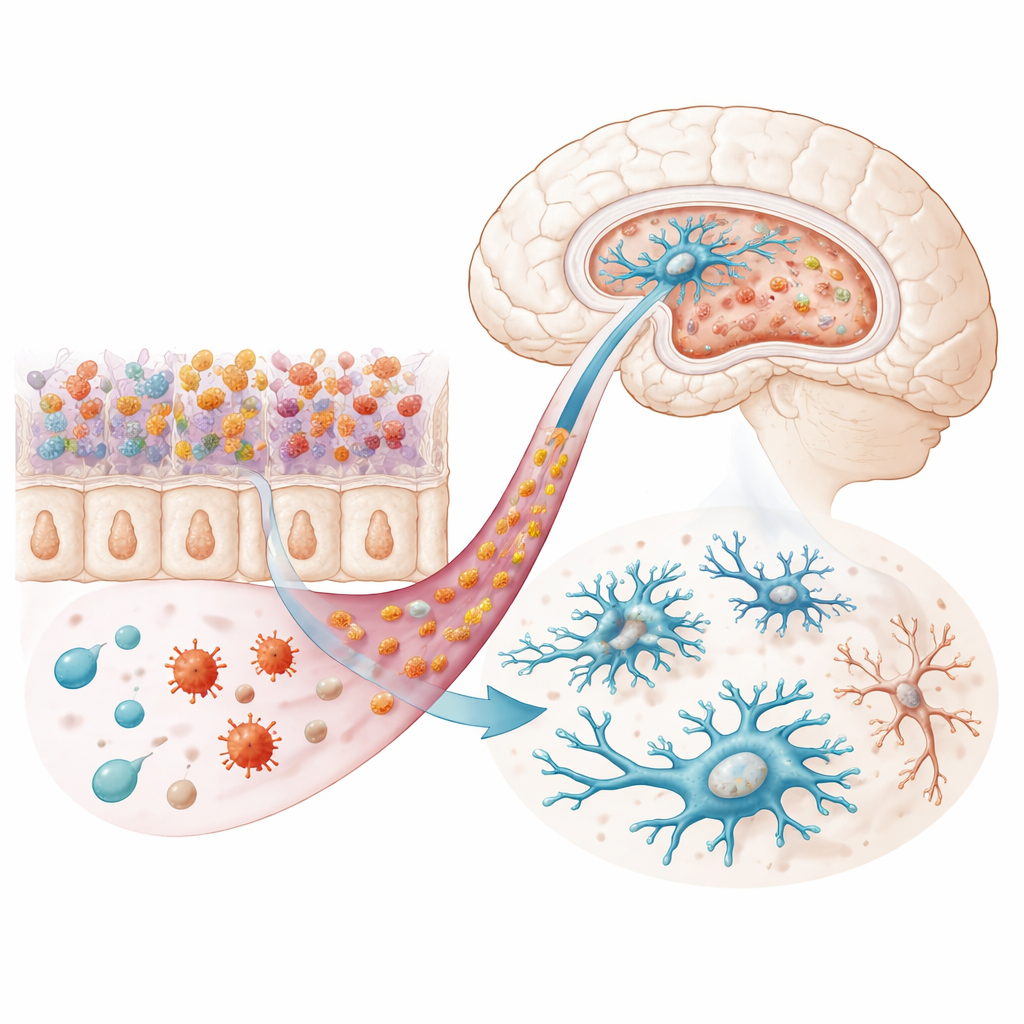
Transferir el microbioma, transferir el estado de ánimo
Para probar si la microbiota alterada era suficiente para cambiar el comportamiento, los investigadores realizaron trasplantes de microbiota fecal. Primero eliminaron las bacterias intestinales de ratones sanos con antibióticos y luego introdujeron heces de donantes infectados o no infectados. Remarkablemente, los receptores de microbiota procedente de donantes infectados desarrollaron comportamientos tipo depresión y evitación ansiosa del centro de un campo abierto, a pesar de que ellos mismos nunca estuvieron expuestos al parásito. Estos ratones también mostraron mayor inflamación, niveles reducidos de triptófano y de moléculas relacionadas con la serotonina en la sangre, y microglías que se asemejaban a las de animales infectados directamente: más abundantes en ciertas regiones, menos ramificadas y llenas de estructuras tipo lisosoma que sugieren mayor estrés celular o actividad de limpieza.
Qué significa esto para la salud humana
Para el público general, el mensaje principal es que una infección crónica en el cuerpo puede perturbar a los habitantes microbianos del intestino y los mensajeros químicos que estos ayudan a producir, y que ello, a su vez, puede influir en las células inmunitarias del cerebro y en los circuitos del ánimo. El estudio no afirma que esta tenia cause depresión clínica en las personas, pero ofrece un mapa detallado de cómo un parásito de larga duración, un intestino inflamado, una microbiota alterada y una química triptófano‑serotonina perturbada podrían actuar conjuntamente para generar comportamientos tipo depresión. Este panorama emergente sugiere que tratar las complicaciones mentales de las infecciones crónicas podría, algún día, incluir no solo eliminar al parásito, sino también calmar la inflamación y restaurar una microbiota intestinal saludable.
Cita: Wen, R., Xin, Y., Bao, S. et al. The gut microbiota mediates depression-like behaviors in mice with chronic Echinococcus multilocularis infection. npj Biofilms Microbiomes 12, 63 (2026). https://doi.org/10.1038/s41522-026-00929-5
Palabras clave: eje intestino‑cerebro, microbioma, infección parasitaria, depresión, metabolismo del triptófano