Clear Sky Science · es
La vía reguladora ppGpp-HpaR1-gum modula la producción de exopolisacáridos en Xanthomonas campestris pv. campestris
Por qué las bacterias «pegajosas» son importantes para los cultivos
Muchas bacterias causantes de enfermedades sobreviven y se diseminan envolviéndose en capas viscosas de azúcares conocidas como biofilms. En cultivos hortícolas como la col y el brócoli, estas capas pueden obstruir los conductos de agua de las plantas, provocando la conocida enfermedad de la «podredumbre negra» y fuertes pérdidas de cosecha. Este estudio examina una de esas bacterias, Xanthomonas campestris, para revelar cómo un sistema interno de alarma química controla la producción de su escudo azucarado. Entender este circuito de control oculto podría ayudar a diseñar mejores estrategias para proteger los cultivos o incluso a aprovechar estos azúcares para obtener materiales útiles.
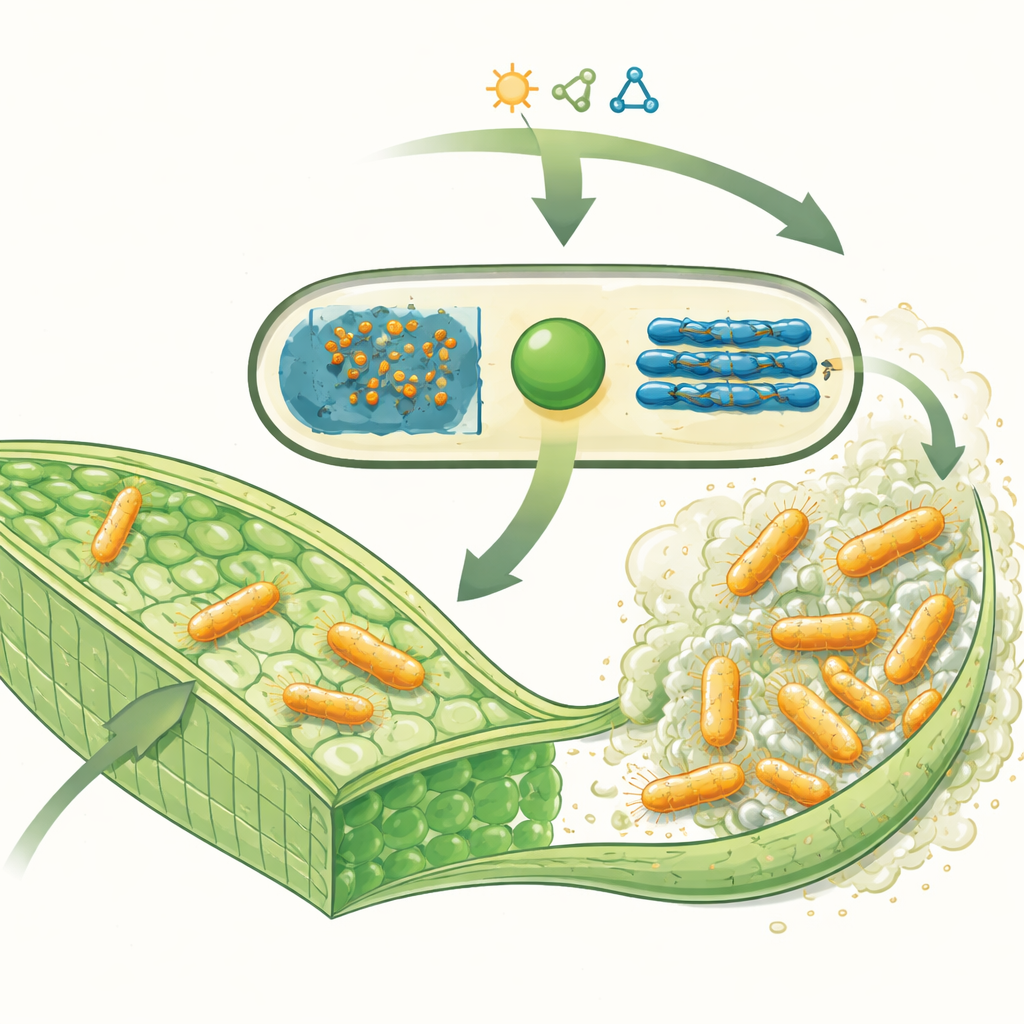
El microbio que infecta plantas y su armadura de azúcar
Xanthomonas campestris penetra en los vasos de las crucíferas —plantas como la col, la coliflor y la mostaza— y produce grandes cantidades de una sustancia viscosa llamada goma xantana. Este material está formado por largas cadenas de unidades de azúcar y constituye una parte importante del biofilm que ayuda a las bacterias a adherirse a los tejidos vegetales, resistir las defensas de la planta y sobrevivir en condiciones adversas. En la planta, estas gruesas capas de azúcar pueden bloquear el flujo de agua, provocando tejido muerto y las características lesiones en forma de V que se observan en la podredumbre negra. Curiosamente, la misma goma xantana se usa ampliamente como espesante en alimentos y otros productos, lo que convierte a este azúcar bacteriano en villano agrícola y a la vez en recurso industrial.
Una alarma interna que modela el comportamiento bacteriano
En el interior de muchas bacterias, una pequeña molécula señal llamada ppGpp actúa como una alarma de emergencia. Cuando escasean nutrientes u surgen otros estreses, los niveles de ppGpp aumentan y desencadenan una amplia «respuesta exigente» que remodela el crecimiento, el metabolismo y las estrategias de supervivencia. Trabajos previos mostraron que ppGpp puede promover la formación de biofilms en varias especies y que eliminarlo en Xanthomonas debilita la capacidad de la bacteria para formar biofilms y causar enfermedad. Lo que quedaba por aclarar era cómo esta diminuta molécula se conecta realmente con la maquinaria que construye el espeso recubrimiento de exopolisacáridos (EPS) en este patógeno vegetal en particular.
Rastreando el camino desde la señal hasta el azúcar
Los investigadores compararon bacterias normales con mutantes incapaces de fabricar ppGpp. En placas ricas en azúcar, los mutantes que carecían de ppGpp formaron colonias más pequeñas y menos mucosas, y las mediciones directas mostraron que producían mucho menos EPS. Sin embargo, el análisis químico mediante espectroscopía infrarroja y la observación por microscopía electrónica revelaron que la composición básica y la conformación de orden superior del EPS seguían siendo las mismas: los mutantes simplemente producían menos cantidad. La atención se centró entonces en el clúster génico «gum», un conjunto de genes que codifica las enzimas que ensamblan la goma xantana. Mediante mediciones de expresión génica y secuenciación de ARN, el equipo descubrió que casi todos los genes gum estaban reprimidos en las células deficientes en ppGpp, situando a ppGpp aguas arriba de este clúster en la jerarquía de control.
Un intermediario clave: el interruptor HpaR1
Entre la alarma ppGpp y los genes gum se encuentra una proteína reguladora llamada HpaR1, un factor de transcripción que se une al ADN y potencia la actividad de los genes gum. El estudio mostró que ppGpp actúa en dos frentes. Primero, las células sin ppGpp presentaron niveles reducidos de actividad del gen hpaR1, lo que significa que había menos proteína HpaR1 disponible. Segundo, en ensayos purificados de laboratorio, añadir ppGpp reforzó directamente la unión de HpaR1 a las regiones de ADN que controlan los genes gum e incluso a su propia región de control. A niveles moderados de ppGpp, esta unión se vio claramente potenciada, aunque niveles extremadamente altos la debilitaban parcialmente, lo que sugiere un equilibrio finamente ajustado. Cuando los científicos aumentaron artificialmente los niveles de HpaR1, la producción de EPS volvió a subir —incluso en bacterias sin ppGpp—, confirmando que HpaR1 es el intermediario crucial entre la señal de alarma y la maquinaria productora de azúcar.
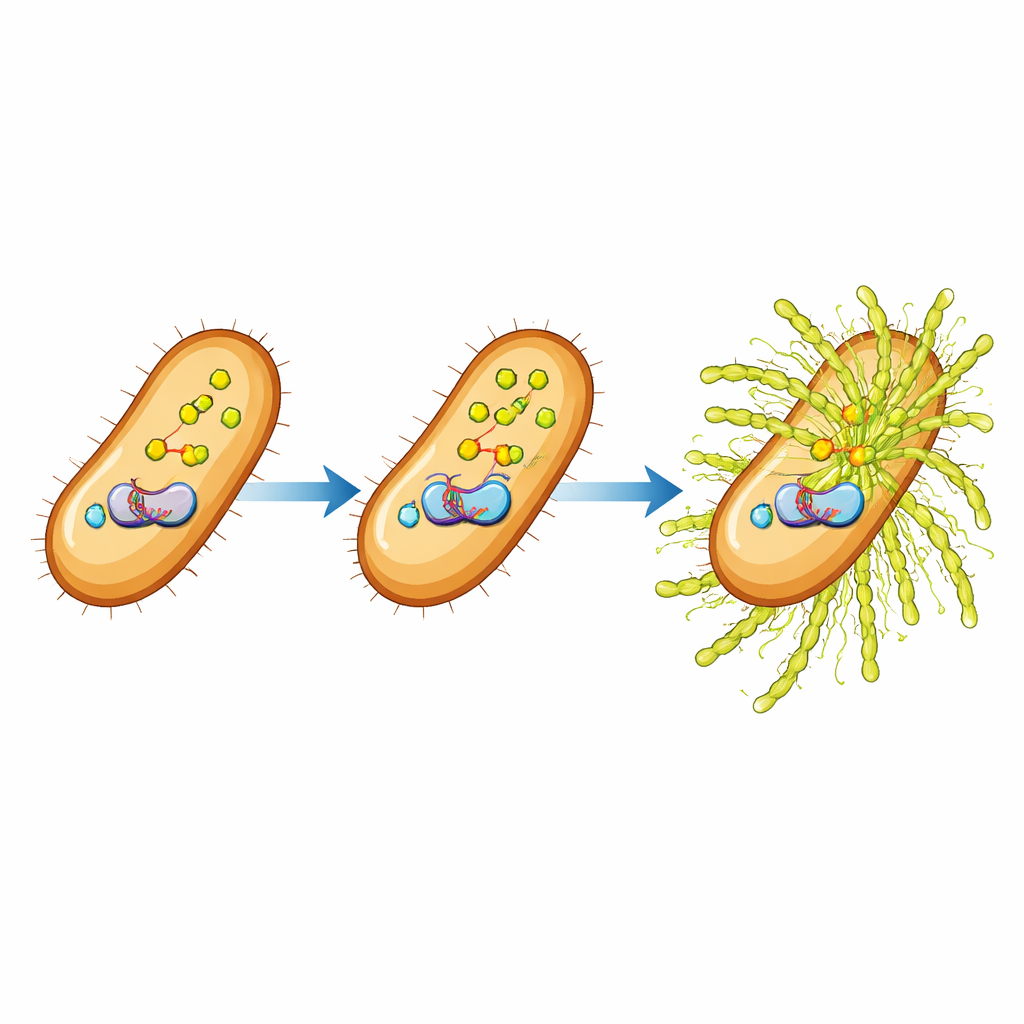
Qué significa este circuito de control para los cultivos y más allá
En términos sencillos, este trabajo descubre un relevo de tres pasos dentro de un patógeno vegetal: una molécula de alarma interna (ppGpp) potencia y fortalece un interruptor de unión al ADN (HpaR1), que a su vez activa una fábrica de producción de azúcares (los genes gum), lo que conduce a un recubrimiento protector más espeso de mucílago alrededor de las bacterias. Al mapear en detalle esta vía ppGpp–HpaR1–gum, el estudio explica cómo las señales de estrés ambiental pueden convertirse en cambios en la producción de la matriz del biofilm. Para agricultores y fitopatólogos, estos hallazgos sugieren nuevos objetivos para interrumpir la armadura bacteriana y reducir el daño por podredumbre negra. Para los microbiólogos en general, los resultados añaden una pieza importante al rompecabezas de cómo las señales universales de estrés controlan la formación de comunidades microbianas complejas.
Cita: Bai, K., Xu, X., Yu, C. et al. The ppGpp-HpaR1-gum regulatory pathway modulates exopolysaccharides production in Xanthomonas campestris pv. campestris. npj Biofilms Microbiomes 12, 60 (2026). https://doi.org/10.1038/s41522-026-00926-8
Palabras clave: biófilms bacterianos, patógenos de plantas, goma xantana, señalización por estrés, exopolisacáridos