Clear Sky Science · es
Caracterización metabólica en tiempo real y alta resolución de bacterias vivas mediante imagen óptica metabólica sin etiquetas
Observar a los gérmenes reaccionar en tiempo real
Las bacterias están por doquier sobre y dentro de nosotros, moldeando silenciosamente nuestra salud. Ayudan a digerir los alimentos, protegen la piel y, en ocasiones, provocan infecciones persistentes que resisten los antibióticos. Este estudio presenta una forma de observar bacterias vivas reaccionando al estrés y a los fármacos en tiempo real, a nivel de células individuales, sin añadir colorantes ni etiquetas. Esa capacidad podría, con el tiempo, ayudar a los médicos a elegir el tratamiento adecuado más rápido y a los científicos a entender por qué algunas infecciones son tan difíciles de curar.
La luz como ventana a la vida bacteriana
En lugar de añadir tinciones o etiquetas genéticas, los investigadores se basan en que las bacterias emiten de forma natural un tenue brillo cuando ciertas moléculas internas son excitadas por luz láser. Dos de estas moléculas, conocidas como NAD(P)H y FAD, son actores centrales en la forma en que las células convierten los alimentos en energía. Con microscopía láser rápida y de alta resolución, el equipo puede medir tanto la intensidad como el pequeño retardo temporal de ese brillo, revelando cuán activo está el metabolismo de una célula. Dado que el método no requiere etiquetas y no es destructivo, las mismas bacterias vivas pueden seguirse durante segundos y minutos mientras cambia su entorno. 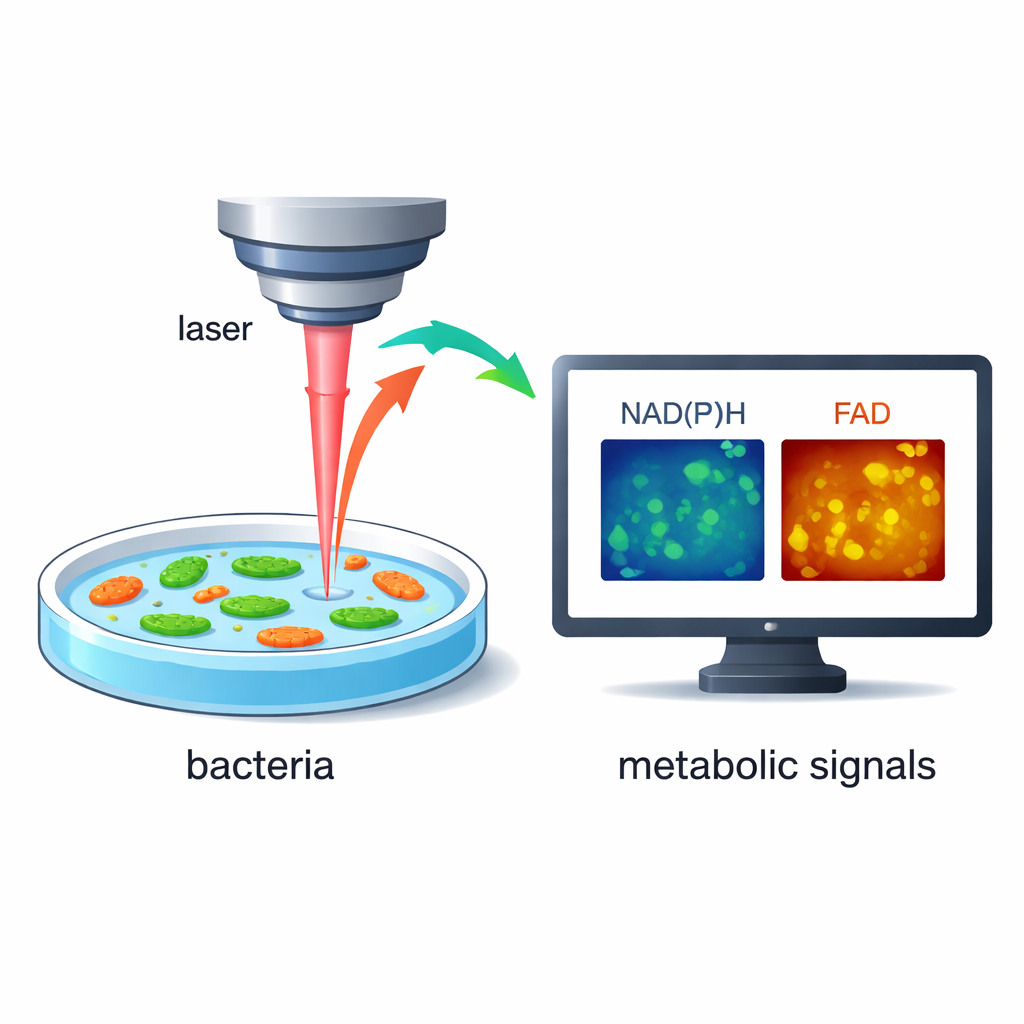
Ver las diferencias entre bacterias individuales
La mayoría de las pruebas de laboratorio estándar agrupan millones de bacterias y solo informan una respuesta promedio. Aquí, los autores muestran que su método de imagen puede identificar células individuales de Staphylococcus aureus en cultivo líquido y analizar cada una por separado, incluso a altas densidades celulares. Al comparar dos colonias de S. aureus cultivadas en las mismas condiciones, una señal clave (la procedente de FAD) difería entre colonias, y también había una dispersión de valores dentro de cada colonia. Esto significa que incluso bacterias genéticamente similares en el mismo matraz pueden encontrarse en estados metabólicos muy distintos, una diversidad oculta que las pruebas convencionales a granel podrían pasar por alto pero que puede influir en la respuesta de las infecciones al tratamiento.
Observar a los antibióticos actuar en segundos
El equipo siguió luego células individuales de S. aureus mientras se exponían a varios tratamientos antibacterianos, incluidos antibióticos comunes y lejía doméstica. Con su configuración de imagen rápida capturaron cambios desde el momento en que la solución farmacológica tocó las células y durante los 30 minutos siguientes. Los tratamientos intensos provocaron caídas en las señales de NAD(P)H y aumentos en las de FAD, a menudo en cuestión de segundos, lo que refleja una detención de la producción de energía y un desplazamiento hacia un estado más oxidado dentro de la célula. El tiempo exacto y el patrón de estos cambios dependieron del tipo y la dosis del fármaco: por ejemplo, los antibióticos que bloquean la síntesis de proteínas o atacan la pared celular produjeron una caída breve y una recuperación parcial, mientras que la lejía provocó un cambio brusco y sostenido. Estas distintas “firmas luminosas” sugieren que la técnica puede detectar no solo si las células están estresadas o muriendo, sino también cómo están siendo dañadas. 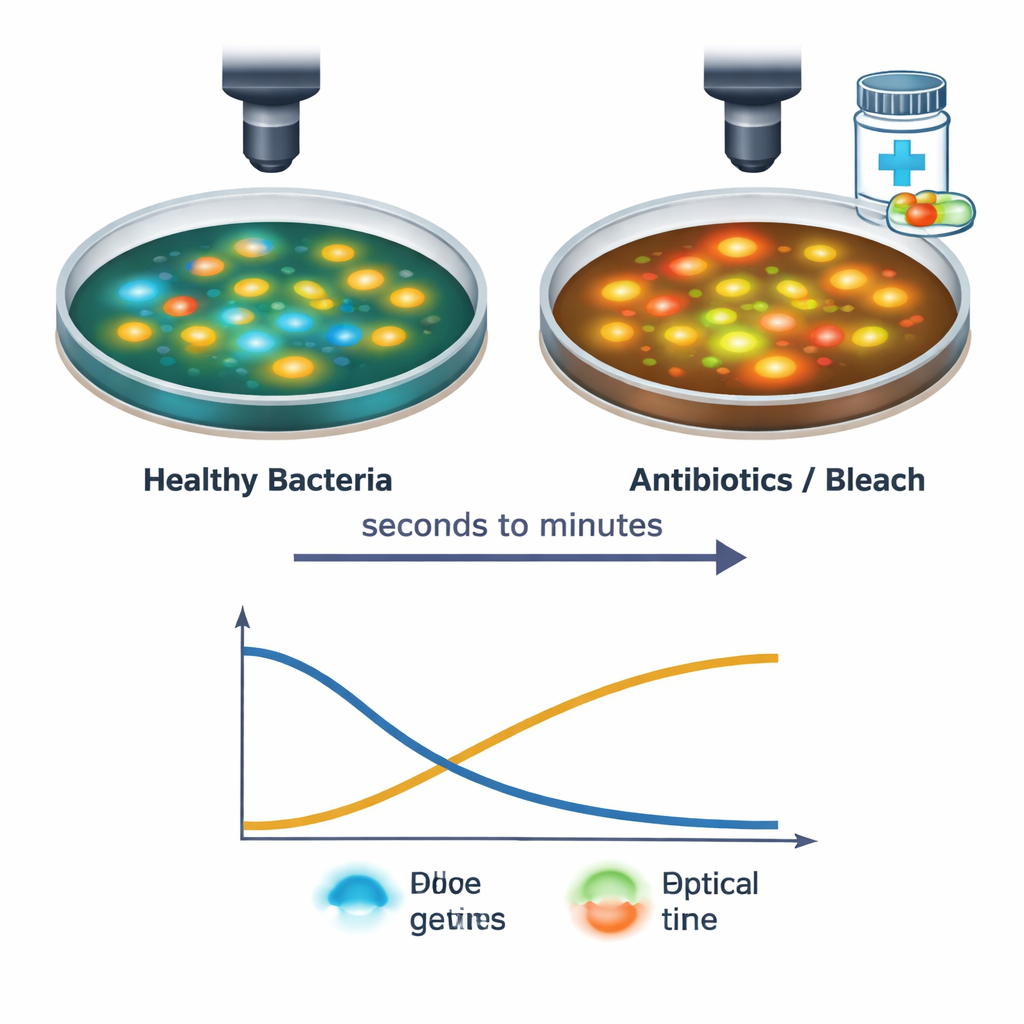
Asomarse al mundo oculto de las biopelículas
Las bacterias rara vez viven aisladas en la naturaleza; en su lugar construyen comunidades viscosas y protectoras llamadas biopelículas sobre superficies que van desde implantes médicos hasta dientes. En estas capas densas, algunas células pueden estar muy activas mientras otras permanecen en letargo, una mezcla que ayuda a la comunidad a sobrevivir a los antibióticos. Usando imágenes grandes cosidas entre sí, los investigadores cartografiaron el paisaje metabólico dentro de biopelículas de S. aureus y lo compararon con células nadando libremente. Encontraron bolsillos brillantes y metabólicamente activos rodeados por regiones menos activas y mostraron que, en varias especies, las bacterias en biopelículas tendían a presentar un perfil metabólico más oxidado que sus contrapartes de vida libre. Señales ópticas adicionales sugirieron mayor presencia de lípidos y proteínas, coherente con el material adhesivo que mantiene unidas a las biopelículas.
Por qué esto importa para la medicina futura
En conjunto, estos resultados muestran que la imagen metabólica óptica sin etiquetas puede proporcionar instantáneas rápidas, detalladas y no invasivas de cómo las bacterias viven, se adaptan y mueren. Para un lector general, el mensaje clave es que los científicos pueden ahora “escuchar” el uso de energía de las bacterias en tiempo real, sin perturbar las células, usando solo luz afinada con precisión. A largo plazo, este tipo de tecnología podría ayudar a identificar bacterias difíciles de cultivar, detectar focos de células tolerantes a fármacos dentro de biopelículas o probar rápidamente cómo responde la infección de un paciente a distintos antibióticos. Eso podría favorecer tratamientos más rápidos y personalizados y profundizar nuestra comprensión de los mundos microbianos invisibles que afectan nuestra salud cada día.
Cita: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
Palabras clave: metabolismo bacteriano, imagen óptica, biopelículas, respuesta a antibióticos, microbioma