Clear Sky Science · es
Modulación inmunitaria impulsada por la microbiota oral a lo largo del eje oral–intestinal: de las señales locales a la inflamación sistémica
Por qué tu boca importa para todo tu cuerpo
Las bacterias que viven en la boca hacen mucho más que provocar caries o mal aliento. Este artículo de revisión explica cómo los microbios orales pueden desplazarse hacia el intestino, alterar sus delicadas defensas y contribuir a desencadenar inflamación que alcanza órganos como el hígado y el cerebro. Comprender este oculto “eje oral–intestinal” ofrece nuevas pistas sobre problemas comunes que van desde la enfermedad hepática grasa hasta el Alzheimer, y apunta a medidas sorprendentemente simples —como una mejor higiene dental y cambios en la dieta— que pueden proteger nuestra salud global.
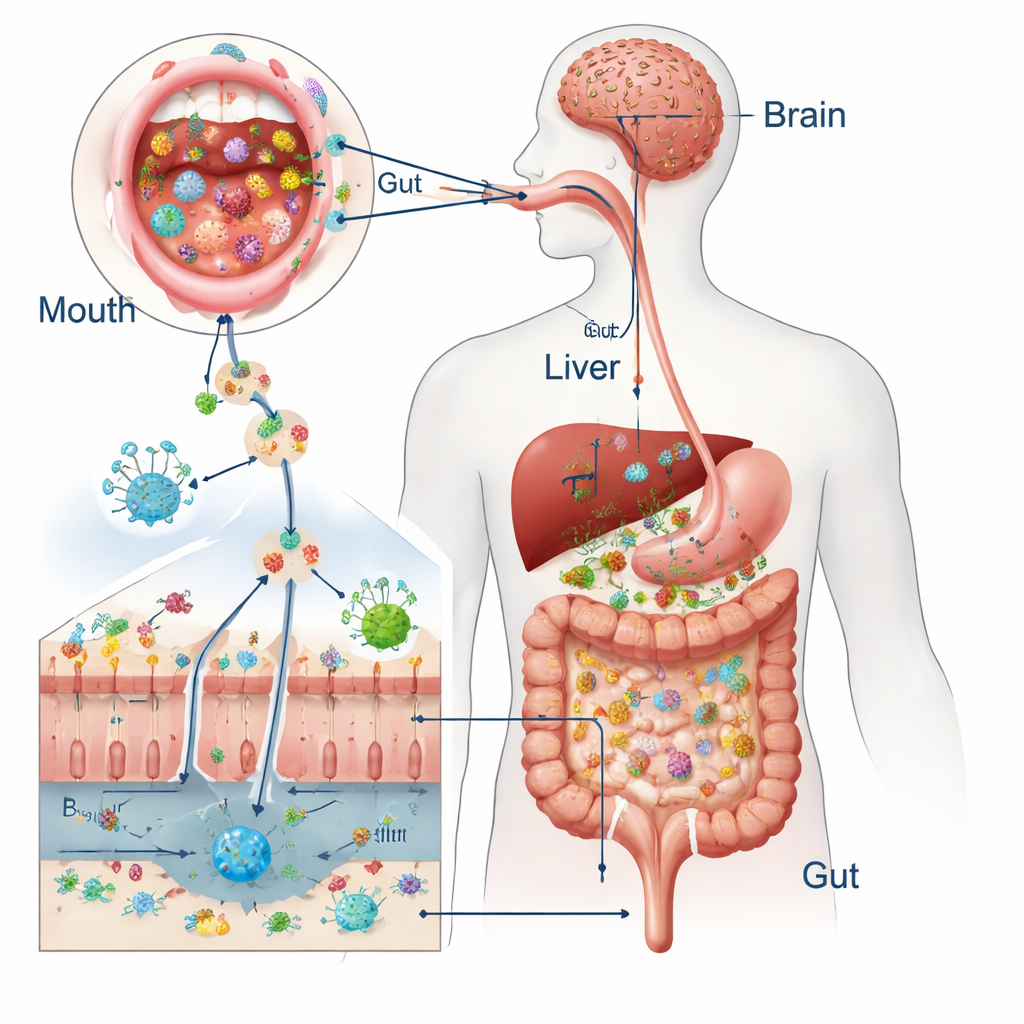
De tragar a efectos en todo el organismo
Cada día tragamos cerca de litro y medio de saliva repleta de miles de millones de microbios orales. En personas sanas, defensas sólidas —los antimicrobianos naturales de la saliva, el ácido gástrico, la bilis, el moco pegajoso y las células intestinales con uniones herméticas— impiden que la mayoría de estos visitantes se establezcan. Estudios que comparan los gérmenes de la boca y de las heces muestran que solo una fracción diminuta de los microbios intestinales proviene directamente de la boca cuando todo funciona bien. Pero los dos ecosistemas se solapan lo suficiente como para que especies orales como Streptococcus y Veillonella a veces se detecten en el intestino, lo que plantea la pregunta de cuándo dejan de ser meros transeúntes inofensivos.
Cuando las barreras se rompen
El panorama cambia bajo estrés. El envejecimiento, la sequedad bucal, una higiene oral deficiente y la enfermedad periodontal crónica pueden sobrecargar la boca con bacterias nocivas. Medicamentos como los antibióticos y los bloqueadores del ácido estomacal debilitan las defensas intestinales al adelgazar el moco, aflojar las uniones entre células y permitir que más microbios sobrevivan al paso por el estómago. Las infecciones orales y los procedimientos dentales pueden incluso empujar bacterias hacia el torrente sanguíneo. La revisión también pone de relieve las vesículas extracelulares bacterianas —“paquetes” nanoescala desprendidos por los microbios— que pueden deslizarse por los tejidos y transportar señales inflamatorias lejos de su origen. Algunas bacterias orales, como Porphyromonas gingivalis y Fusobacterium nucleatum, incluso se ocultan dentro de células inmunitarias y viajan por el cuerpo a modo de “caballo de Troya” microbiano.
Cómo las bacterias bucales aprenden a vivir en el intestino
No todos los microbios orales que llegan al intestino pueden quedarse. Los que lo consiguen suelen tener trucos especiales de supervivencia. Ciertas cepas remodelan sus membranas celulares para resistir ácidos fuertes o la bilis; otras se alimentan de azúcares del moco que recubre la pared intestinal o se asocian con bacterias residentes para formar biopelículas adherentes. Al mismo tiempo, aprenden a pasar desapercibidos para el sistema inmunitario. Algunas bloquean la capacidad letal de las células asesinas naturales y de los linfocitos T; otras interfieren con sensores de alerta temprana que normalmente detectan componentes microbianos y disparan respuestas protectoras. Al impulsar el equilibrio hacia tipos de células más inflamatorias y menos “frenos” reguladores, crean un nicho donde la colonización a largo plazo y de bajo grado se vuelve posible.
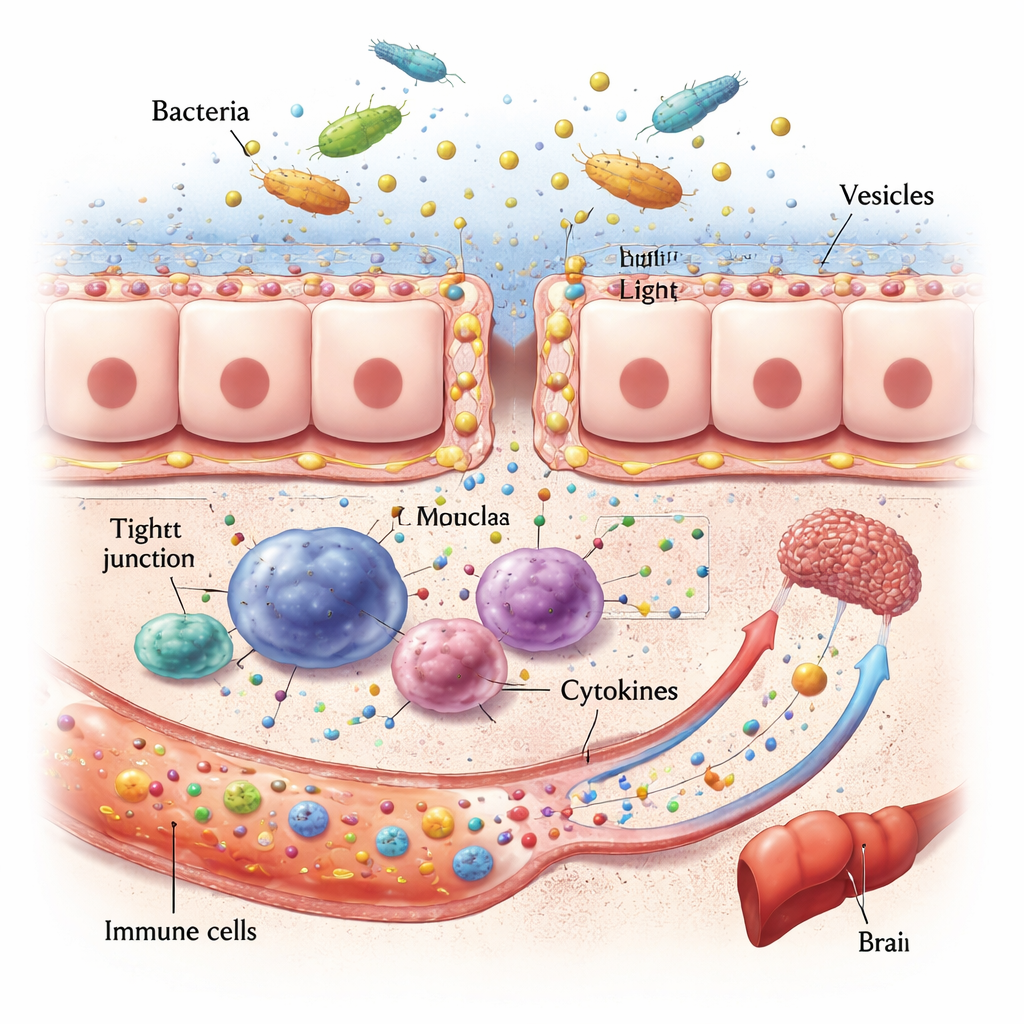
Del intestino permeable a órganos enfermos
Una vez establecidos, los microbios orales invasivos y sus vesículas pueden dañar la primera línea del intestino. Degradan las proteínas que sellan las células vecinas, adelgazan la capa de moco e incluso pueden matar directamente células intestinales. Esto hace que la pared intestinal sea más permeable, permitiendo que fragmentos bacterianos y toxinas se filtren al torrente sanguíneo. Allí activan células inmunitarias y desencadenan ráfagas de moléculas señalizadoras llamadas citocinas. Como la sangre intestinal fluye directamente al hígado, ese órgano queda especialmente expuesto: datos en animales y humanos vinculan patógenos orales con enfermedad hepática grasa, fibrosis y empeoramiento de la inflamación. Vías similares conectan la disbiosis oral y la disrupción intestinal con el cerebro, donde la inflamación crónica y los metabolitos microbianos alterados parecen agravar la acumulación de proteínas relacionadas con el Alzheimer y alterar el estado de ánimo y la cognición.
Nuevas formas de intervenir
Reconocer el eje oral–intestinal abre estrategias multinivel para la prevención y la terapia. En la boca, el tratamiento periodontal rutinario, las terapias con luz y los péptidos antimicrobianos naturales pueden reducir las bacterias nocivas y disminuir el número que llega al intestino. En el intestino, probióticos, dietas ricas en fibra y suplementos que restauran los ácidos grasos de cadena corta ayudan a reconstruir la barrera intestinal y a calmar la inmunidad sobreactiva. Mirando al futuro, dispositivos sofisticados de “órgano en un chip” que conecten mini tejidos de boca, intestino, hígado y cerebro, junto con mapas de big data sobre qué microbios provocan qué reacciones inmunitarias, podrían permitir enfoques personalizados para prevenir enfermedades inflamatorias crónicas.
Qué significa esto para ti
Para un lector no especializado, el mensaje central es que la boca no es un compartimento aislado: sus microbios pueden moldear la salud intestinal y, a través del intestino, influir en todo el organismo. Cuando las bacterias orales evaden o erosionan las barreras naturales, pueden contribuir a una inflamación duradera en órganos tan distantes como el hígado y el cerebro. El artículo concluye que proteger la salud oral, preservar la barrera intestinal y dirigir con suavidad nuestras comunidades microbianas mediante tratamientos dirigidos podrían convertirse en herramientas importantes para combatir las enfermedades crónicas modernas.
Cita: Li, C., Fan, Y. & Chen, X. Oral microbiota–driven immune modulation along the oral–gut axis: from local signals to systemic inflammation. npj Biofilms Microbiomes 12, 46 (2026). https://doi.org/10.1038/s41522-026-00912-0
Palabras clave: microbioma oral, barrera intestinal, inflamación sistémica, enfermedad hepática, salud cerebral