Clear Sky Science · es
La terapia antibiótica potenciada con enzimas reduce los biofilms a niveles indetectables en un modelo de infección asociada a implantes
Por qué importan las infecciones persistentes en implantes
Las prótesis de cadera y rodilla transforman vidas, pero cuando las bacterias colonizan estos implantes metálicos pueden formar comunidades viscosas llamadas biofilms. Estos biofilms actúan como ciudades fortificadas que protegen a los gérmenes tanto del sistema inmunitario como de los antibióticos, provocando infecciones dolorosas y prolongadas que son muy difíciles de curar. Este estudio explora un nuevo tratamiento de doble vía que primero ayuda a desmantelar las defensas del biofilm y luego baña la zona con dosis elevadas de antibióticos, un enfoque que algún día podría permitir salvar más implantes en lugar de reemplazarlos.
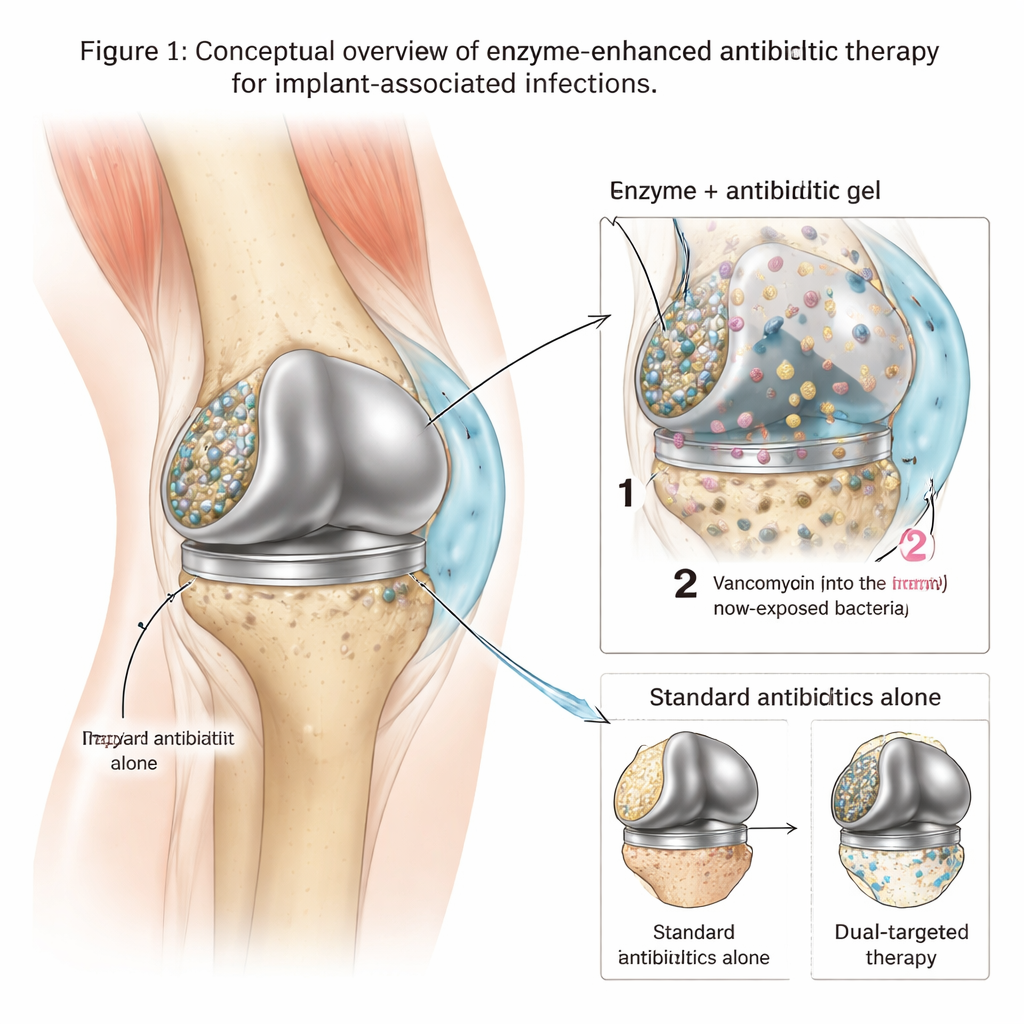
Los bastiones ocultos en los implantes metálicos
Cuando bacterias como Staphylococcus aureus resistente a meticilina (MRSA) se adhieren a una articulación artificial, rápidamente construyen una matriz pegajosa de ADN, azúcares y otras moléculas sobre la superficie metálica. Dentro de este biofilm protegido, las bacterias crecen despacio, cambian su comportamiento y pueden tolerar niveles de antibiótico cientos o incluso miles de veces superiores a los que matan a los microbios en suspensión. Como resultado, los tratamientos estándar—even fármacos potentes como la vancomicina—suelen fracasar en eliminar por completo la infección, obligando a los pacientes a someterse a cirugías repetidas o al reemplazo total del implante. Los médicos necesitan herramientas que no solo maten bacterias, sino que también rompan su fortaleza protectora para que los fármacos puedan alcanzarlas.
Un gel inteligente que administra enzimas y antibióticos
Los investigadores diseñaron un tratamiento local basado en un hidrogel termosensible hecho de un compuesto llamado poloxámero 407. Este gel es líquido cuando está frío, lo que facilita su inyección alrededor de un implante, pero se convierte rápidamente en un sólido blando a la temperatura corporal, ayudando a que permanezca en su sitio. En este gel, el equipo cargó dos ingredientes clave: un antibiótico potente (vancomicina) y un cóctel de tres enzimas que degradan los componentes principales de la matriz del biofilm. En pruebas de laboratorio, ajustaron el gel para que las enzimas se liberen primero—aflojando y adelgazando el biofilm—mientras que la vancomicina se libera más lentamente durante varios días, manteniendo niveles locales de fármaco muy altos justo donde viven las bacterias.
De las placas de laboratorio a los cobayos
Para comprobar si la estrategia funcionaba realmente, el equipo la probó primero en biofilms cultivados sobre piezas de titanio en el laboratorio y luego en un modelo de cobayas que imita implantes infectados. In vitro, dos aplicaciones del gel enzimático-antibiótico, separadas por 48 horas, redujeron el número de bacterias vivas en superficies metálicas más de 100.000 veces y casi eliminaron la masa del biofilm. En animales, los investigadores colocaron quirúrgicamente jaulas perforadas que contenían cuentas de titanio bajo la piel, las infectaron con MRSA y luego las trataron con distintas combinaciones de antibióticos sistémicos y gels locales. El régimen más eficaz combinó: (1) el gel local que contenía tanto enzimas como vancomicina, administrado dos veces, y (2) un tratamiento general con vancomicina más un segundo antibiótico, rifampicina, que penetra especialmente bien en los biofilms.
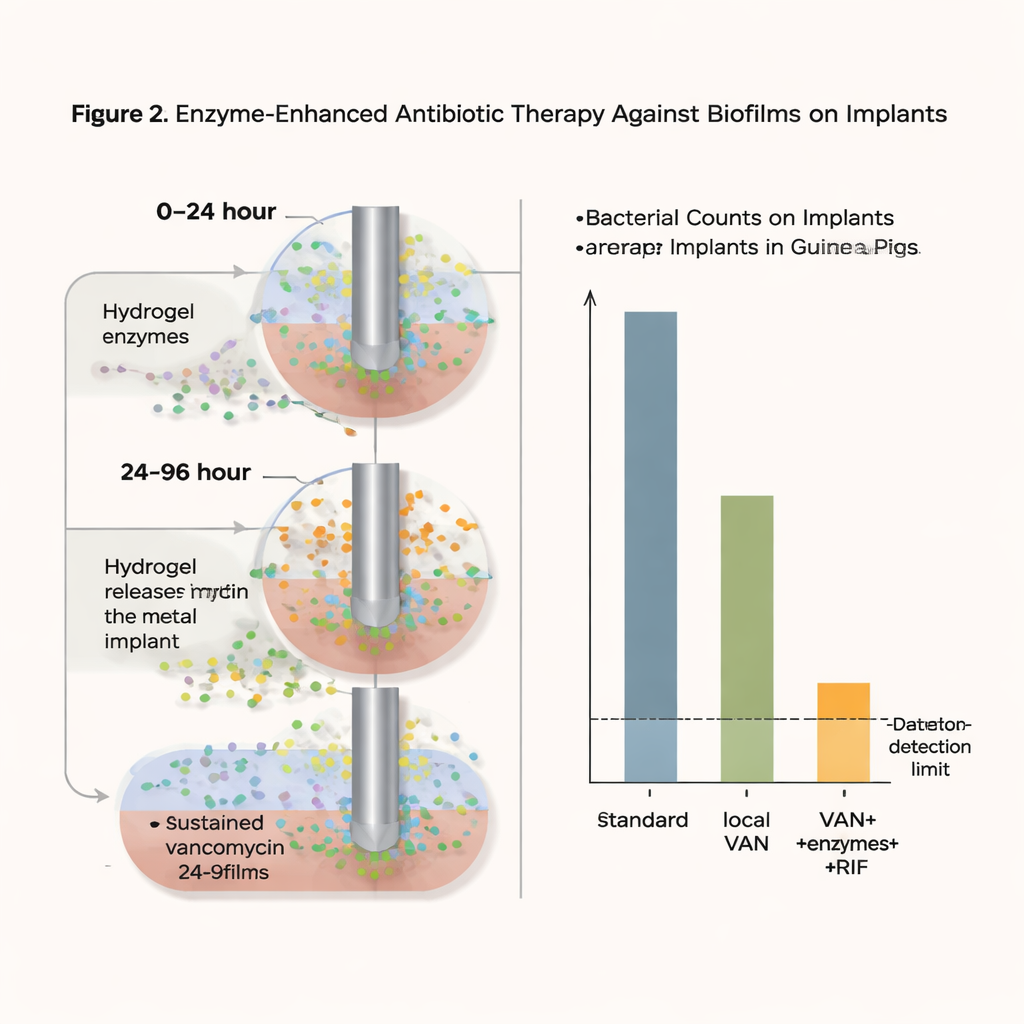
Lo que logró el nuevo enfoque
Con esta estrategia intensiva pero localizada, los recuentos bacterianos en el material del implante cayeron hasta el límite de detección—efectivamente “sin bacterias recuperables” en este modelo—en el 75 por ciento de las jaulas tratadas un día después de finalizar la terapia, y en el 37,5 por ciento incluso cinco días después. Importante: no se observó aumento de la resistencia a la vancomicina, y los altos niveles locales de vancomicina parecieron prevenir la aparición de cepas resistentes a la rifampicina. Pruebas de seguridad con células en cultivo y un modelo de piel humana reconstruida no mostraron signos de toxicidad ni de irritación por las formulaciones del gel. Aunque en algunos casos se produjo un leve re-crecimiento bacteriano y el periodo de tratamiento fue más corto que el que suelen recibir los pacientes, los resultados demuestran que combinar enzimas que rompen el biofilm con una liberación local sostenida de antibiótico puede reducir drásticamente infecciones que de otro modo serían persistentes.
Lo que esto podría significar para los pacientes
Para las personas con infecciones relacionadas con implantes, este trabajo señala hacia un futuro en el que los cirujanos podrían inyectar un gel inteligente alrededor de una articulación infectada, en lugar de retirar o reemplazar inmediatamente el hardware. Al debilitar primero el escudo del biofilm y luego inundar la zona con dosis altas y sostenidas de antibióticos—respaldadas por un tratamiento sistémico—esta estrategia de doble objetivo pretende reducir los números bacterianos hasta niveles indetectables y disminuir el riesgo de resistencia. Aunque aún hacen falta más estudios, tratamientos más prolongados y ensayos en humanos, el enfoque ofrece un plan prometedor para convertir algunas de las infecciones ortopédicas más persistentes en problemas más manejables y, potencialmente, curables.
Cita: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Palabras clave: infección por biofilm, implantes ortopédicos, vancomicina, terapia enzimática, rifampicina