Clear Sky Science · es
Una exploración teórica de los protocolos para tratar infecciones de prótesis articulares con combinaciones de antibióticos y bacteriófagos
Por qué importan las infecciones de implantes articulares
Los reemplazos de cadera y rodilla han transformado la vida de millones de personas, permitiéndoles caminar sin dolor. Pero cuando las bacterias colonizan estas articulaciones artificiales, pueden formar comunidades viscosas llamadas biopelículas que se adhieren firmemente a superficies de metal y plástico. Una vez establecida una biopelícula, las dosis normales de antibióticos y las defensas inmunitarias del cuerpo a menudo tienen dificultades para erradicarla, a veces obligando a los pacientes a someterse a más cirugías. Este estudio se pregunta si añadir virus que atacan específicamente a las bacterias —llamados bacteriófagos, o fagos— a los antibióticos estándar puede ofrecer una mejor forma de tratar estas infecciones persistentes.
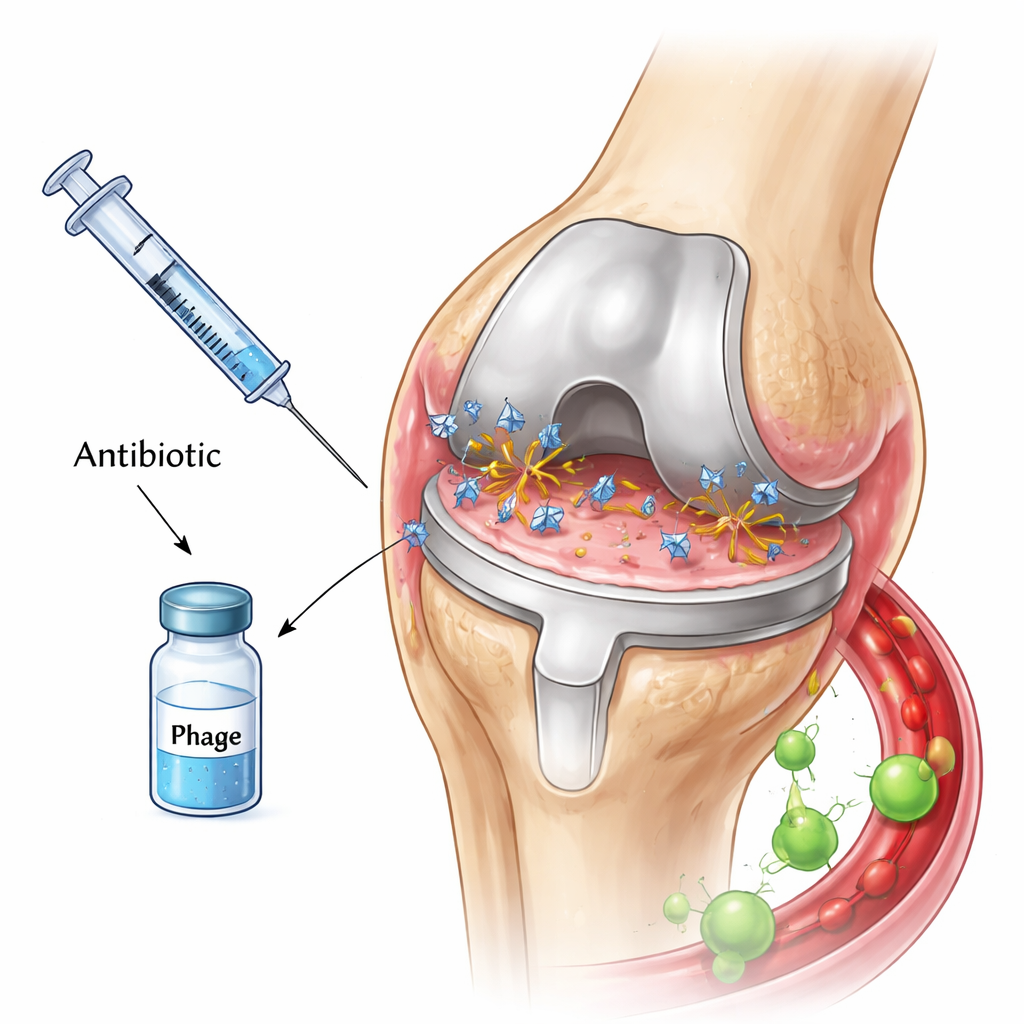
Virus diminutos que cazan bacterias
Los fagos son depredadores naturales de las bacterias. Se adhieren a una célula bacteriana, inyectan su material genético, convierten la célula en una fábrica de virus y finalmente la hacen estallar, liberando una multitud de nuevos fagos. Algunos fagos también llevan enzimas que pueden degradar el material adhesivo que rodea las biopelículas, abriendo potencialmente las capas protectoras que protegen a las bacterias de los fármacos. Debido a estas características, muchos investigadores han confiado en que la combinación de fagos con antibióticos podría proporcionar un golpe doble potente contra las infecciones de prótesis articulares, especialmente cuando las bacterias desarrollan resistencia a los medicamentos.
Construir infecciones dentro de un ordenador
En lugar de ir directamente a experimentos con animales o ensayos clínicos, los autores construyeron primero un modelo matemático y computacional detallado de una infección de prótesis articular. Su sistema virtual tenía dos zonas principales: bacterias flotantes libres en los fluidos corporales y bacterias integradas en una biopelícula sobre la superficie del implante. El modelo también seguía a las células inmunitarias, los nutrientes para el crecimiento bacteriano, los antibióticos y los fagos, todos entrando y saliendo de la articulación. Al cambiar condiciones como la dosis del fármaco, el momento y la presencia de bacterias resistentes a antibióticos, pudieron explorar muchas estrategias de tratamiento que serían difíciles, lentas o costosas de probar en pacientes reales.
Cuando los medicamentos actúan solos y en combinación
Las simulaciones mostraron que ni el sistema inmunitario ni los antibióticos por sí solos eliminaban fácilmente las infecciones por biopelícula. Los antibióticos redujeron fuertemente las bacterias flotantes, pero apenas afectaron a la población de la biopelícula. Los fagos pudieron controlar inicialmente la infección con más eficacia, pero introdujeron ciclos de auge y caída: a medida que los fagos mataban bacterias, su presa se volvía demasiado escasa, provocando una caída en el número de fagos y permitiendo que las bacterias se recuperaran. Cuando se administraron antibióticos y fagos al mismo tiempo, el antibiótico tendía a dominar el resultado, y añadir fagos a menudo no hacía mucho más de lo que el antibiótico podía conseguir por sí solo.
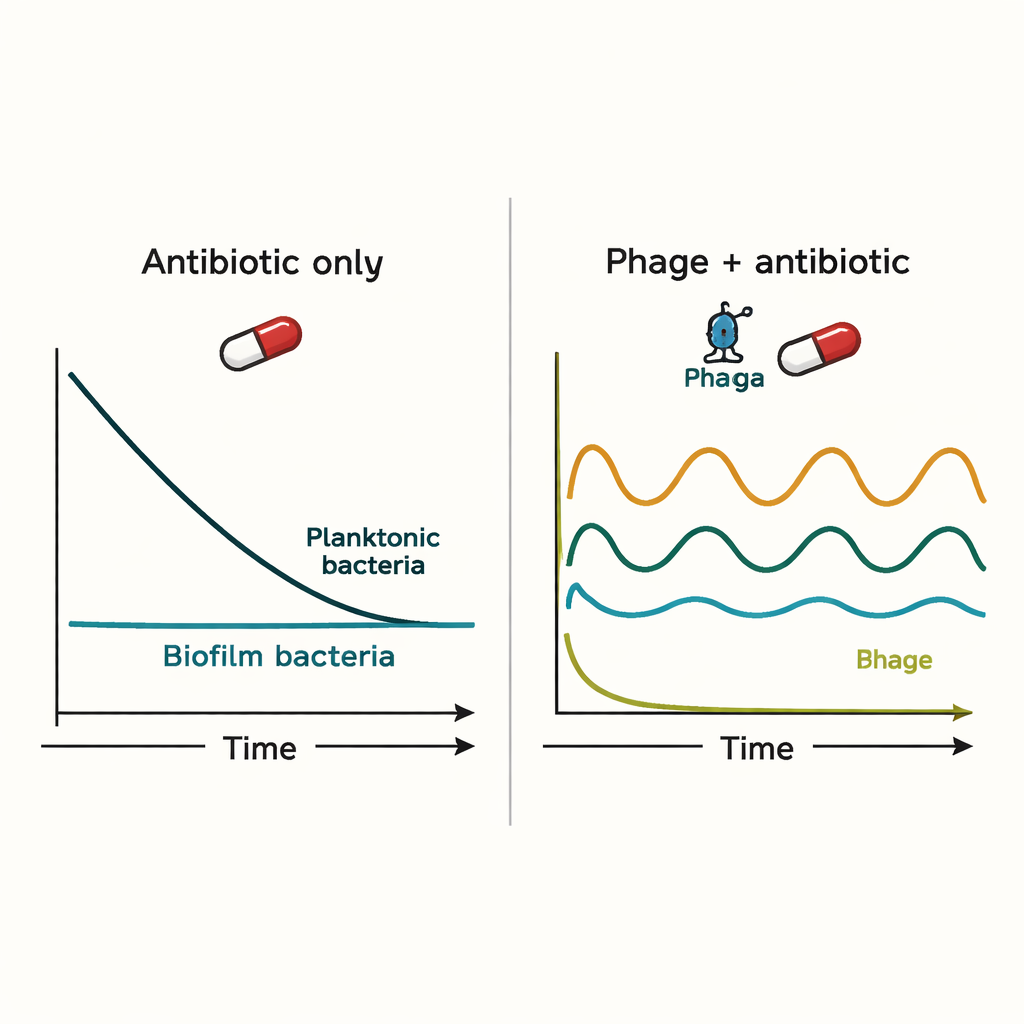
El papel especial del tiempo y la resistencia
El modelo se volvió más esperanzador cuando se incluyeron bacterias resistentes a antibióticos. Los fagos pudieron atacar estas células resistentes, a veces eliminándolas por completo. Si el tratamiento con fagos se iniciaba primero y los antibióticos se añadían varias horas después, la estrategia combinada reducía las bacterias flotantes por muchos órdenes de magnitud y eliminaba las subpoblaciones resistentes en las simulaciones. Aun así, las bacterias asociadas a la biopelícula no se erradicaron por completo; en cambio, su número se mantenía en niveles más bajos que podrían ser más manejables para el sistema inmunitario. Esto sugiere que los fagos pueden ser más útiles no como balas de plata, sino como auxiliares que previenen la resistencia y mantienen las infecciones bajo control.
Qué significa esto para pacientes y médicos
Para las personas con una prótesis articular infectada, este trabajo ofrece tanto cautela como esperanza. El modelo sugiere que simplemente añadir fagos a los antibióticos estándar probablemente no cure por sí solo las infecciones profundas de biopelícula. Sin embargo, los fagos todavía podrían ser herramientas valiosas: pueden ayudar a eliminar bacterias resistentes a los antibióticos y reducir el número total de gérmenes lo suficiente como para que el cuerpo lo gestione, especialmente si se usan antes o con una sincronización cuidadosa respecto a los antibióticos. Los autores enfatizan que estas son predicciones teóricas, no pruebas clínicas. Su mensaje principal es que se necesitan experimentos bien pensados —guiados por modelos como este— para descubrir cuándo la terapia con fagos puede mejorar realmente los resultados en pacientes con infecciones de prótesis articulares.
Cita: Levin, B.R., Gil-Gil, T., Berryhill, B.A. et al. A theoretical exploration of protocols for treating prosthetic joint infections with combinations of antibiotics and bacteriophage. npj Biofilms Microbiomes 12, 51 (2026). https://doi.org/10.1038/s41522-025-00908-2
Palabras clave: infección de prótesis articular, biopelícula, terapia con bacteriófagos, resistencia a antibióticos, modelización matemática