Clear Sky Science · es
Etapas de la formación de condensados biomoleculares en el ensamblaje pro-β-carboxisoma
Por qué importan las microfábricas de carbono
Las redes tróficas de la Tierra dependen de la fotosíntesis, sin embargo la enzima clave que extrae dióxido de carbono (CO2) del aire, Rubisco, es lenta y se confunde fácilmente con el oxígeno. Las cianobacterias —microbios fotosintéticos microscópicos— resolvieron este problema hace mucho tiempo construyendo “microfábricas” proteicas llamadas carboxisomas que concentran CO2 alrededor de Rubisco. Este estudio desentraña cómo un complejo adaptador crucial, formado por proteínas llamadas ApN y CM, se autoensambla en etapas para ayudar a construir un carboxisoma funcional. Comprender esta coreografía podría guiar esfuerzos para instalar sistemas similares de potenciación de CO2 en cultivos y aumentar su rendimiento.
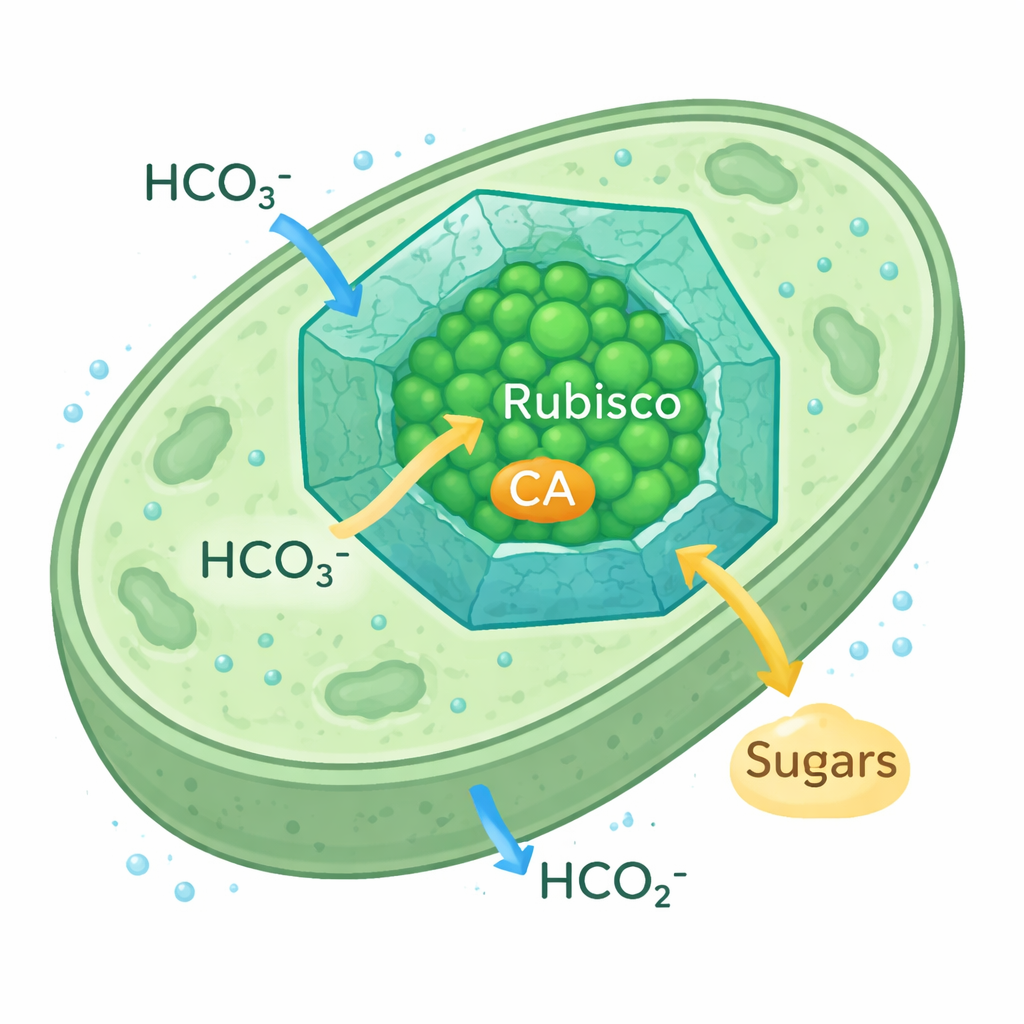
Cómo los microbios potencian la captura de carbono
Los carboxisomas de las cianobacterias son pequeños compartimentos proteicos icosaédricos que se sitúan dentro de la célula. Su envoltura proteica permite la entrada de iones bicarbonato mientras ralentiza la fuga de CO2, creando una burbuja rica en CO2 alrededor de Rubisco y su enzima compañera, la anhidrasa carbónica (CA), que convierte bicarbonato en CO2. Este mecanismo de concentración de CO2 permite a las cianobacterias prosperar incluso cuando el CO2 ambiental es escaso. Dado que la forma de Rubisco usada en estos carboxisomas se asemeja a la Rubisco vegetal, los investigadores los consideran un modelo realista para reingeniería de cloroplastos vegetales con el fin de captar carbono con mayor eficiencia.
La pieza del rompecabezas que conecta con la envoltura
Antes de que se forme la envoltura proteica rígida, las cianobacterias construyen primero un condensado blando, similar a una gota, llamado “pro-carboxisoma”. Trabajos anteriores mostraron que una proteína andamio llamada CM reúne a Rubisco y a la CA dentro de esta gota. El eslabón perdido era cómo la proteína adaptadora de la envoltura ApN se incorpora a esta estructura y más tarde la conecta con las proteínas de la envoltura. Los autores descubrieron que cuando ApN se expresa sola forma un tetrámero que ignora a los demás componentes del carboxisoma. En ese estado ApN no puede ser incorporada a las gotas con Rubisco, CM y CA, lo que sugiere que durante el ensamblaje real del carboxisoma debe existir otra forma de ApN.
Adaptadores co-construidos y un interruptor redox
Al observar la disposición genética en cianobacterias, el equipo notó que apn se encuentra inmediatamente después de cm en el mismo operón, por lo que ambas proteínas suelen sintetizarse juntas. Imitando esto en bacterias, coexpresaron ApN y CM a partir de un mismo fragmento de ADN. Bajo estas condiciones ApN dejó de formar un tetrámero independiente. En su lugar, tres subunidades de ApN y una subunidad de CM se ensamblaron en un complejo adaptador específico de cuatro partes, denotado (ApN)3:CM. Este hetero‑complejo se unió con facilidad a Rubisco, CA y CM y pudo incorporarse a condensados. El modelado estructural y la criomicroscopía electrónica mostraron que ApN y CM se encuentran mediante una interfaz «lengua‑y‑ranura» finamente ajustada; cuando residuos clave de ApN en esta interfaz fueron mutados, el adaptador no se formaba y las células no construían carboxisomas adecuados.
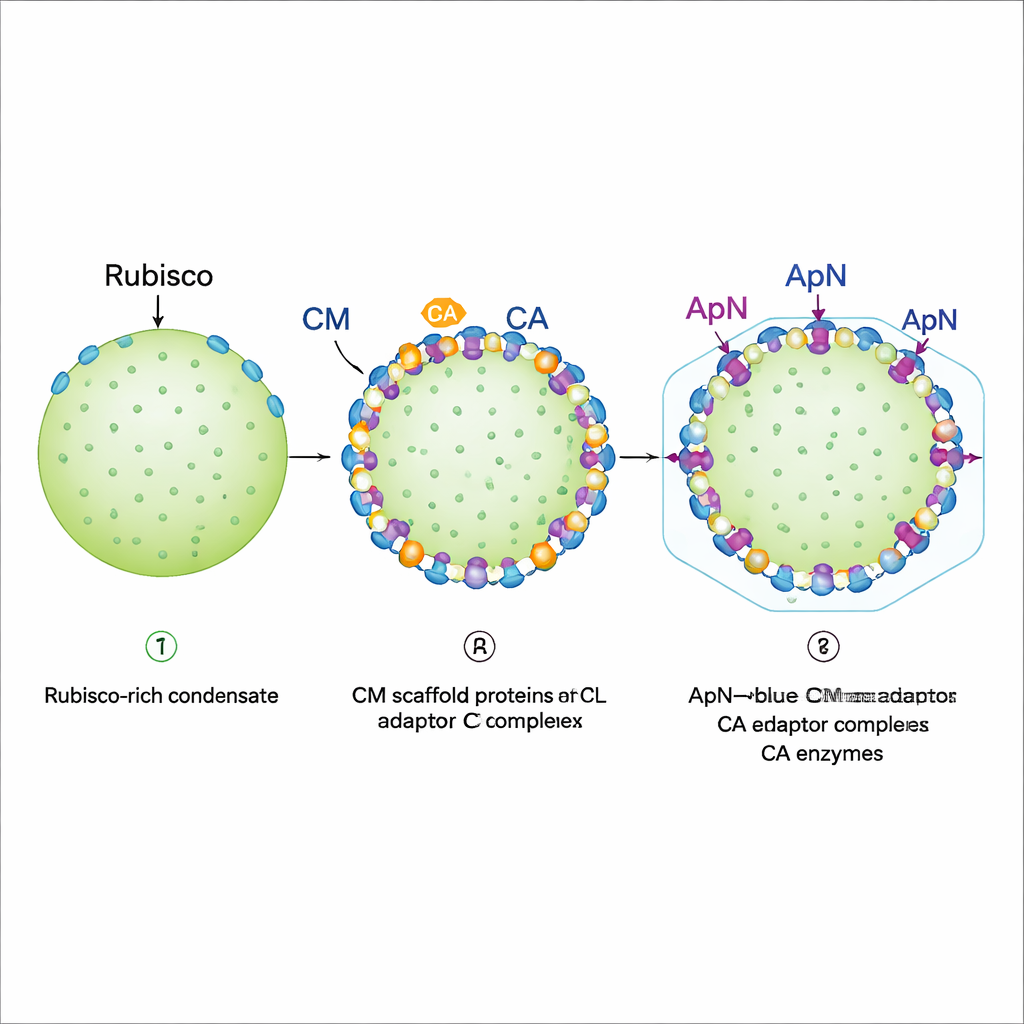
Posicionamiento en el borde y preparación para la envoltura
La imagen por fluorescencia de gotas reconstituidas reveló un programa de ensamblaje por pasos. Primero, Rubisco, CM de longitud completa y una variante más corta de CM forman un condensado denso que se comporta como un gel: Rubisco queda esencialmente inmovilizado. A continuación se añaden CA y el complejo (ApN)3:CM. Ambos tienden a asentarse en el borde exterior de la gota existente, siempre que CA llegue antes o al mismo tiempo que (ApN)3:CM. Esta localización en el borde es crucial porque la cola de ApN porta un «péptido de encapsulación» que se une a las proteínas de la envoltura. Los autores también descubrieron un interruptor redox incorporado: a medida que el interior del carboxisoma en maduración se vuelve más oxidante, dos residuos de cisteína conservados en ApN pueden oxidarse, empujando al adaptador desde un tetrámero (ApN)3:CM hacia un trímero (ApN)2:CM. En células cianobacterianas vivas, alterar estas cisteínas ralentizó el crecimiento y produjo carboxisomas sobredimensionados pero aún funcionales, subrayando su papel en el ajuste fino de la maduración.
Lecciones para diseñar mejores cultivos
Para un no especialista, estos detalles moleculares pueden sonar arcánicos, pero se resumen en un mensaje sencillo: el tiempo y la asociación importan. El trabajo muestra que ApN debe producirse de forma concomitante con CM para evitar formar un autoensamblaje inútil y, en su lugar, convertirse en un adaptador que se coloca en la superficie del pro‑carboxisoma, listo para reclutar la envoltura. Un paso sensible al estado redox ayuda luego a remodelar este adaptador a medida que el compartimento se cierra y su química interna cambia. Para los ingenieros vegetales que esperan trasplantar la maquinaria cianobacterial de concentración de CO2 a cultivos, el estudio destaca que no basta con mover piezas individuales; también hay que respetar el orden, las proporciones y los disparadores químicos que guían el ensamblaje del carboxisoma en la naturaleza.
Cita: Zang, K., Hong, X., Nguyen, N.D. et al. Stages of biomolecular condensate formation in pro-β-carboxysome assembly. Nat. Plants 12, 447–464 (2026). https://doi.org/10.1038/s41477-026-02227-6
Palabras clave: ensamblaje del carboxisoma, mecanismo de concentración de CO2 en cianobacterias, condensados de Rubisco, condensados biomoleculares, fotosíntesis sintética