Clear Sky Science · es
El perfil molecular multicapa informa el diagnóstico y la terapia dirigida del tumor desmoplásico de pequeñas células redondas
Un cáncer raro que necesita mejores respuestas
El tumor desmoplásico de pequeñas células redondas (DSRCT) es un cáncer extremadamente raro y agresivo que afecta principalmente a niños, adolescentes y adultos jóvenes. Debido a su escasa frecuencia y a que puede imitar a otros tumores al observarlo al microscopio, los médicos a menudo tienen dificultades para diagnosticarlo correctamente y elegir tratamientos efectivos. Este estudio plantea una pregunta simple pero poderosa: si analizamos en profundidad los tumores de DSRCT en muchos niveles moleculares —no solo el ADN, sino también el ARN, los patrones proteicos y las marcas químicas en el ADN—, ¿podemos afinar el diagnóstico y descubrir nuevas opciones de tratamiento más precisas para pacientes que ya han agotado las terapias estándar?
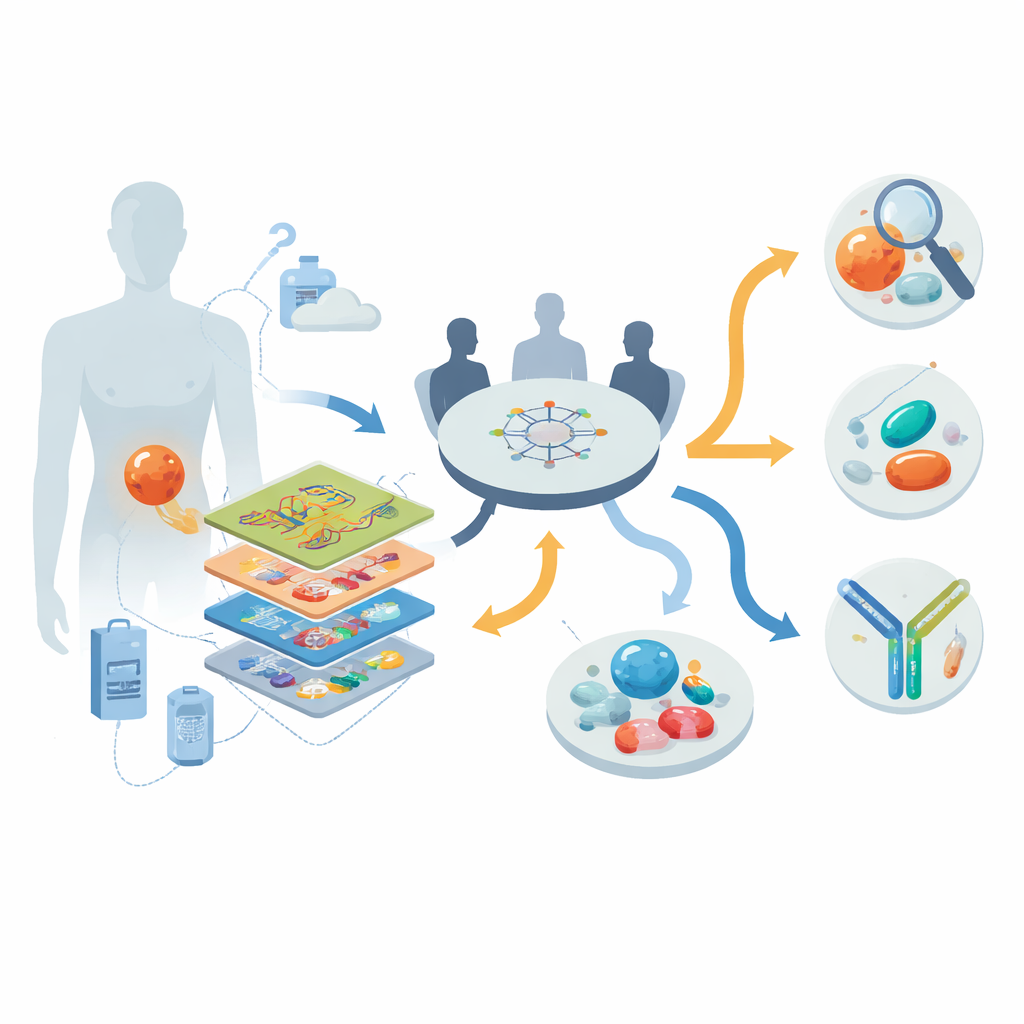
Mirar los tumores capa por capa
Los investigadores trabajaron dentro de un programa nacional de oncología de precisión en Alemania, reclutando a 30 personas con DSRCT avanzado, en su mayoría resistente al tratamiento, entre 2013 y 2022. Para cada paciente aplicaron un conjunto de herramientas “multi-ómicas”: secuenciación del genoma completo o del exoma para estudiar el ADN; secuenciación de ARN para ver qué genes estaban activamente encendidos; perfilado de metilación del ADN para capturar huellas epigenéticas; y, en nueve pacientes, mediciones detalladas de proteínas y fosfoproteínas que revelan qué vías de señalización están realmente activas. Una junta multidisciplinaria de tumores revisó estos datos junto con la historia clínica de cada paciente para generar recomendaciones individualizadas de clarificación diagnóstica, fármacos dirigidos y ensayos clínicos.
Corregir diagnósticos erróneos y revelar dianas ocultas
Un hallazgo sorprendente fue la frecuencia con la que el perfilado profundo corrigió el diagnóstico inicial. En ocho de los 30 pacientes, tumores etiquetados inicialmente como otras entidades —como cánceres de origen desconocido o sarcomas vagamente definidos— fueron reclasificados como DSRCT una vez que se identificó una fusión génica distintiva (EWSR1::WT1) y un patrón de metilación característico. Al mismo tiempo, el ADN de estos tumores resultó estar relativamente tranquilo: había pocas mutaciones y solo cambios ocasionales en el número de copias, por lo que los enfoques clásicos de “gen mutado = diana terapéutica” ofrecían poco. En cambio, las pistas más ricas provinieron de las capas de ARN y proteína. Al comparar la actividad génica en DSRCT con cientos de otros sarcomas, el equipo encontró sobreexpresión reiterada de varias moléculas de superficie y enzimas de señalización que, en principio, podrían ser atacadas con fármacos existentes o emergentes.
De las señales moleculares a tratamientos personalizados
Basándose en estos patrones, la junta tumoral emitió 107 sugerencias de manejo informadas molecularmente para 28 de los 30 pacientes. La mayoría de las recomendaciones incluían fármacos que bloquean tirosina quinasas —enzimas clave que impulsan el crecimiento celular y la formación de vasos sanguíneos— o estrategias más nuevas que se dirigen a proteínas de superficie altamente expresadas. Ejemplos incluidos inhibidores de quinasas de pequeña molécula como pazopanib; radiación basada en péptidos dirigida a receptores de somatostatina; células CAR T experimentales dirigidas a la molécula de adhesión CLDN6; y conjugados anticuerpo–fármaco que entregan toxinas a las células que presentan el receptor ERBB2 (HER2). Diecisiete pacientes se consideraron elegibles para ensayos clínicos emparejados con biomarcadores, lo que subraya cómo datos moleculares detallados pueden abrir puertas a estudios que de otro modo serían difíciles de acceder para personas con una enfermedad ultra-rara.
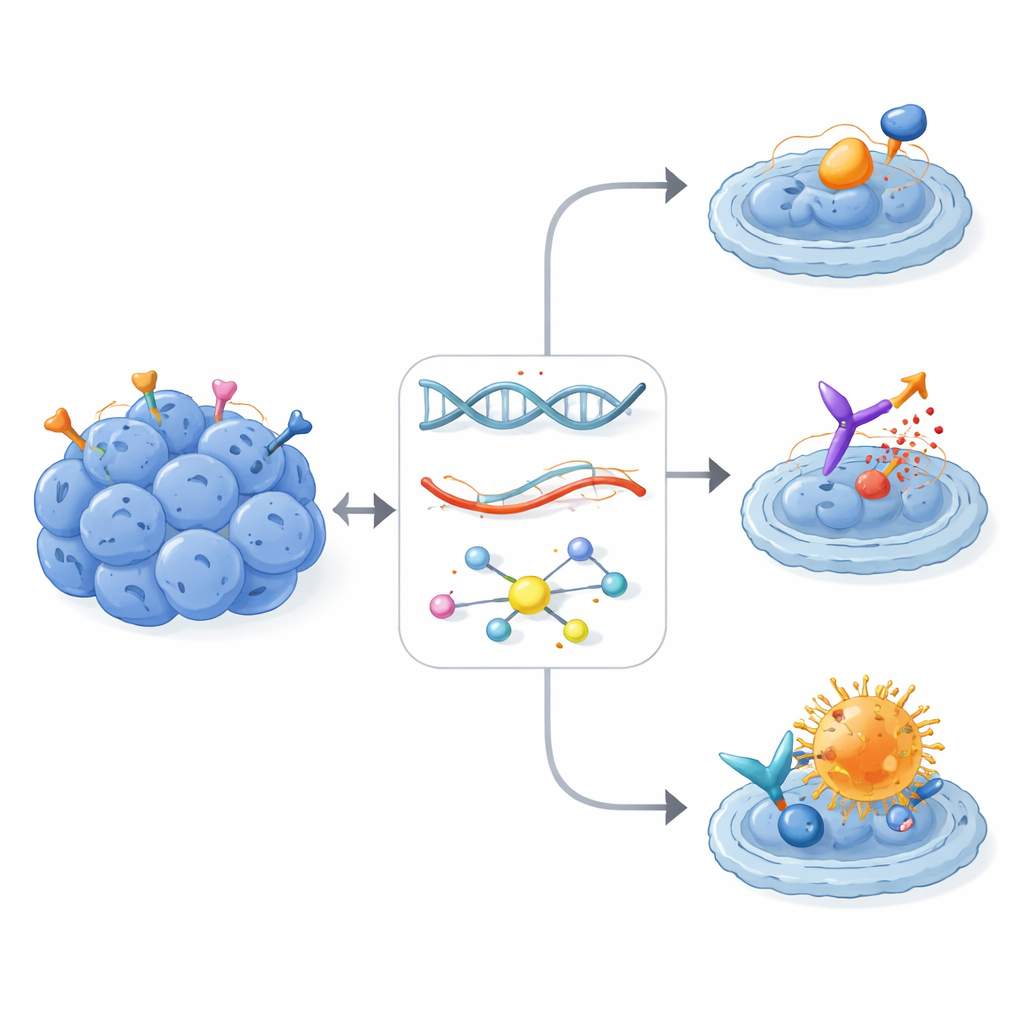
Impacto en el mundo real en pacientes muy pretratados
De todas las terapias personalizadas recomendadas, 16 se administraron realmente a 13 pacientes, todas guiadas por señales a nivel de ARN y a veces refinadas por datos de fosfoproteínas. Aunque estos individuos ya habían pasado por múltiples rondas de quimioterapia y tratamientos locales, ocho de los 13 lograron control de la enfermedad —cinco con reducción parcial del tumor y tres con enfermedad estable. Los inhibidores multitarget de tirosina quinasa, con mayor frecuencia pazopanib, produjeron beneficios significativos y en ocasiones duraderos en varios pacientes, especialmente cuando las dianas conocidas del fármaco estaban claramente sobreactivadas en el tumor. Quizá lo más notable fueron dos pacientes con alta expresión de ERBB2 que recibieron el conjugado anticuerpo–fármaco trastuzumab deruxtecan (T-DXd). Ambos experimentaron respuestas prolongadas de hasta dos años o más, a pesar de haber agotado muchas líneas terapéuticas previas y a pesar de que el receptor ERBB2 no mostraba el patrón de activación fuerte típicamente requerido para los fármacos clásicos que bloquean ERBB2.
Qué significa esto para los pacientes y la atención futura
Para las personas con DSRCT, el estudio ofrece un mensaje de cauteloso optimismo. Aunque este cáncer tiene pocas mutaciones de ADN evidentes para explotar, analizar múltiples capas moleculares puede tanto corregir errores diagnósticos como revelar debilidades accionables que son invisibles para las pruebas estándar. El trabajo demuestra que, incluso en una enfermedad rara y agresiva, un enfoque guiado por la biología puede producir beneficio clínico real, incluidas respuestas duraderas a fármacos como pazopanib y trastuzumab deruxtecan. Más ampliamente, apoya que los pacientes con DSRCT —y, por extensión, otros cánceres ultra-raros— se beneficien del acceso rutinario a un perfilado molecular exhaustivo y a la revisión experta, allanando el camino para futuros ensayos en los que los tratamientos se elijan no solo por el tipo de tumor, sino por las huellas moleculares únicas del cáncer de cada persona.
Cita: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
Palabras clave: tumor desmoplásico de pequeñas células redondas, oncología de precisión, perfilado multi-ómico, terapia dirigida, conjugados anticuerpo-fármaco