Clear Sky Science · es
Interacción de la acetilación O de ácido siálico en el Golgi dependiente e independiente de SLC33A1 en la catálisis por CASD1
Cómo pequeños ajustes azucarados pueden moldear la salud y la enfermedad
Nuestras células están recubiertas por cadenas de azúcares complejas que actúan como carnés de identidad molecular, orientando la inmunidad, el desarrollo e incluso la forma en que los virus se adhieren. Este estudio explora una modificación sutil pero poderosa de esos azúcares: la adición de pequeñas “tapas” químicas llamadas grupos acetilo a un azúcar terminal denominado ácido siálico, y revela una sorprendente máquina molecular de dos partes que controla este proceso dentro del aparato de Golgi de la célula. Comprender este sistema oculto ayuda a explicar ciertos trastornos neurológicos graves y ofrece pistas sobre cómo las células ajustan finamente su superficie en salud y enfermedad. 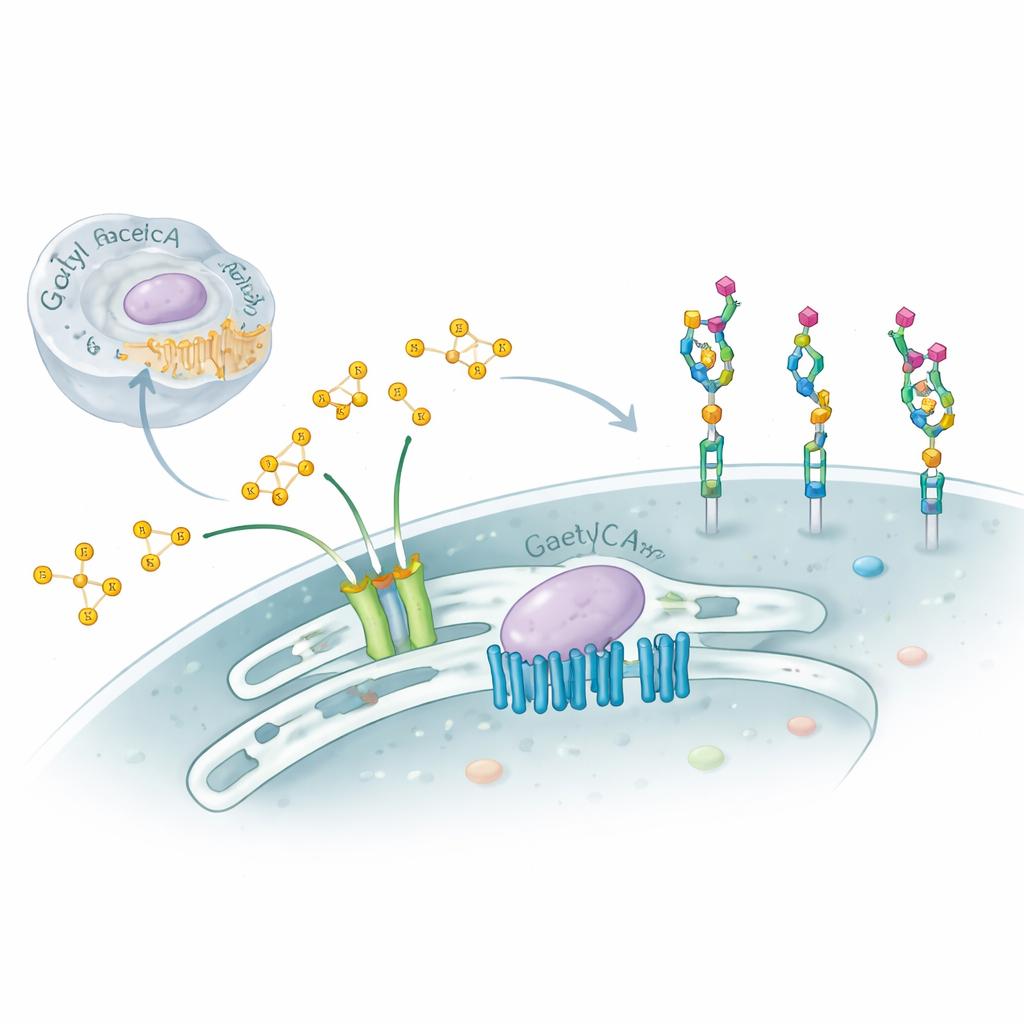
Los azúcares especiales en la superficie celular
Los ácidos siálicos se sitúan en las puntas externas de muchos azúcares de superficie celular en proteínas y lípidos, especialmente en moléculas denominadas gangliósidos en el cerebro. Al modificar ligeramente los ácidos siálicos —por ejemplo añadiendo uno o dos grupos acetilo en posiciones específicas—, las células pueden enmascarar sitios de reconocimiento existentes o crear otros nuevos. Virus como la influenza C y algunos coronavirus buscan específicamente estos azúcares modificados, y los gangliósidos acetilados pueden influir en si las neuronas sobreviven o mueren, así como en el crecimiento del cáncer. Sin embargo, a pesar de su importancia, el funcionamiento interno de la maquinaria celular que coloca estos grupos acetilo en el Golgi ha permanecido poco comprendido.
Un transportador y una enzima trabajan mano a mano
Los investigadores se centraron en dos proteínas que residen en o alrededor del Golgi: SLC33A1, un transportador que mueve acetil‑CoA (el principal donante de acetilos de la célula) a través de membranas, y CASD1, una enzima conocida por transferir grupos acetilo a los ácidos siálicos. Usando edición génica en líneas celulares humanas y de hámster, eliminaron SLC33A1 y observaron qué ocurría con gangliósidos específicos. Las células sin SLC33A1 todavía podían sintetizar los gangliósidos básicos GD3 y GD2, pero perdían por completo sus formas 9‑O‑acetiladas, una modificación distintiva vinculada al cáncer y la función neuronal. Reintroducir SLC33A1 humano restauró estos gangliósidos acetilados, demostrando que SLC33A1 es un suministrador crucial de acetil‑CoA para esta vía. 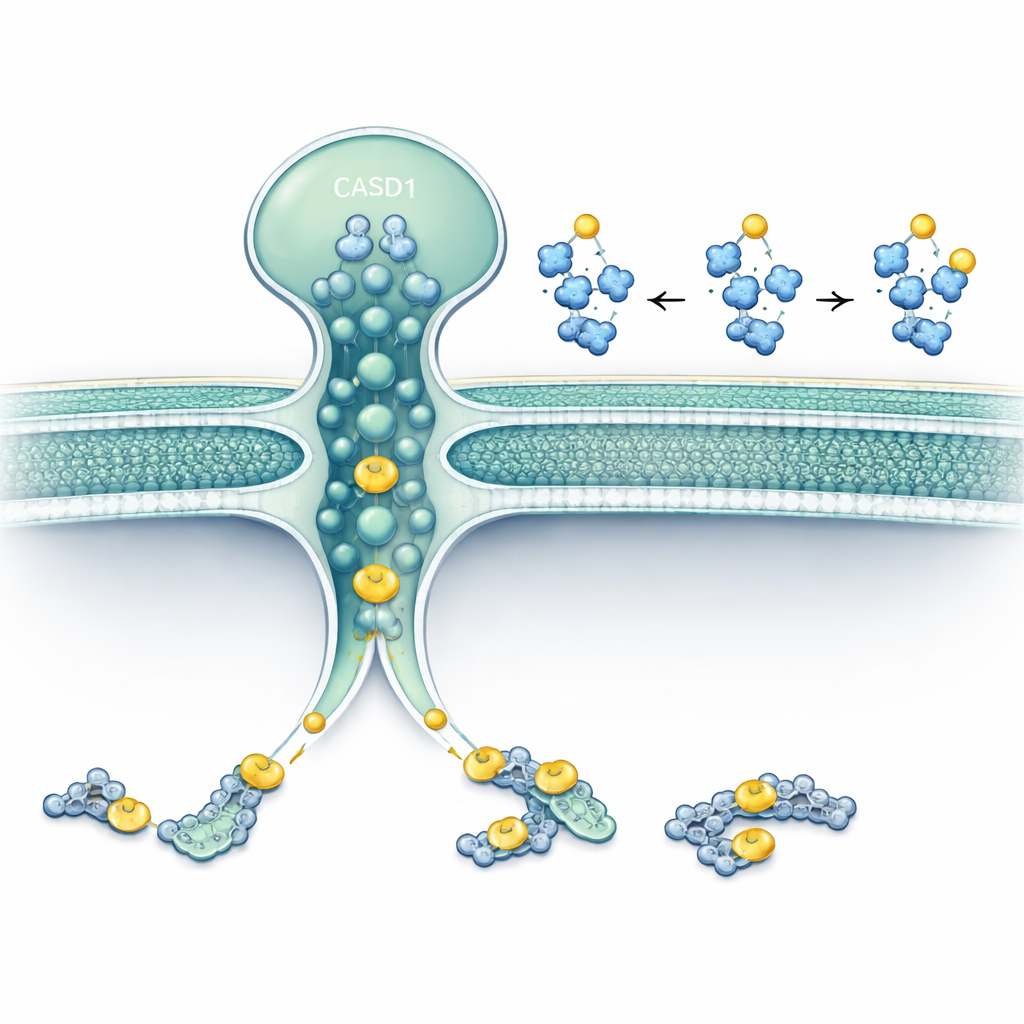
Mutaciones en pacientes revelan relevancia clínica
SLC33A1 se ha implicado en varias enfermedades neurológicas raras, incluyendo un trastorno infantil severo (síndrome de Huppke–Brendel), una forma de paraplejía espástica hereditaria y ataxia cerebelosa de aparición tardía. El equipo recreó cuatro variantes de SLC33A1 derivadas de pacientes en células carentes del transportador normal y probó si estas proteínas alteradas podían rescatar la acetilación de gangliósidos. Las cuatro mostraron función reducida, y las mutaciones más graves de inicio en la infancia apenas restauraron la acetilación. Guiados por una estructura tridimensional recientemente resuelta de SLC33A1, los autores mapearon estas mutaciones en la proteína y mostraron cómo probablemente alteran su arquitectura o su capacidad para unirse a acetil‑CoA. Esto sugiere con fuerza que la deficiente acetilación de gangliósidos contribuye a los síntomas neurológicos observados en los pacientes.
Un segundo sitio activo oculto en CASD1
El trabajo también descubrió un giro inesperado: CASD1 parece ser una enzima con doble propósito. Su conocida porción en la luz del Golgi utiliza acetil‑CoA suministrado por SLC33A1. Pero cuando SLC33A1 fue eliminado, las células aún consiguieron colocar un único grupo acetilo en ciertos ácidos siálicos en algunas condiciones, aunque no lograron añadir el segundo acetilo necesario para patrones más complejos. Empleando predicción avanzada de estructuras y simulaciones moleculares, los autores mostraron que la parte transmembrana de CASD1 se asemeja mucho a una acetiltransferasa transmembrana conocida de lisosomas. Identificaron aminoácidos clave en esta región que se unen a acetil‑CoA en el lado citosólico y transmiten su grupo acetilo a través de la membrana directamente al ácido siálico. Cuando estos residuos se mutaron, CASD1 perdió esta segunda actividad tanto en ensayos de tubo de ensayo como en células vivas.
Dos vías, un código azucarado finamente ajustado
En conjunto, los datos respaldan un modelo de “dos sitios catalíticos”. Una vía depende de SLC33A1 para llevar acetil‑CoA al lumen del Golgi, donde el dominio luminal de CASD1 añade un grupo acetilo al ácido siálico, permitiendo patrones de acetilación simples y dobles. La otra vía está integrada en el núcleo transmembrana de CASD1, que toma directamente acetil‑CoA citosólico y puede todavía llevar a cabo un nivel básico de acetilación incluso cuando falta SLC33A1. Para el lector general, esto significa que una sola enzima, alimentada por dos fuentes diferentes de acetilos, escribe sutiles “marcas de puntuación” en los azúcares de la superficie celular. Cuando el transportador o cualquiera de las partes de la enzima falla, estas marcas se colocan mal o faltan, lo que puede ayudar a explicar ciertas enfermedades neurodesarrollativas y neurodegenerativas y resalta una nueva capa de regulación en cómo nuestras células moldean su identidad externa.
Cita: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Palabras clave: ácido siálico, acetilación en el Golgi, gangliósidos, SLC33A1, CASD1