Clear Sky Science · es
Dinamismo estructural del midnolin-proteasoma durante la degradación de sustratos independiente de ubiquitina
Cómo las células tiran la basura con urgencia
Dentro de cada célula, las proteínas se fabrican y se destruyen de forma continua. Muchas se marcan con pequeñas moléculas llamadas ubiquitina antes de ser alimentadas a la principal máquina de reciclaje celular, el proteasoma. Pero algunas proteínas nucleares deben eliminarse tan deprisa que no hay tiempo para etiquetarlas. Este estudio revela cómo una proteína auxiliar poco conocida, la midnolina, se acopla directamente al proteasoma para eliminar estos objetivos urgentes, ofreciendo pistas sobre cómo las células mantienen la actividad génica bajo un control estricto y rápido.
Un atajo hacia la trituradora celular
El proteasoma 26S es un complejo en forma de barril que descompone las proteínas en fragmentos pequeños. Tradicionalmente, reconoce los objetivos leyendo cadenas de ubiquitina unidas a ellos. Trabajos recientes han descubierto una ruta alternativa: una vía «atajo» en la que la midnolina escolta ciertas proteínas nucleares—especialmente productos de genes inmediatos tempranos que activan y silencian genes con rapidez—directamente al proteasoma sin etiquetas de ubiquitina. Estas proteínas, como factores de transcripción implicados en respuestas al estrés e inflamación, deben aparecer y desaparecer en cuestión de minutos. El nuevo artículo combina microscopía crioelectrónica de alta resolución con experimentos bioquímicos para mapear, casi fotograma a fotograma, cómo la midnolina se engancha al proteasoma y posiciona su carga para la destrucción.
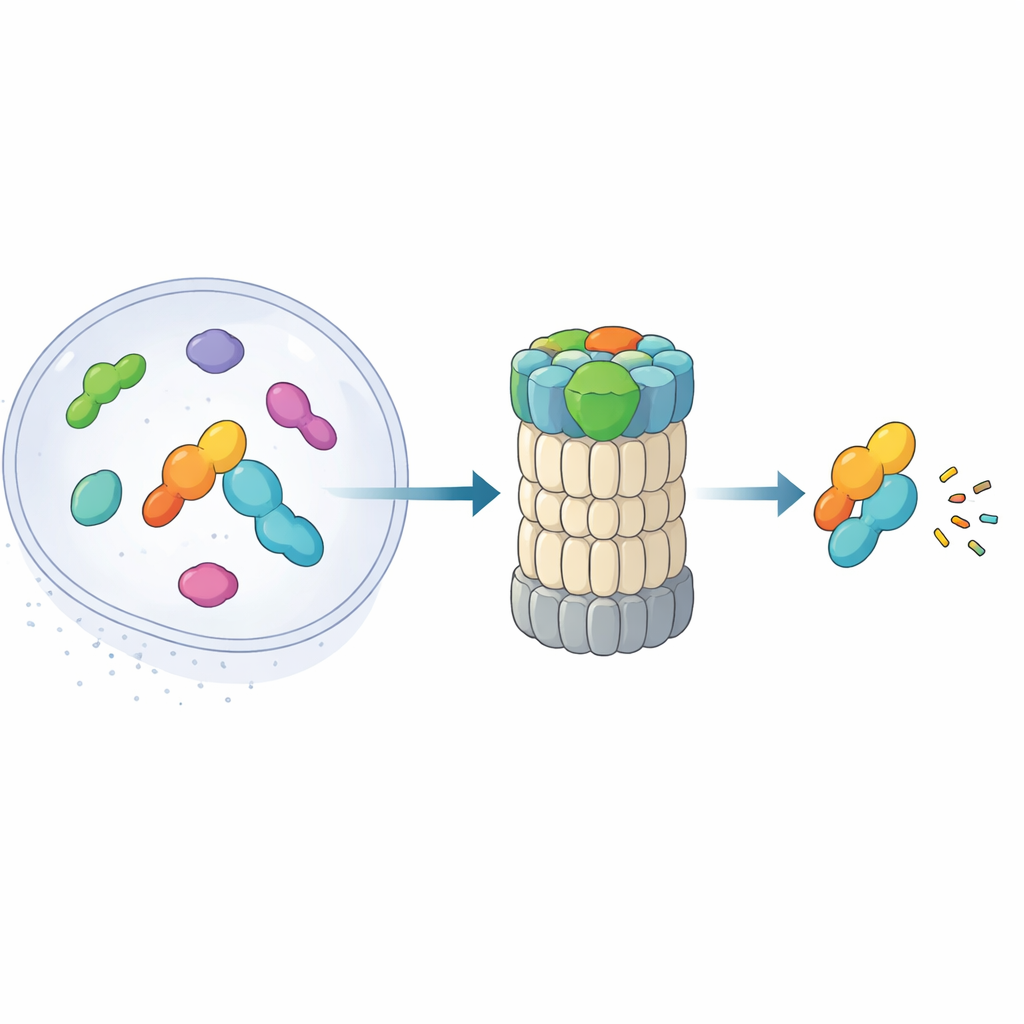
El ayudante de tres partes que agarra y apunta a los objetivos
La midnolina funciona como una herramienta multifunción con tres módulos clave. Un extremo, una hélice C-terminal, se inserta en un sitio de acoplamiento en un componente del proteasoma llamado RPN1, anclando la midnolina a la máquina de reciclaje. Una región central, el «Catch», reconoce y sujeta una característica tipo hebra (un degrón) en sus proteínas objetivo. En el extremo opuesto se sitúa un dominio similar a la ubiquitina. Sorprendentemente, este dominio no sirve principalmente para unir el proteasoma, como hacen dominios similares en otras proteínas portadoras. En cambio, los autores muestran que se aposenta frente a RPN11, una enzima que normalmente recorta la ubiquitina de los sustratos. Aquí, RPN11 actúa más como un andamio: al abrazar el segmento similar a ubiquitina de la midnolina, ayuda a mantener el dominio Catch y su carga directamente sobre el estrecho poro de entrada al proteasoma.
Guiando la proteína hacia el núcleo triturador
Una vez que la midnolina se ha anclado, el motor del proteasoma, un anillo AAA+ ATPasa hambriento de energía, toma el control. Este anillo se sitúa justo debajo del poro de entrada y tira de las cadenas de proteínas desplegadas hacia el núcleo, paso a paso. Las instantáneas de crio-EM revelan una serie de posiciones en forma de «escalera en espiral» adoptadas por las seis subunidades del motor mientras sujetan y transfieren el sustrato por el canal central. Los autores capturaron cuatro etapas consecutivas de este ciclo, todas con material unido a la midnolina pasado por el poro, e incluso observaron cómo la liberación de un ion magnesio en una subunidad coincide con un desplazamiento descendente de todo el anillo. Esto sugiere que el uso coordinado de ATP y la liberación de magnesio ayudan a avanzar enérgicamente la proteína hacia la cámara donde residen los sitios de corte.
Por qué importan el posicionamiento y la coexpresión
El equipo probó cómo contribuye cada módulo de la midnolina a la eficiencia. La hélice de anclaje por sí sola puede unirse a RPN1 pero no aumenta significativamente la actividad del proteasoma. Eliminar el dominio Catch deja muchos proteasomas en un estado inactivo sin sustrato, aunque la midnolina todavía puede acoplarse; sustituir el Catch por un sustrato fusionado permanentemente tampoco logra restaurar la actividad plena. Estos hallazgos indican que Catch hace más que simplemente agarrar el objetivo: también debe orientar la proteína con precisión en la entrada del poro. Datos bioquímicos y de transcriptomas tumorales muestran además que la midnolina tiende a producirse junto con sus sustratos. Cuando se coexpresan, la midnolina se pliega mejor y forma complejos estables, creando un paquete «degrádame» listo que puede entregarse rápidamente al proteasoma cuando la célula necesita restablecer la expresión génica.
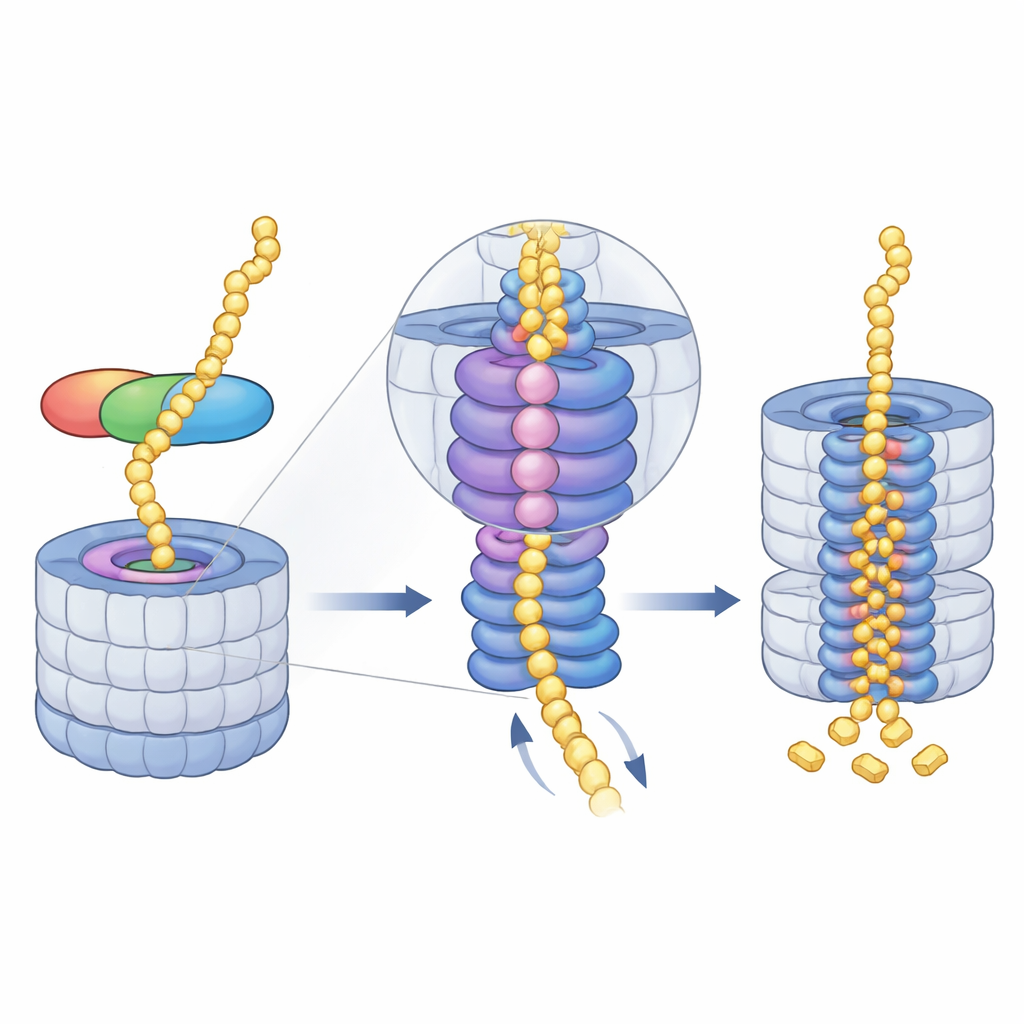
Autolimpieza y posibles aplicaciones médicas futuras
Después de que la proteína objetivo haya sido introducida y troceada, la midnolina misma no queda exenta. Sus propias regiones desestructuradas pueden ser también enhebradas en el motor y alimentadas a la misma cámara de destrucción, lo que asegura que el ayudante no se acumule innecesariamente. Al iluminar esta vía al proteasoma libre de ubiquitina, el estudio amplía nuestra comprensión de cómo las células gestionan la vida útil de las proteínas en calendarios muy ajustados. También sugiere nuevas estrategias terapéuticas: mediante el diseño de moléculas basadas en midnolina que unan directamente proteínas nucleares causantes de enfermedad al proteasoma, los investigadores podrían algún día eliminar objetivos «no modulables» por fármacos, incluidos ciertos impulsores del cáncer, de forma más rápida y selectiva.
Cita: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Palabras clave: proteasoma, midnolina, degradación de proteínas, vía independiente de ubiquitina, genes inmediatos tempranos