Clear Sky Science · es
La competencia transcripcional define el potencial de nucleación de heterocromatina de unidades MSR aisladas
Interruptores ocultos en nuestro ADN
Nuestros genomas están empaquetados dentro del núcleo celular en dos estados principales: regiones activas que albergan genes, y tramos fuertemente compactados considerados durante mucho tiempo como “materia oscura” genética. Este estudio plantea una pregunta aparentemente simple: ¿qué indica a un fragmento de ADN que debe convertirse en este material compactado que silencia genes—conocido como heterocromatina—en primer lugar? Al diseccionar una clase específica de ADN repetitivo en ratones, los autores revelan que no todos los repetidos son iguales: solo aquellos capaces de soportar un tipo especial de transcripción pueden activar el interruptor que construye y mantiene estos vecindarios silenciosos de ADN.
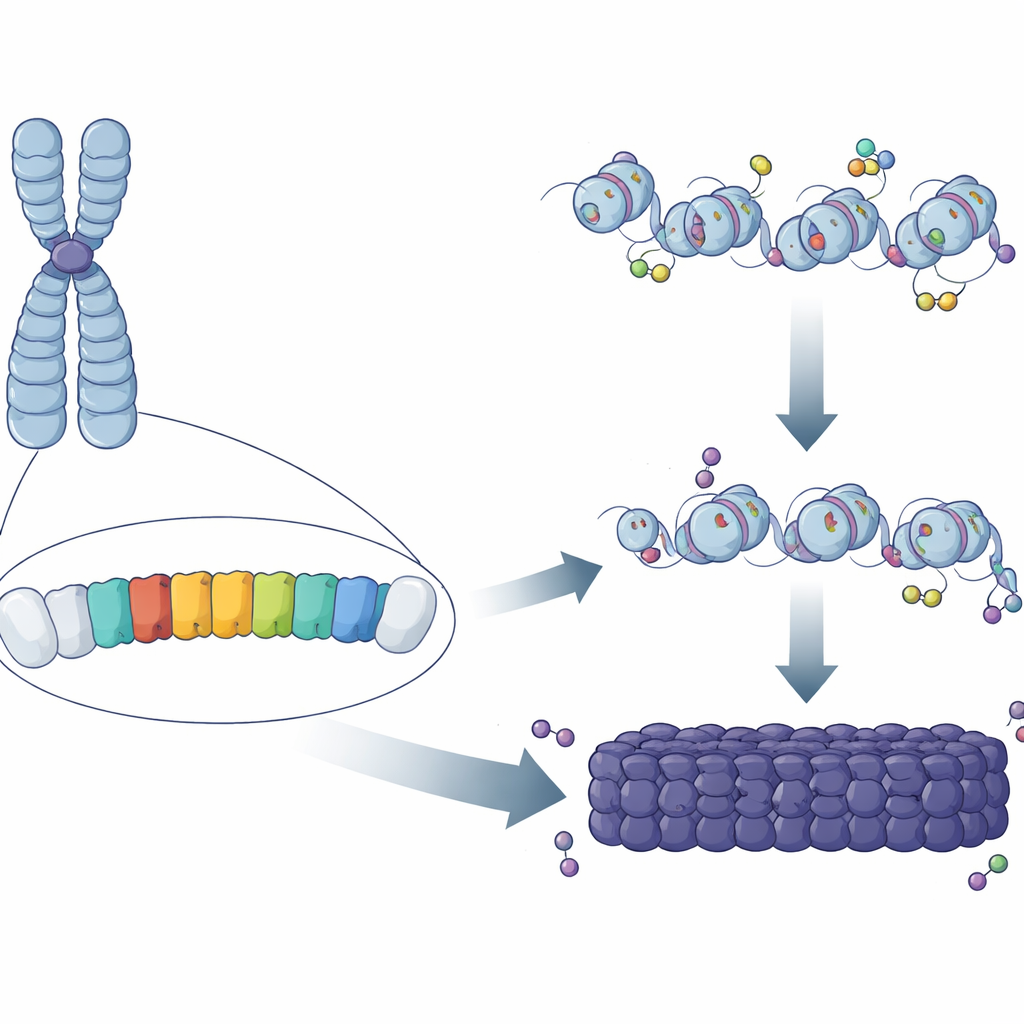
Patrones repetitivos en el genoma
Casi la mitad del ADN de los mamíferos está compuesto por secuencias repetidas, muchas de ellas agrupadas en regiones alrededor del centro del cromosoma. En ratones, un componente principal de estas regiones es la “repetición mayoritaria satélite” (MSR), una corta secuencia rica en A/T copiada cientos de miles de veces. Estudios clásicos mostraron que estas regiones están recubiertas por marcas químicas y proteínas que bloquean el ADN en un estado compacto y protector. Pero seguía siendo un misterio por qué algunas copias de MSR se volvían completamente heterocromáticas mientras otras, dispersas en el genoma, no lo hacían. Los autores razonaron que pequeñas diferencias en la secuencia o el comportamiento de unidades MSR individuales podrían determinar si pueden sembrar, o “nucleizar”, un parche de heterocromatina.
Construir un sitio de prueba en el genoma
Para probar esta idea de forma limpia, el equipo ingenió células madre embrionarias de ratón para contener una plataforma de inserción artificial en un tramo silencioso del cromosoma 2—una región sin genes ni repeticiones cercanas y sin actividad detectable. En este sitio neutro insertaron distintos fragmentos de ADN: unidades MSR intactas, variantes MSR muy reordenadas y elementos de control como promotores virales o secciones de elementos móviles. Esto les permitió preguntar, unidad por unidad, qué secuencias son capaces de atraer las características distintivas de la heterocromatina: una marca química específica en histonas (H3K9me3), unión de proteínas HP1 e incorporación de la histona enlace H1, todo lo cual, en conjunto, espesa y estabiliza la cromatina local.
Sólo los repetidos preparados para la transcripción siembran cromatina silenciosa
Los resultados fueron notablemente selectivos. Una sola unidad MSR intacta insertada en el sitio de prueba no fue suficiente para cambiar la cromatina. Sin embargo, tres o más copias en tándem de la secuencia MSR intacta convirtieron la región circundante en una “isla” de heterocromatina, con H3K9me3 fuerte, HP1 y histona H1. En contraste, tramos de igual longitud de secuencia MSR reordenada, o de otro tipo de repetido (la región 5' no traducida de LINE-1), no lograron hacerlo, aunque podían impulsar una transcripción intensa. La diferencia clave fue que las unidades MSR intactas en multicopia sostenían una transcripción moderada y bidireccional que producía pequeñas moléculas de ARN no estándar estrechamente asociadas a la cromatina. Este patrón, más que una transcripción alta similar a la génica, se correlacionó con la capacidad de nucleizar heterocromatina.
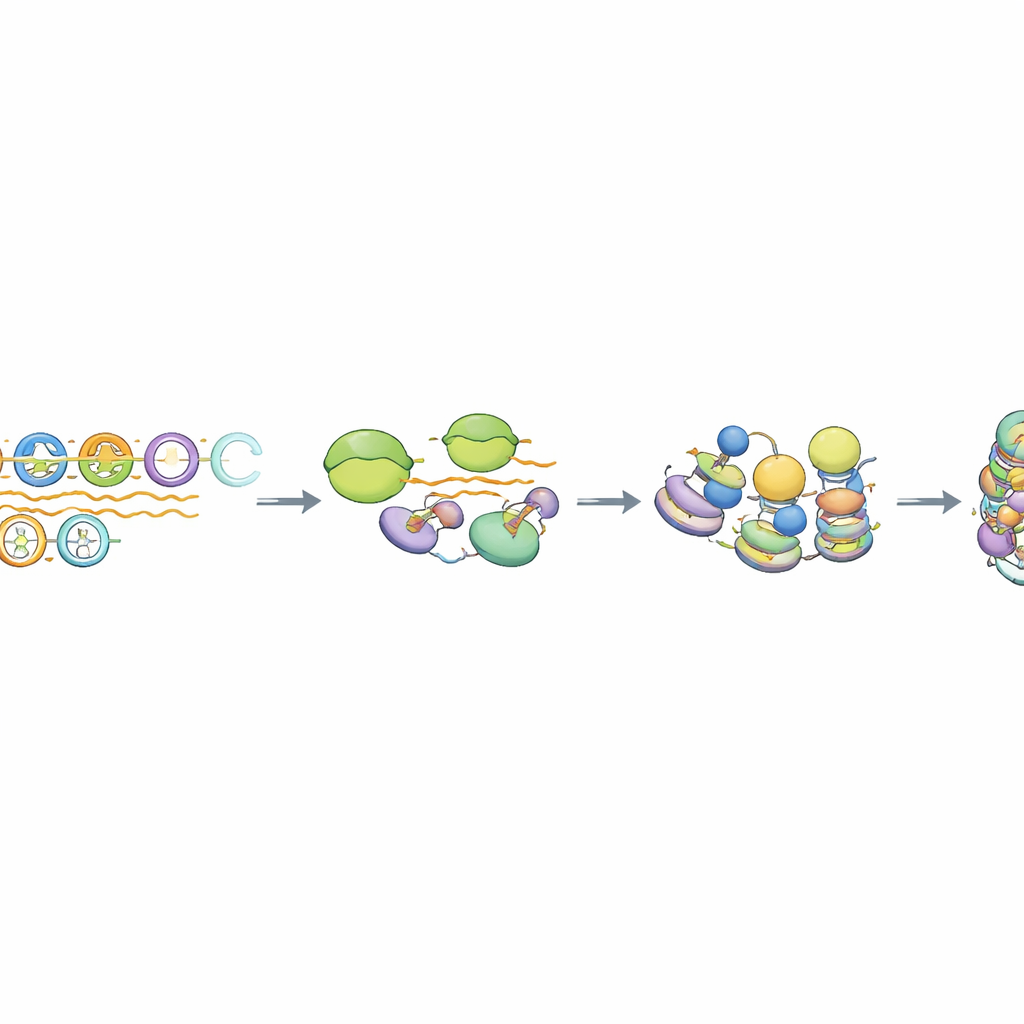
Un tipo especial de transcripción y procesamiento de ARN
Al profundizar, los autores encontraron que la ARN polimerasa II, la enzima que normalmente sintetiza ARNm, se compromete brevemente con las matrices MSR pero no avanza eficientemente hacia transcritos largos. Los ARN resultantes carecen de señales típicas de ARNm, como el cap 5' protector y largas colas poli‑A, y permanecen cerca del ADN que los produjo. Una maquinaria proteica llamada complejo Integrador, conocida por recortar y terminar ciertos ARN no codificantes, estaba específicamente enriquecida en unidades MSR intactas. Cuando se redujo la actividad de corte del Integrador, los niveles de ARN derivados de MSR aumentaron considerablemente, pero la marca histona represiva clave persistió mientras que la unión de HP1 cambió sutilmente. El análisis a escala del genoma mostró que solo el ~10–15% más intacto de las copias MSR se comporta de esta manera, destacando un subconjunto de repetidos “competentes” predispuestos a esta vía de silenciamiento acoplada a la transcripción.
ADN desenrollado como imitación de un promotor
El equipo también exploró cómo el propio ADN MSR favorece esta transcripción inusual. Los arreglos MSR en multicopia, pero no las copias simples o dobles, mostraron signos claros de ADN localmente desenrollado e híbridos ARN:ADN, características estructurales observadas con frecuencia cerca de promotores activos y en sitios de pausa. Estas configuraciones se intensificaron cuando se inhibieron enzimas topoisomerasas, y coincidieron con una mayor transcripción de MSR y rasgos de heterocromatina más fuertes. Los autores proponen que tres o más unidades MSR en tándem crean una topología física del ADN que imita un promotor, invitando a la polimerasa y a los factores de transcripción a participar lo justo para generar ARN cortos que, junto con proteínas específicas, refuerzan una arquitectura de cromatina compacta.
Por qué esto importa para la salud genómica
Para un observador no especializado, este trabajo revela que partes de nuestro ADN “basura” actúan como interruptores finamente ajustados, usando una mezcla de forma del ADN, transcripción de bajo nivel y procesamiento de ARN para construir la capa protectora del genoma. Solo las unidades MSR que pueden soportar esta transcripción controlada y no codificante pueden provocar nueva heterocromatina, mientras que los elementos reordenados o excesivamente activos no pueden. Esta lógica basada en ADN/ARN ayuda a explicar cómo las células distinguen entre regiones que deben mantenerse silenciosas y aquellas que pueden albergar genes, y por qué los ARN satélite mal regulados se asocian con cáncer y problemas del desarrollo. En esencia, el estudio muestra que el “fondo” repetitivo del genoma no es relleno pasivo sino un ingeniero activo de la arquitectura y la estabilidad nuclear.
Cita: Lo, YH., Shukeir, N., Erikson, G. et al. Transcriptional competence defines the heterochromatin nucleating potential of isolated MSR units. Nat Commun 17, 2653 (2026). https://doi.org/10.1038/s41467-026-70991-2
Palabras clave: heterocromatina, ADN satélite, ARN no codificante, estructura de la cromatina, estabilidad genómica