Clear Sky Science · es
Heterogeneidad espacial de las MDSC mediada por la señalización ANXA1-FPRs impulsa la supresión inmunitaria en la progresión del OSCC
Por qué las defensas del cuerpo flaquean ante algunos cánceres bucales
El carcinoma de células escamosas oral, una forma común de cáncer de la boca, a menudo resiste los tratamientos oncológicos más prometedores de hoy: las inmunoterapias que liberan las defensas del propio organismo. Este estudio plantea una pregunta básica pero crucial: ¿por qué células inmunitarias potentes, que deberían reconocer y destruir el cáncer, fracasan tan a menudo en estos tumores? Al cartografiar dónde se encuentran las distintas células dentro del tumor y cómo se comunican entre sí, los investigadores descubren un juego cambiante de “gato y ratón” entre las células cancerosas, las células supresoras inmunitarias y las células T citotóxicas que ayuda a explicar el fracaso del tratamiento—y sugiere una forma de corregirlo. 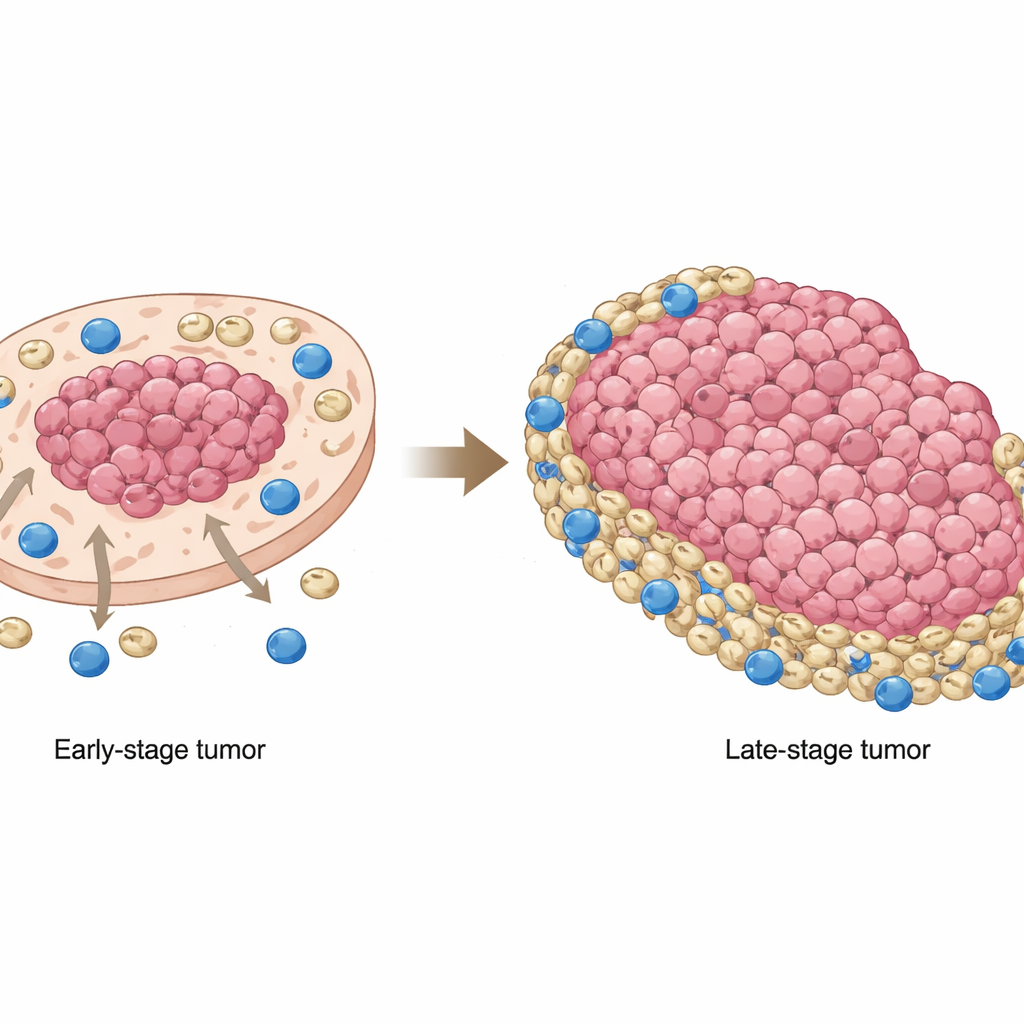
El paisaje oculto dentro de un tumor
Los autores combinaron dos enfoques de vanguardia: secuenciación de ARN unicelular, que lee la actividad de células individuales, y transcriptómica espacial, que muestra dónde se ubican esas células en cortes reales de tejido tumoral. Analizando tumores de pacientes con cáncer oral en estadios tempranos y avanzados, identificaron los principales actores celulares: células epiteliales cancerosas, células T CD8 “asesinas”, otras células T y B, fibroblastos que proporcionan soporte estructural y células inmunitarias especializadas llamadas células supresoras derivadas de la médula (MDSC). Mientras que en tumores tempranos se observó mayor actividad de las células T CD8, en tumores de estadio tardío se detectó una señalización T debilitada y señales inmunosupresoras más intensas procedentes de células mieloides, lo que apunta a un entorno progresivamente más hostil para la inmunidad anticancerígena.
Células supresoras en movimiento
Uno de los hallazgos más llamativos fue cómo cambiaba la posición de las MDSC a medida que avanzaba el tumor. En cánceres en fase temprana, estas células supresoras tendían a agruparse dentro de regiones ricas en células tumorales, cerca del núcleo del tumor. En fases más avanzadas, se desplazaban hacia el exterior, acumulándose en áreas pobres en tumor y en los márgenes, donde las células T CD8 eran más comunes. Esto significaba que en tumores avanzados las células T citotóxicas quedaban en gran parte empujadas hacia los bordes y allí se encontraban con un cinturón de MDSC que amortiguaba su capacidad de atacar a las células cancerosas. Muestras de pacientes y modelos en ratón confirmaron que esta redistribución no era solo una curiosidad: cuando la superposición entre MDSC y células tumorales era menor y las MDSC acampaban en regiones no tumorales, los pacientes presentaban una supervivencia global peor. 
Un cambio de señalización entre células cancerosas y supresoras
El estudio se centró en una “conversación” molecular entre células tumorales y MDSC que implicaba una proteína llamada anexina A1 (ANXA1) en las células tumorales y una familia de receptores llamada FPR en las células mieloides. En la enfermedad temprana, ANXA1 en las células cancerosas activaba fuertemente FPR1 y FPR3, especialmente en MDSC y macrófagos asociados al tumor, ayudando a reclutar y mantener a estas células supresoras en el núcleo tumoral. A medida que el cáncer progresó, los niveles de ANXA1 en las células tumorales disminuyeron, debilitando esas conexiones originales. Al mismo tiempo, más MDSC comenzaron a expresar otro receptor, FPR2, y la señalización ANXA1–FPR2 emergió como una vía compensatoria para mantener a las MDSC comprometidas. Un subconjunto específico de células tumorales con altos niveles de ANXA1, que también mostraba rasgos similares a células madre, pareció actuar como “cebo”, atrayendo a las MDSC en fases tempranas; cuando ANXA1 disminuyó, las MDSC dejaron de estar ancladas en el núcleo y se desplazaron hacia regiones ricas en células T CD8.
Desactivar el escudo para ayudar a que la inmunoterapia funcione
Para comprobar si romper esta comunicación podía mejorar el tratamiento, los investigadores usaron un modelo murino de cáncer oral y bloquearon FPR2 con un inhibidor de pequeña molécula llamado WRW4. Por sí sola, la inhibición de FPR2 redujo la presencia de MDSC y aumentó las células T CD8 en el microambiente tumoral, pero no ralentizó lo suficiente el crecimiento tumoral. De igual modo, el tratamiento con un anticuerpo anti–PD-1 por sí solo produjo beneficios modestos, porque las MDSC seguían formando una barrera supresora. Sin embargo, cuando ambos fármacos se combinaron, el crecimiento tumoral se redujo drásticamente y los ratones vivieron más tiempo. En estos animales, la infiltración de MDSC cayó en picado mientras que las células T CD8 penetraron más profundamente en regiones ricas en células tumorales, lo que sugiere que bloquear FPR2 elimina un escudo clave que normalmente protege a las células cancerosas del ataque inmunitario.
Qué significa esto para la atención oncológica futura
En conjunto, el trabajo muestra que no solo los tipos de células sino también su disposición espacial y sus asociaciones de señalización determinan si la inmunoterapia puede tener éxito en el cáncer oral. A medida que los tumores avanzan, las MDSC migran del centro a los bordes, donde interceptan a las células T citotóxicas, y la señalización ANXA1–FPR2 ayuda a mantener esta disposición supresora. Al interrumpir esta vía—especialmente en combinación con los fármacos de bloqueo de puntos de control existentes—los médicos podrían reconfigurar el microambiente tumoral para que las propias células inmunitarias del organismo vuelvan a reconocer y destruir el cáncer. Esto sugiere una estrategia concreta: combinar bloqueadores de FPR2 con inmunoterapia podría mejorar los resultados en pacientes cuyos cánceres orales resisten actualmente los mejores tratamientos disponibles.
Cita: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
Palabras clave: carcinoma de células escamosas oral, microambiente tumoral, células supresoras derivadas de la médula, transcriptómica espacial, inmunoterapia del cáncer