Clear Sky Science · es
La señalización FGFR establece gradientes espaciales de identidades de células secretoras a lo largo del eje proximal-distal de la vía aérea
Cómo nuestras vías respiratorias ordenan y defienden silenciosamente el aire que respiramos
Cada respiración hace pasar aire sobre millones de células que recubren la tráquea y los pulmones. Estas células hacen mucho más que ofrecer una superficie pasiva: desintoxican contaminantes, combaten gérmenes y ayudan a evitar el colapso de los pequeños sacos de aire. Este estudio revela que las células secretoras en la vía aérea del ratón no son todas iguales. En cambio, están organizadas en gradientes suaves desde la región próxima a la garganta (proximal) hasta las partes más profundas del pulmón (distal), y una vía de señalización clave, denominada FGFR2b, contribuye a establecer y mantener estos desplazamientos graduales en la identidad y función celular. Comprender este orden oculto aporta información sobre cómo los pulmones se mantienen sanos y qué puede fallar en las enfermedades pulmonares crónicas.
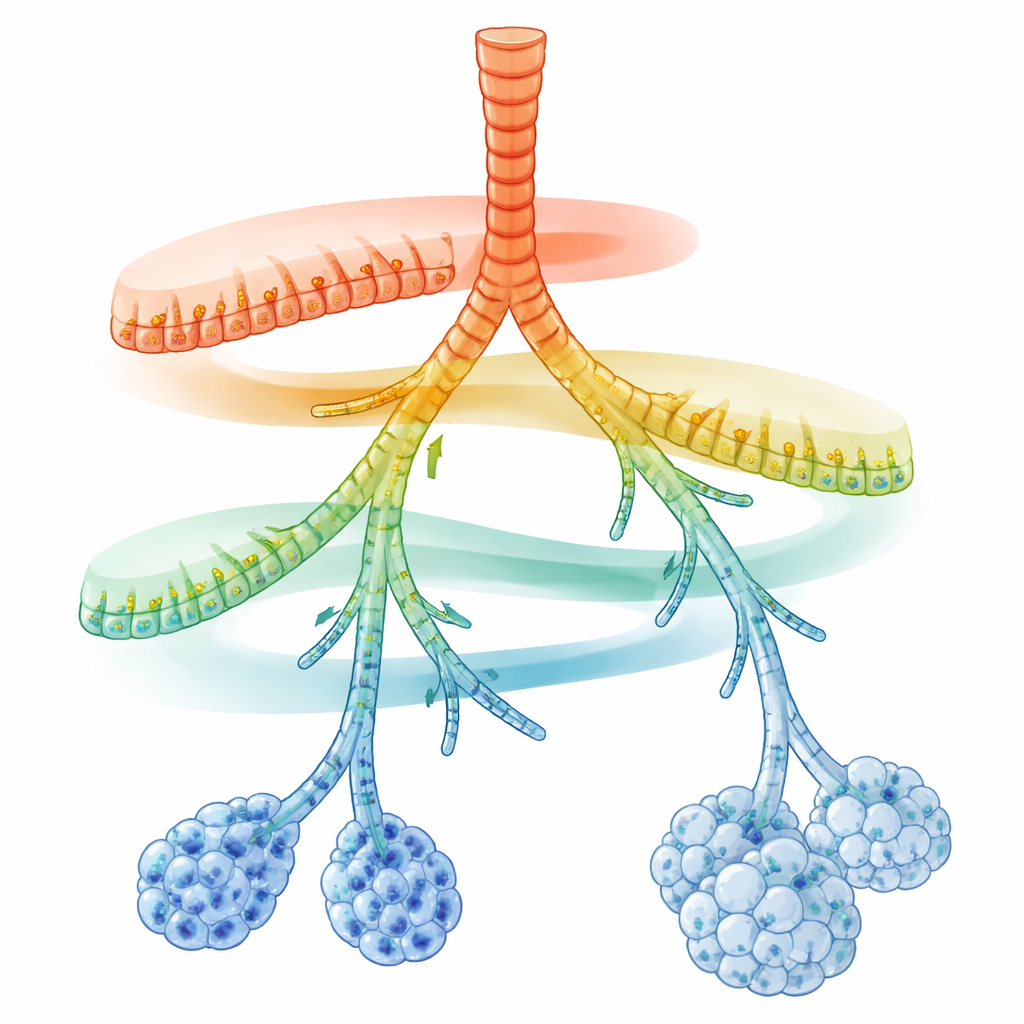
Un mapa oculto a lo largo de los tubos respiratorios
Los investigadores se centraron en las células secretoras, que recubren los conductos aéreos y secretan moco, péptidos antimicrobianos y surfactante. Mediante secuenciación de ARN unicelular, identificaron los genes activos en miles de células individuales de pulmones de ratón adulto. Al proyectar estas células en un mapa de similitud molecular, las células secretoras no se agruparon en pocos tipos rígidos. En lugar de ello, formaron una cadena continua de estados que conecta las vías aéreas grandes con los diminutos sacos alveolares. Sobre un programa central compartido para desintoxicar compuestos inhalados, surgieron dos gradientes opuestos de actividad génica: cerca de las vías aéreas más grandes, las genes implicados en la defensa innata rápida alcanzaban su máxima expresión; hacia las ramas más distales y los alvéolos, dominaban los genes relacionados con el manejo de lípidos, la producción de surfactante y la presentación de antígenos.
De un punto de partida a muchos estados celulares especializados
Para ver cómo emerge este patrón, el equipo marcó precursores secretores en la vida fetal tardía y siguió a sus descendientes durante la primera etapa de la vida usando trazado de linaje y análisis unicelular. Estas células marcadas formaron inicialmente una reserva inmadura con potente maquinaria de síntesis proteica y genes asociados a la construcción tisular. Tras el nacimiento, a medida que comenzaban la respiración y la exposición al exterior, estas células se diversificaron gradualmente en varios grupos maduros: células secretoras proximales ricas en genes de defensa innata, células más centrales con señales de desarrollo y regulación, células doble positivas que conectan identidades aéreas y alveolares, y células alveolares tipo 2 especializadas en surfactante. El programa de desintoxicación se activó pronto y de forma amplia, mientras que los programas de inmunidad innata y presentación de antígenos surgieron más tarde y en regiones concretas, lo que indica que las características de las células secretoras se adquieren en una secuencia temporal definida.
Cómo una señal de crecimiento moldea la identidad de la vía aérea distal
Una pista importante sobre lo que impulsa estos gradientes vino de un receptor llamado FGFR2b, parte de una vía de factores de crecimiento ya conocida por ser esencial para las células alveolares tipo 2. FGFR2b y sus genes diana estaban más activos en las células de las vías aéreas distales y en los alvéolos que en las proximales. Cuando los investigadores desactivaron FGFR2b específicamente en células secretoras justo después del nacimiento, el programa distal normal se debilitó. Los genes necesarios para la producción de surfactante y el tráfico vesicular disminuyeron, mientras que aumentaron genes típicos de las células alveolares tipo 1 aplanadas, componentes mitocondriales, canales iónicos y factores de supervivencia al estrés. Algunas células intermedias de la vía aérea comenzaron a coexpresar niveles moderados de marcadores proximales de defensa innata y marcadores distales, difuminando efectivamente el patrón espacial normal. En cultivos de organoides derivados de células de la vía aérea, añadir ligandos de FGFR suprimió los marcadores proximales de defensa innata y potenció genes relacionados con el surfactante de una forma coherente con los hallazgos in vivo, confirmando que activar FGFR2b es suficiente para empujar a las células hacia una identidad secretora distal.
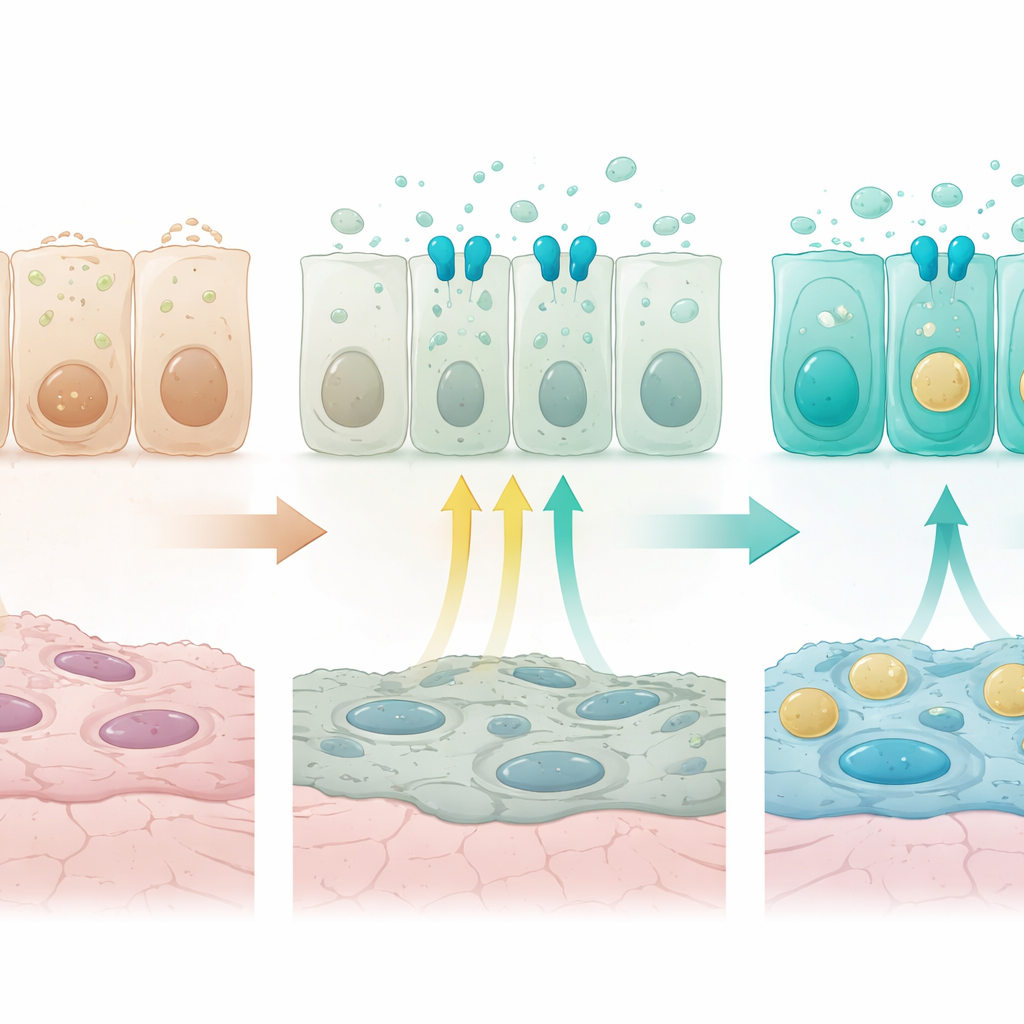
Ajuste fino mediante la interacción con otras señales
El equipo también investigó cómo la señalización FGFR2b interactúa con otra vía mediada por VEGFA, conocida principalmente por moldear los vasos sanguíneos. En organoides, VEGFA por sí sola pudo atenuar algunos genes de defensa innata, y bloquear su receptor alteró ciertos marcadores distales, pero no pudo sustituir completamente a FGFR2b. De hecho, la pérdida de FGFR2b in vivo redujo la expresión de Vegfa, y la estimulación combinada de ambas vías retroalimentó para disminuir los niveles de FGFR2b, lo que apunta a un cross-talk complejo entre estos sistemas de señalización. En ratones adultos, apagar FGFR2b ya no remodelaba de forma tan dramática los gradientes de inmunidad innata, pero seguía siendo necesario para mantener la expresión de marcadores distales clave, como el gen de surfactante Sftpb y el marcador clásico secretor de las vías aéreas Scgb1a1, y para conservar células híbridas vía aérea–alveolares.
Por qué estos gradientes importan para la salud pulmonar
La imagen que emerge es la del revestimiento de la vía aérea como un paisaje finamente graduado en lugar de un mosaico de zonas aisladas. Las regiones proximales están afinadas para una defensa rápida basada en mucosidad, mientras que las regiones distales combinan la producción de surfactante con una comunicación inmune más especializada. La señalización FGFR2b ayuda a establecer y sostener esta disposición, especialmente en los compartimentos distales, promoviendo programas relacionados con lípidos y vesículas y reprimiendo rasgos inapropiados de tipo proximal. Alterar estos gradientes, ya sea por genética, ambiente o enfermedad, podría desplazar el equilibrio entre defensa, desintoxicación y apoyo al intercambio gaseoso, contribuyendo a condiciones en las que las vías aéreas distales adquieren rasgos más proximales. Este marco ofrece una nueva manera de pensar sobre los trastornos pulmonares que “reconfiguran” el árbol de la vía aérea y puede orientar futuras estrategias para restaurar la organización celular adecuada.
Cita: Sountoulidis, A., Theelke, J., Liontos, A. et al. FGFR signaling establishes spatial gradients of secretory cell identities along the airway proximal-distal axis. Nat Commun 17, 2651 (2026). https://doi.org/10.1038/s41467-026-70842-0
Palabras clave: epitelio de la vía aérea, células secretoras, señalización FGFR2b, desarrollo pulmonar, gradientes espaciales