Clear Sky Science · es
Los aptámeros sintéticos mecanorreceptores permiten la detección de fuerzas específicas por célula y el control temporal mediante circuitos de ADN
Escuchar a las células mediante tirones suaves
Nuestros cuerpos están llenos de células que constantemente empujan y tiran de su entorno, usando diminutas fuerzas para decidir cuándo crecer, moverse o cambiar. Este estudio describe una nueva forma de escuchar esas fuerzas con dispositivos basados en ADN que pueden ajustarse a tipos celulares específicos y activarse o desactivarse a lo largo del tiempo. Esta tecnología podría, en el futuro, ayudar a los ingenieros a guiar el crecimiento de tejidos, comprender el comportamiento de tumores o diseñar materiales inteligentes que reaccionen a células vivas en tiempo real.
Usar el ADN como un pequeño interruptor mecánico
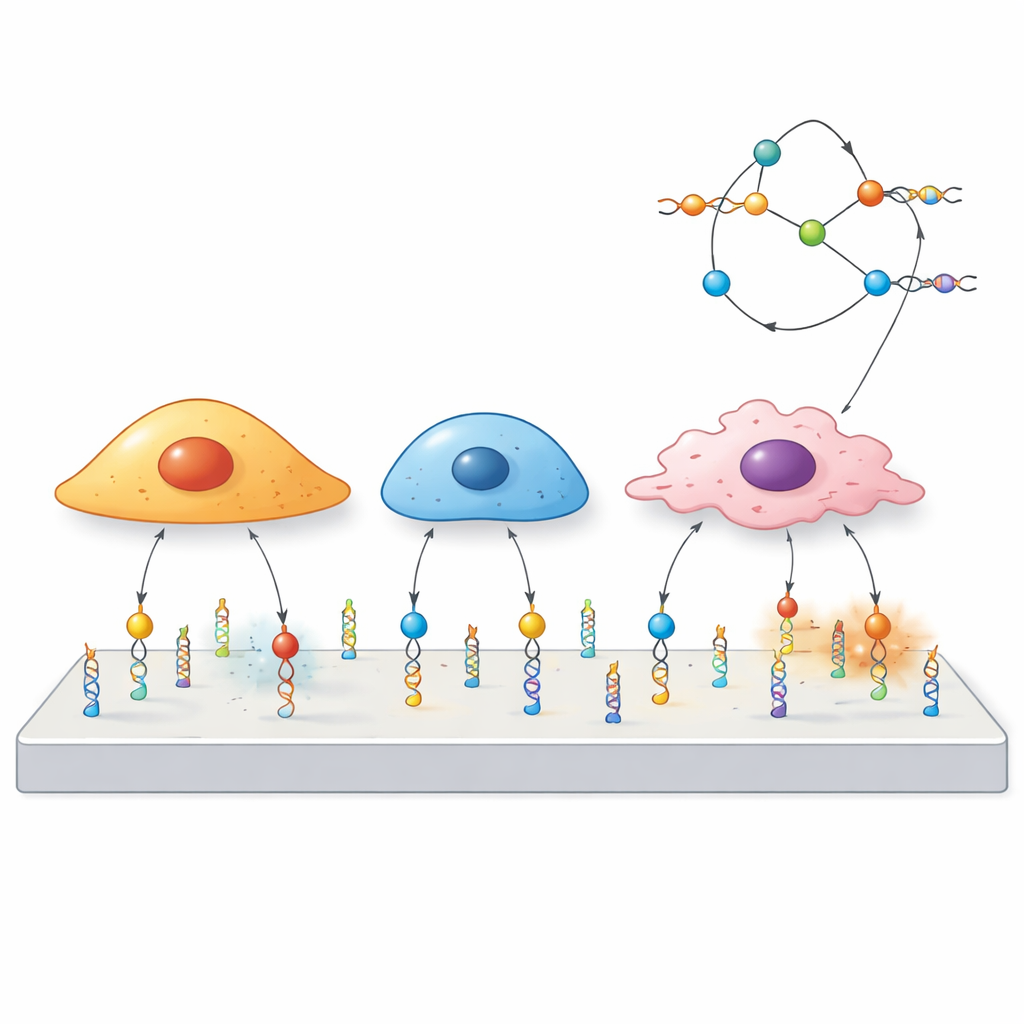
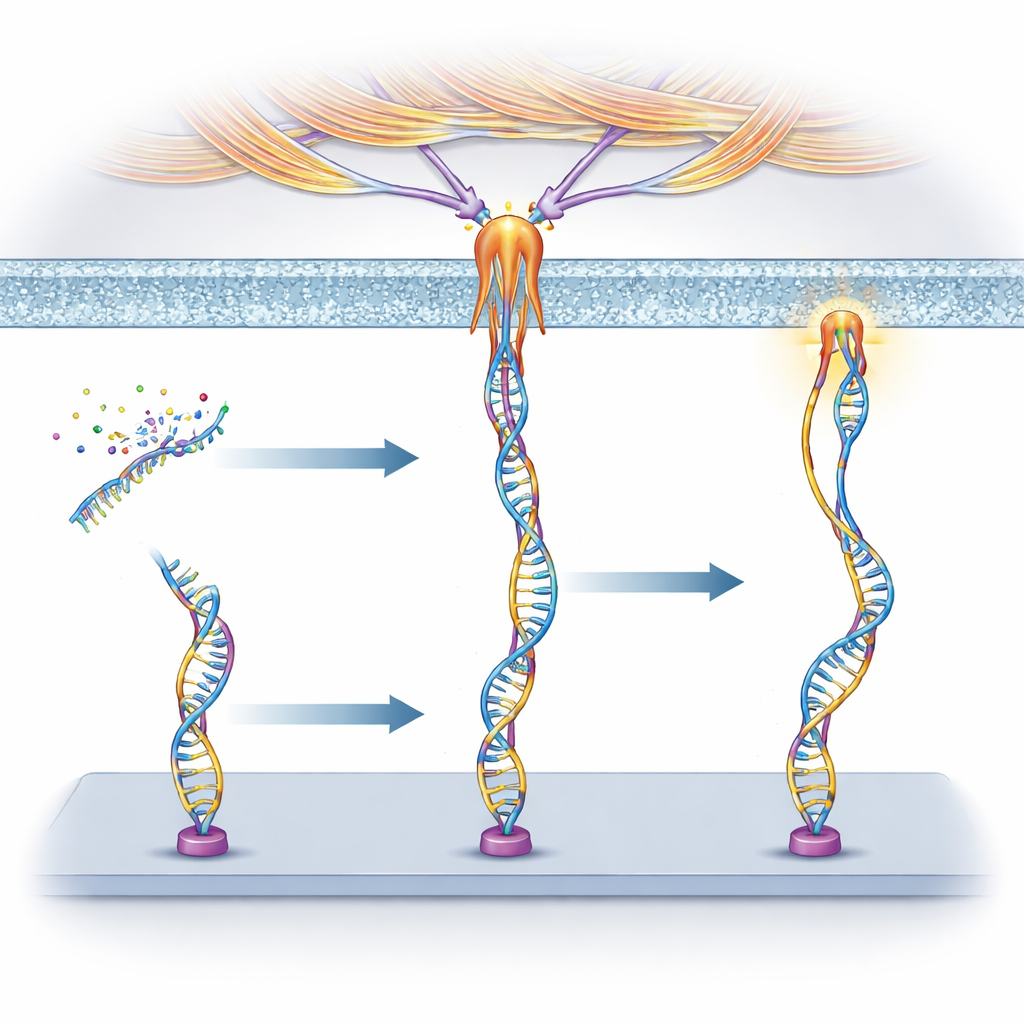
Los investigadores construyeron «mecano-sondas» a partir de ADN, la misma molécula que porta la información genética. Cada sonda tiene tres partes: una secuencia corta de ADN llamada aptámero que se adhiere a una proteína elegida en la superficie celular, un segmento pareado de ADN que actúa como un muelle afinado para romperse a una fuerza determinada, y una molécula fluorescente que se ilumina cuando ese muelle se rompe. Cuando una célula tira del receptor al que está unido el aptámero con suficiente fuerza, el dúplex de ADN se abre y la señal se enciende. Como diferentes aptámeros se fijan a distintos receptores, el equipo puede decidir de antemano qué células o proteínas podrán activar la sonda.
Encontrar vías de fuerza ocultas en las superficies celulares
La mayoría de los sensores de fuerza existentes se centran en las integrinas, proteínas bien conocidas que ayudan a las células a agarrarse al entorno pero que se encuentran en muchos tipos celulares, lo que limita la selectividad. Aquí, el equipo orientó en su lugar receptores «no canónicos» que normalmente no se consideran mecánicos. Mostraron que un aptámero llamado AS1411, que se une a una proteína llamada nucleolina común en células cancerosas, solo producía señal cuando podía reconocer específicamente su diana. Al diseñar sondas que requerían fuerzas más débiles o más fuertes para abrirse, descubrieron que la nucleolina transmite fuerzas moderadas en comparación con las integrinas y que por sí sola no ayuda a las células a extenderse sobre una superficie. En contraste, otro aptámero, Sgc8, que reconoce el receptor PTK7, podía informar de fuerzas incluso cuando las células apenas estaban adheridas, formando patrones en forma de anillo que sugerían una fuente de movimiento distinta.
Rastrear de dónde proceden las fuerzas
Para entender qué tiraba de estos dispositivos de ADN, los investigadores usaron fármacos que bloquean selectivamente distintos procesos celulares. Para la nucleolina, encontraron que sus fuerzas dependían en gran medida de la miosina, la misma proteína motora que ayuda a los músculos a contraerse, y aparecían en sitios donde la célula forma adhesiones focales—puntos de contacto especiales usados para agarrarse y detectar la rigidez. Esto sugiere que la nucleolina está vinculada de forma indirecta con la maquinaria interna de actina–miosina de la célula y puede compartir sus fuerzas contractiles. Para PTK7, sin embargo, bloquear un proceso llamado macropinocitosis—donde las células remueven la membrana y engullen fluido—redujo mucho las señales. Las fuerzas surgían principalmente de los primeros movimientos de ondulación de la membrana impulsados por el crecimiento de actina, no de pasos posteriores en el sellado de vesículas, revelando una vía mecánica distintiva.
Ajustar la selectividad celular con precisión molecular
Puesto que cada aptámero reconoce un receptor de superficie particular, el mismo andamiaje de ADN puede reprogramarse simplemente cambiando un aptámero por otro. El equipo demostró esto con sondas para tres dianas diferentes—PTK7, mucina-1 y EpCAM—a lo largo de un panel de líneas celulares cancerosas con niveles altos o bajos de cada proteína. Las células ricas en un determinado receptor producían señales fuertes, mientras que aquellas con poco receptor apenas respondían, incluso cuando se mezclaban en el mismo cultivo. De manera notable, células que compartían el mismo receptor aún podían mostrar diferentes patrones espaciales de fuerza, lo que subraya que el flujo de fuerza a través de un receptor depende no solo de su presencia sino también del cableado interno de cada tipo celular.
Programar cuándo se permite a las células tirar
Aprovechando que los aptámeros están hechos de ADN, los investigadores conectaron sus sondas a redes de reacción de ADN que controlan si el aptámero puede unirse o no. Hebras complementarias «bloqueadoras» pueden ocultar temporalmente el aptámero, y hebras «activadoras» pueden después eliminar los bloqueadores mediante una reacción de intercambio de hebras, restaurando la sensibilidad a la fuerza. También diseñaron un bloqueador basado en ARN que puede ser cortado por una enzima llamada RNasa H, y ralentizaron aún más este corte con moléculas señuelo que compiten por la enzima. De este modo, convirtieron la detección mecánica en un programa temporizado: las células solo podían generar señales tras un retraso incorporado o dentro de ventanas de tiempo elegidas.
Por qué esto importa para futuros materiales vivos
En términos cotidianos, este trabajo convierte al ADN en una cerradura mecánica inteligente que se abre solo para ciertas células, solo bajo ciertas fuerzas y solo en momentos prefijados. Al revelar que receptores menos evidentes como la nucleolina y PTK7 pueden portar información mecánica mediante rutas muy diferentes dentro de la célula, amplía nuestra visión de cómo las células «perciben» su entorno. Dado que todo el sistema está construido a partir de ácidos nucleicos, puede integrarse directamente en la caja de herramientas en rápido crecimiento de circuitos y nanodispositivos de ADN. Esto crea una base para materiales y tejidos diseñados que no solo detectan cuándo las células empujan o tiran, sino que también responden con acciones bioquímicas temporizadas, potencialmente orientando la curación, el crecimiento o el tratamiento del cáncer de manera altamente programable.
Cita: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Palabras clave: mecanotransducción, aptámeros de ADN, mecánica celular, biología sintética, redes de reacción de ADN