Clear Sky Science · es
Un actuador mioneural con biofísica diseñada para sistemas biohíbridos implantables
Reconstruir músculos como máquinas vivas inteligentes
Imagine que los médicos pudieran convertir el propio músculo de una persona en un motor vivo que no se cansa, que puede ser dirigido por un ordenador y que puede convivir de forma segura junto a órganos delicados durante años. Este estudio describe una forma de lograrlo. Los investigadores diseñan un “actuador mioneural” en ratas: un músculo cuyo cableado nervioso se reorganiza deliberadamente para que pueda ser controlado por electrónica, resista la fatiga y aun así se comporte como tejido natural. Tales actuadores vivos podrían, en el futuro, restaurar el movimiento, apoyar órganos en falla o proporcionar sensaciones realistas desde prótesis avanzadas.
Por qué los músculos vivos son mejores motores
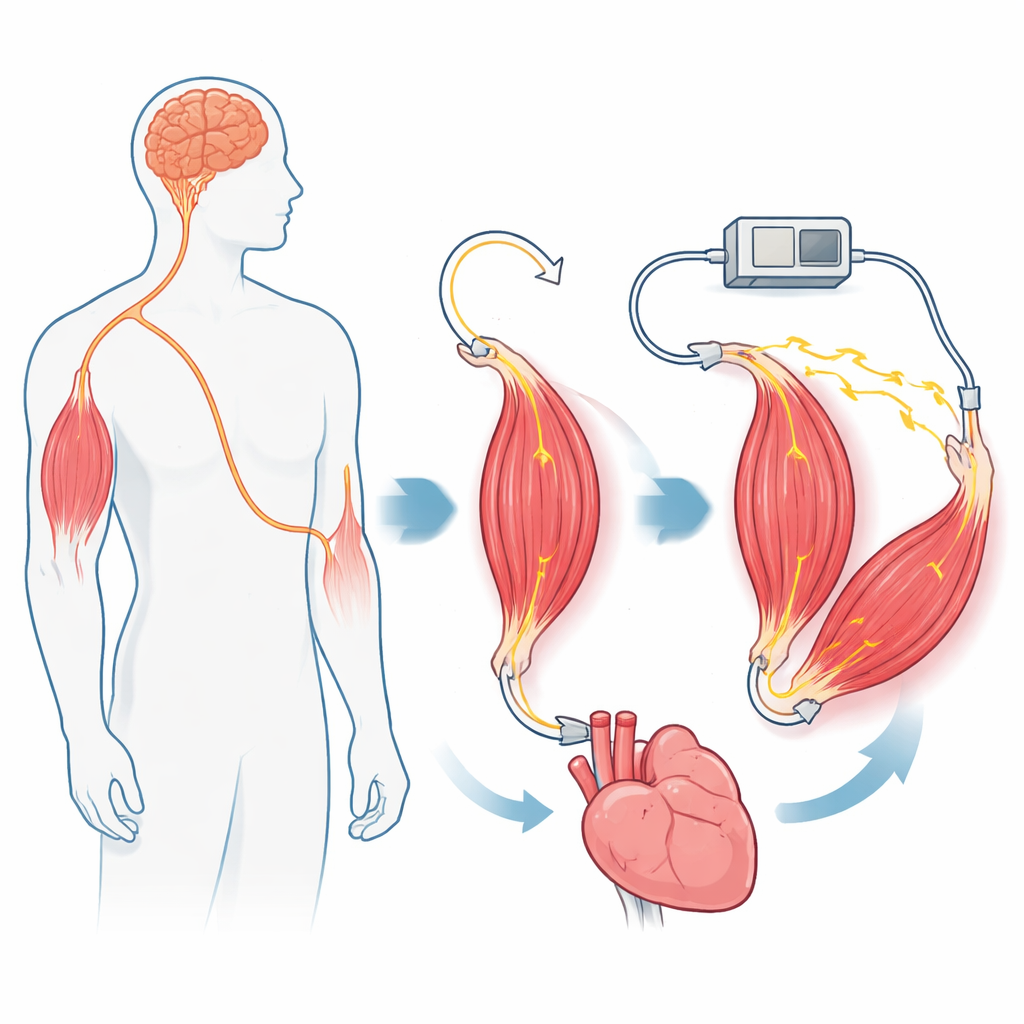
Los motores artificiales que funcionan con electricidad, aire o fluidos son potentes, pero son pesados, difíciles de reducir a tamaños compatibles con el cuerpo y están hechos de materiales que no se integran bien con el tejido vivo. En contraste, el músculo esquelético es ligero, eficiente energéticamente, capaz de autorrepararse y ya está diseñado para funcionar dentro del cuerpo. Puede crecer, adaptarse y responder a señales nerviosas muy pequeñas. Sin embargo, cuando los músculos se controlan directamente mediante pulsos eléctricos desde un dispositivo implantado, se fatigan rápidamente. Esta fatiga ocurre porque la estimulación eléctrica estándar tiende a reclutar en exceso primero las fibras más grandes y rápidas, pero menos duraderas. Para aprovechar el músculo como un motor implantable y fiable, el equipo necesitó cambiar cómo se organizan y reclutan sus fibras nerviosas—sin renunciar a la salud y sostenibilidad naturales del músculo.
Cambiar vías nerviosas para reescribir el control
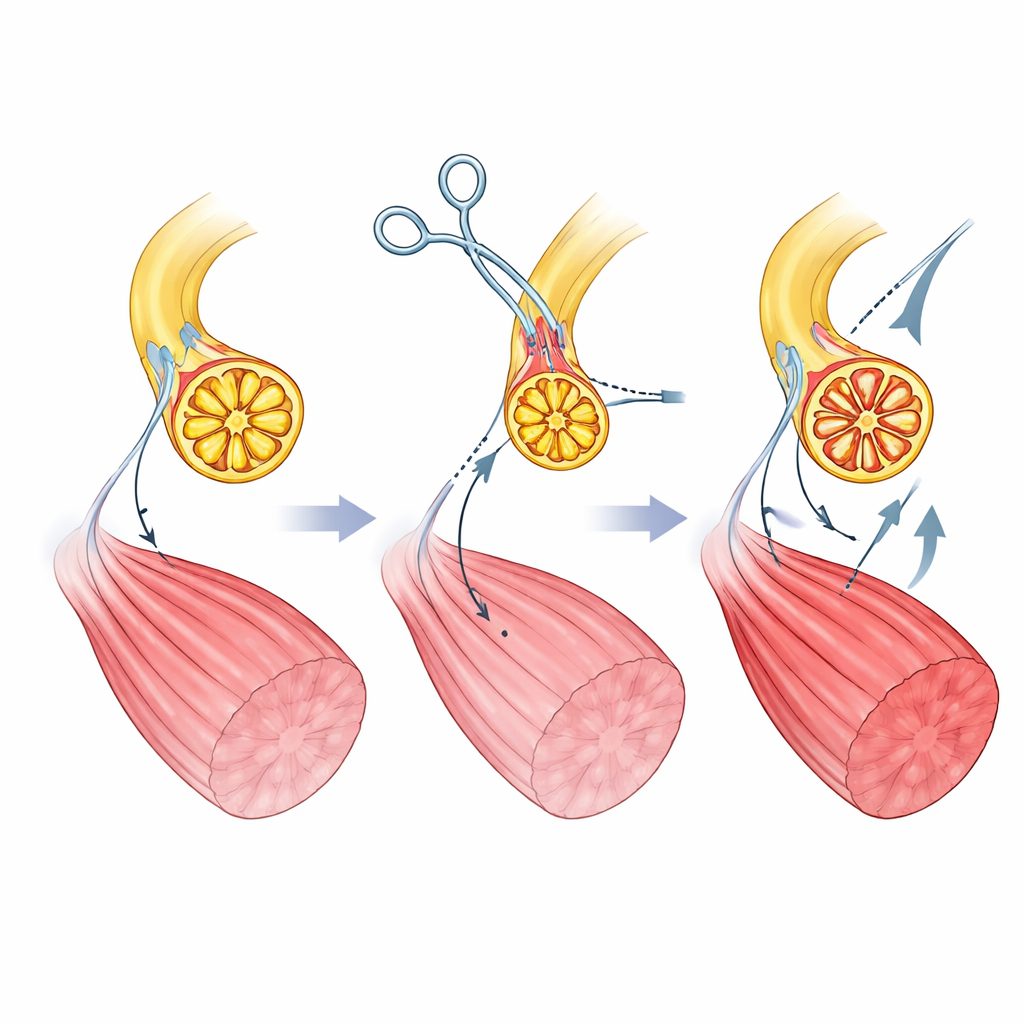
Los autores crean su actuador mioneural en ratas mediante la reconfiguración quirúrgica de un músculo de la pata. Primero cortan el nervio motor normal que transmite las órdenes desde la médula espinal y evitan que vuelva a crecer. Luego redirigen un nervio distinto—uno que normalmente transmite señales de tacto y estiramiento desde la piel y los tejidos—directamente hacia el músculo. Con el tiempo, este nervio “sensitivo” regenera su crecimiento dentro del músculo y forma nuevos puntos de contacto con las fibras musculares. La microscopía muestra que estas nuevas uniones se parecen y funcionan como las conexiones motoras normales, y el músculo recupera la capacidad de contraerse cuando se estimula eléctricamente el nervio sensitivo. Es importante que los axones en este nervio sensitivo sean más uniformes y de menor tamaño que los del nervio motor original, lo que prepara el terreno para un reclutamiento de fibras musculares más equilibrado bajo control informático.
Músculos que siguen funcionando bajo esfuerzo
Una vez que los músculos reconectados habían sanado, el equipo los sometió a rutinas de prueba exigentes. Compararon músculos nativos con los nuevos actuadores durante contracciones repetidas simples y durante largos periodos de contracción continua. Los actuadores mioneurales perdieron fuerza mucho más lentamente y mostraron una salida más estable con el tiempo, con una mejora del 260 por ciento en la resistencia a la fatiga bajo trabajo continuo. Su comportamiento durante minutos fue fundamentalmente distinto al del músculo no modificado: en lugar de una caída rápida de fuerza, la fuerza disminuía de forma más gradual y luego se estabilizaba. A pesar de perder algo de masa durante el proceso de reconexión, los actuadores conservaron una estructura de fibras sana y produjeron una fuerza por unidad de masa similar a la del músculo nativo, además de mantener su condición durante al menos 15 semanas incluso sin ejercicio ni estimulación adicional.
Control por ordenador sin perturbar el cerebro
Debido a que el nuevo cableado nervioso desconecta el músculo de las señales motoras normales del cerebro, todas las contracciones proceden ahora de un estimulador externo. Los investigadores integran el músculo en un bucle de retroalimentación: un sensor mide la fuerza, un controlador ajusta la estimulación del nervio y el sistema sigue un objetivo de fuerza elegido a lo largo de muchos ciclos. Los músculos nativos fallan rápidamente en este montaje, pero los actuadores mioneurales continúan siguiendo las señales de comando. Para hacer el sistema más seguro y flexible, el equipo también introduce un “bloqueo nervioso” reversible. Aplicando una señal eléctrica de alta frecuencia en el nervio más próxima a la médula espinal, evitan que los pulsos de estimulación envíen señales indeseadas de vuelta al sistema nervioso central mientras permiten que el lado muscular responda. En las pruebas, el actuador siguió generando fuerzas controladas mientras el cerebro permanecía efectivamente aislado de la estimulación artificial.
De extremidades biónicas a ayudar órganos en fallo
Para mostrar cómo podría usarse este motor vivo, los autores construyen dos sistemas de demostración en ratas. En el primero, acoplan el actuador en serie con otro músculo que representa el músculo residual en el sitio de una amputación. Al apretar o relajar este par, cambian el estiramiento del músculo residual y, a su vez, la actividad de sus fibras nerviosas sensoriales—esencialmente modulando el sentido de posición y fuerza de la extremidad. Esta “interfaz mecanoneural propioceptiva” podría proporcionar eventualmente retroalimentación con sensación natural desde extremidades robóticas o avatares virtuales. En el segundo sistema, envuelven el actuador alrededor de un segmento de intestino delgado lleno de líquido. Cuando se activa mediante estimulación nerviosa, el músculo aprieta y suelta el segmento intestinal, y el seguimiento del movimiento muestra que el órgano se mueve al compás del actuador. Esto apunta a dispositivos futuros que podrían aportar fuerza mecánica a órganos debilitados como el intestino, la vejiga o incluso el corazón.
Qué podría significar esto para la medicina futura
En conjunto, este trabajo muestra que, mediante una reruta cuidadosa de los nervios, el propio músculo de una persona puede convertirse en un actuador resistente a la fatiga, controlado por ordenador, que aún se comporta como tejido nativo y puede aislarse eléctricamente del cerebro cuando sea necesario. Dado que el enfoque se basa en técnicas quirúrgicas y electrodos que ya se asemejan a herramientas clínicas existentes, podría ser más fácil de trasladar a la práctica clínica que implantes totalmente sintéticos o tejidos cultivados en laboratorio. Si se pueden construir y controlar de forma segura actuadores mioneurales similares en humanos, podrían formar el núcleo de nuevos sistemas biohíbridos que restauren la sensación de las extremidades, asistan órganos en fallo y proporcionen señales mecánicas precisas al cuerpo sin la masa y rigidez de las máquinas tradicionales.
Cita: Song, H., Herrera-Arcos, G., Friedman, G.N. et al. A myoneural actuator with engineered biophysics for implantable biohybrid systems. Nat Commun 17, 2584 (2026). https://doi.org/10.1038/s41467-026-70626-6
Palabras clave: actuador biohíbrido, neuroprótesis, fatiga muscular, regeneración nerviosa, soporte de órganos