Clear Sky Science · es
StrucGAP: una plataforma modular, optimizada y trazable de minería de datos para glicoproteómica estructural y sitio-específica
Comprendiendo los recubrimientos azucarados de las proteínas
Cada célula de nuestro cuerpo está cubierta por un bosque de estructuras azucaradas unidas a proteínas. Estos “recubrimientos azucarados”, conocidos como glicanos, ayudan silenciosamente a regular cómo las células se adhieren, se comunican y responden a su entorno. Los instrumentos modernos pueden catalogar estos patrones de azúcares con un detalle asombroso, pero los investigadores suelen verse desbordados por el volumen y la complejidad de los datos. Este estudio presenta StrucGAP, una nueva plataforma computacional diseñada para convertir esas mediciones densas en relatos claros y biológicamente significativos, usando el envejecimiento del útero de ratón como caso de prueba.
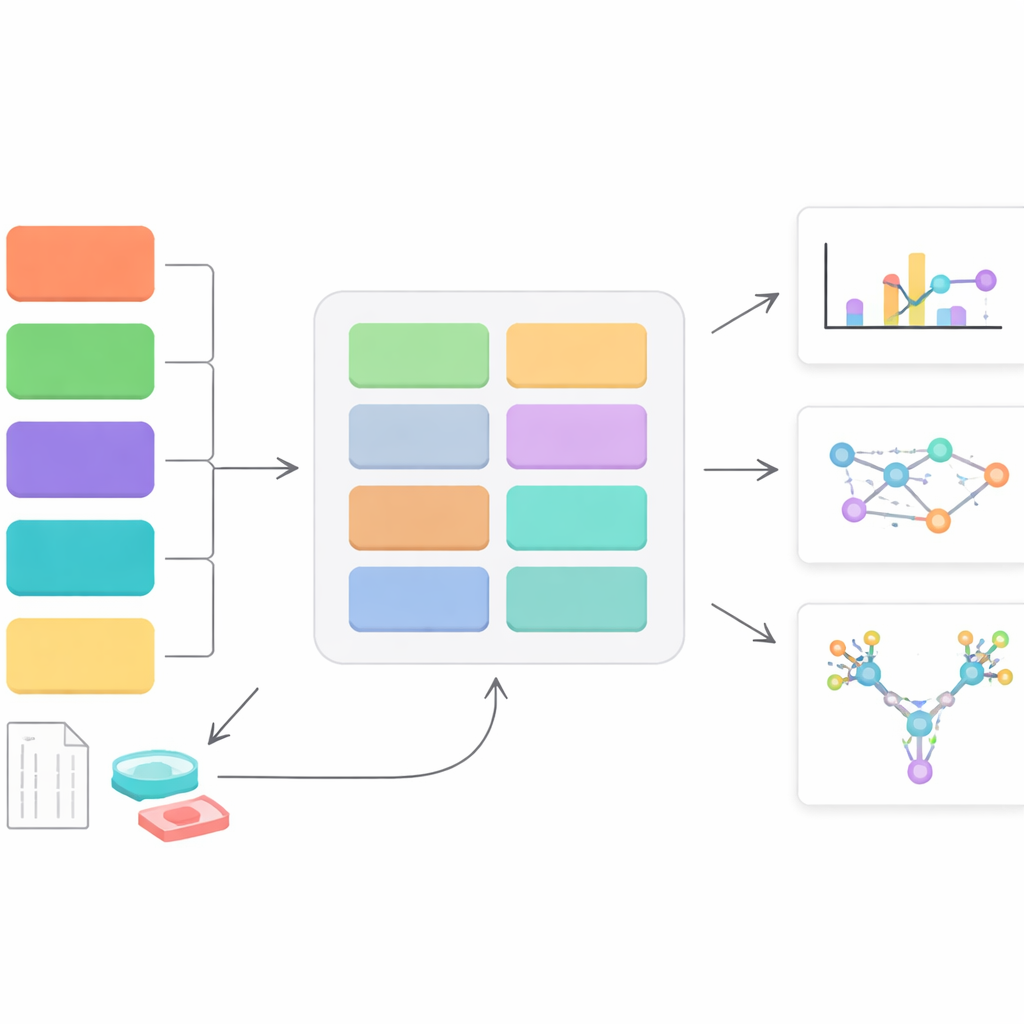
Un nuevo centro de control para datos de recubrimientos azucarados
StrucGAP es una plataforma de software construida para analizar un tipo específico de decoración azucarada: los glicanos N-enlazados, que se adhieren a sitios concretos en las proteínas. En lugar de intentar ser una herramienta de uso general, StrucGAP está diseñada desde cero para este problema. Acepta resultados de varios “motores de búsqueda” de espectrometría de masas populares que identifican qué glicanos están en qué sitios proteicos. Una vez realizadas esas identificaciones, StrucGAP las procesa mediante una serie de módulos que verifican la calidad de los datos, resumen los patrones generales de glicanos, siguen cómo cambian sitios específicos entre condiciones y vinculan esos cambios con funciones biológicas y vías conocidas.
Descomponer azúcares complejos en partes significativas
La mayoría de las herramientas existentes tratan cada glicano como un objeto único e indivisible. StrucGAP adopta un enfoque diferente: descompone cada glicano en bloques de construcción más pequeños y biológicamente significativos, como núcleos comunes, patrones de ramificación y motivos bien conocidos que incluyen fucosa o ácido siálico. Luego no solo pregunta qué glicanos enteros aumentan o disminuyen, sino qué motivos aparecen con mayor o menor frecuencia, o en nuevas combinaciones. Esta visión de “subestructura” hace que el análisis sea más robusto frente a asignaciones inciertas y ayuda a descubrir patrones que de otro modo podrían quedar ocultos, especialmente cuando motivos raros pero importantes se enriquecen en una condición específica.
Siguiendo los cambios azucarados durante el envejecimiento uterino
Para mostrar lo que StrucGAP puede hacer, los autores lo aplicaron a un conjunto de datos detallado del tejido uterino de ratones hembras jóvenes y de mediana edad. El experimento bruto identificó más de veinte mil glicopéptidos únicos, cada uno representando un sitio proteico particular con un glicano específico. StrucGAP primero limpió y estandarizó los datos, y luego trazó cómo se distribuían los glicanos entre los sitios proteicos y cuántas variaciones estructurales aparecían en cada posición. El útero resultó ser rico tanto en glicanos simples de tipo high-mannose como en tipos más elaborados y complejos, con muchas composiciones de glicanos existiendo como múltiples isómeros estructurales. Al acercarse a las subestructuras, la plataforma catalogó con qué frecuencia ocurrían y coocurrían distintos núcleos, recuentos de ramas y motivos como los epítopos Lewis o formas concretas de ácido siálico.
De patrones a función: adhesión y remodelado
El módulo cuantitativo de StrucGAP comparó entonces úteros jóvenes y envejecidos, encontrando más de mil glicopéptidos que aumentaron y unos pocos cientos que disminuyeron con la edad. Un tema recurrente fue la “fucosilación core” —una forma específica en que una fucosa se une al núcleo del glicano—, que mostró cambios en ambas direcciones, lo que sugiere una regulación finamente ajustada en lugar de un interruptor simple de encendido/apagado. Surgieron otros patrones al endurecer los umbrales estadísticos: glicanos con más ramas, motivos específicos tipo Lewis y ácidos siálicos que contienen Neu5Ac se enriquecieron progresivamente. Al vincular estas características estructurales con bases de datos de funciones génicas y vías, StrucGAP reveló que los glicanos cambiantes se concentraban en proteínas implicadas en la adhesión celular, las interacciones con la matriz circundante y el remodelado de la arquitectura tisular. La plataforma también conectó estos patrones con cambios en las enzimas que construyen y recortan glicanos, así como con proteínas que se unen a glicanos, esbozando redes coordinadas que podrían impulsar el envejecimiento uterino.
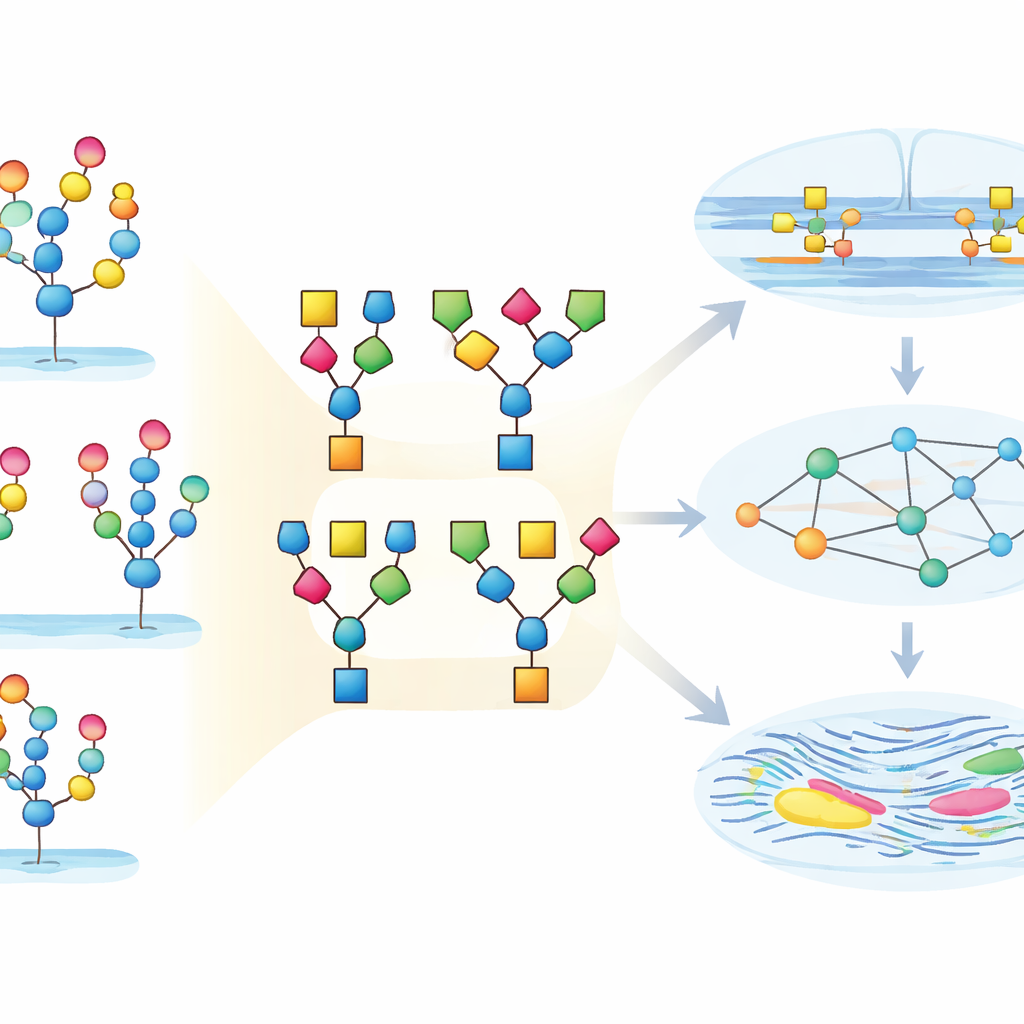
Convertir la avalancha de datos en conocimiento biológico
En términos cotidianos, este trabajo muestra cómo una masa altamente técnica de mediciones de “azúcar-sobre-proteína” puede convertirse en un mapa legible de cómo cambian los tejidos con el tiempo. StrucGAP actúa tanto como guardián de la calidad como motor narrativo: limpia los datos, resume los motivos azucarados clave, los vincula con las enzimas que los modelan y con las vías que influyen, y genera automáticamente gráficos e informes que destacan los hallazgos más importantes. En el útero de ratón, esto revela un cambio coordinado hacia glicanos más densamente decorados, ricos en Neu5Ac y fucosa, vinculados a la adhesión y al remodelado tisular. En términos más generales, StrucGAP ofrece a los investigadores una forma práctica de pasar de datos brutos de glicoproteómica a ideas comprobables sobre cómo los recubrimientos azucarados ayudan a controlar la salud, la enfermedad y el envejecimiento.
Cita: Yang, M., Wu, Y., Zhang, Z. et al. StrucGAP: a modular, streamlined and traceable data mining platform for structural and site-specific glycoproteomics. Nat Commun 17, 2579 (2026). https://doi.org/10.1038/s41467-026-70560-7
Palabras clave: glicoproteómica, N-glicosilación, plataforma bioinformática, envejecimiento uterino, glicosilación de proteínas