Clear Sky Science · es
Transiciones estructurales en el ensamblaje escalonado de las partículas centrales del proteasoma
Cómo las células eliminan la basura molecular
Dentro de cada una de nuestras células, las proteínas gastadas y dañadas deben descomponerse antes de acumularse como basura. Una enorme máquina molecular llamada proteasoma realiza gran parte de esta limpieza y ya es diana de fármacos anticancerígenos. Este estudio asoma detrás de las escenas para ver cómo se construye paso a paso el núcleo catalítico del proteasoma en levadura, revelando atajos inesperados y mecanismos de seguridad que ayudan a garantizar que la máquina final funcione con precisión y solo cuando esté lista.
Construir un barril triturador de proteínas
La parte activa del proteasoma es un núcleo en forma de barril formado por anillos apilados de subunidades proteicas. Este barril alberga los sitios de corte ocultos que desmenuzan otras proteínas en fragmentos pequeños. Como activar estos cortadores demasiado pronto sería peligroso, las células ensamblan el barril mediante una serie de intermedios parcialmente formados. Los autores se centraron en versiones tempranas del núcleo, conocidas como complejos precursores, que suelen ser raros y efímeros. Al ralentizar ligeramente uno de los últimos pasos del ensamblaje, pudieron capturar y purificar estas formas tempranas de levadura y obtener imágenes mediante crio–microscopía electrónica de alta resolución, que congela las moléculas en acción y revela sus formas tridimensionales.
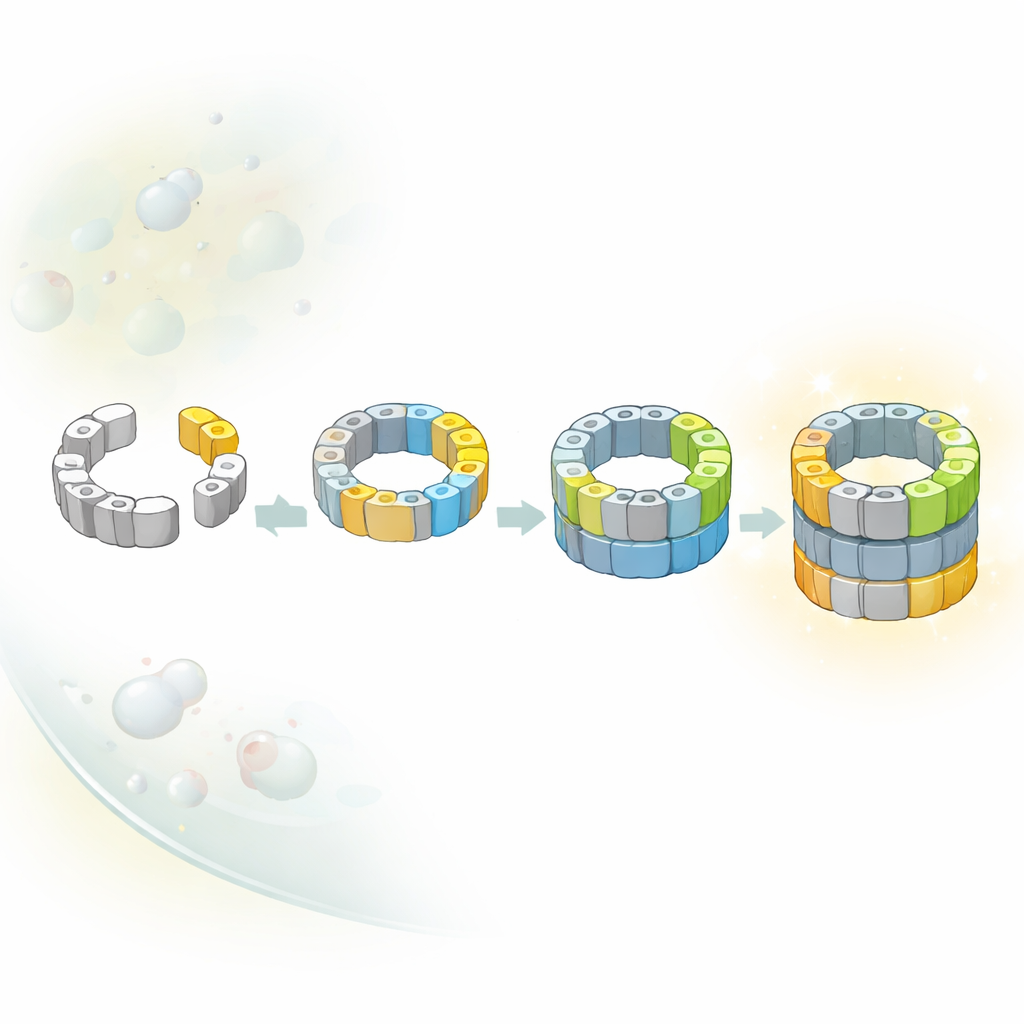
Múltiples caminos hacia el mismo núcleo
Los diagramas clásicos de libro de texto suelen sugerir que las máquinas complejas dentro de las células se construyen siguiendo una única ruta fija. Aquí, los investigadores descubrieron que no es así para el núcleo del proteasoma. Identificaron varios intermedios distintos que difieren en qué subunidades catalíticas se han unido al barril a medio hacer. Combinando instantáneas estructurales con trucos genéticos que encienden y apagan subunidades individuales, mostraron que al menos dos caminos alternativos conducen de un semibarril temprano a uno casi completo. En una ruta, una subunidad en particular llamada β5 llega primero; en otra, una subunidad diferente, β1, puede unirse antes. El equilibrio entre estas vías probablemente depende de qué bloques de construcción estén más disponibles en el entorno celular, que es muy concurrido.
De piezas sueltas a una cámara de corte bloqueada
Las estructuras también revelan cómo los sitios de corte del proteasoma se preparan cuidadosamente a medida que avanza el ensamblaje. En intermedios tempranos, las regiones de asas clave que rodean los residuos de corte enterrados son flexibles y están poco ordenadas, y los centros catalíticos siguen bloqueados por segmentos cortos llamados «propéptidos». A medida que más subunidades encajan alrededor del anillo, esas asas adoptan gradualmente formas más definidas que alinean aminoácidos cruciales necesarios para la autoactivación. Solo cuando dos semibarriles finalmente se juntan, completando el barril de doble anillo, estas asas se bloquean por completo en su disposición activa y se desencadena la eliminación de los segmentos bloqueantes. Esta acoplación entre geometría y química ayuda a garantizar que la potente actividad de corte aparezca únicamente dentro de una cámara sellada, protegiendo al resto de la célula.
Las chaperonas guían y luego se separan
En el proceso, proteínas auxiliares especializadas llamadas chaperonas escoltan el barril en ensamblaje e impiden combinaciones incorrectas. Una chaperona, Ump1, comienza mayormente desestructurada pero se pliega progresivamente a medida que más subunidades la rodean, quedando finalmente atrapada en la cavidad central y luego degradada una vez que el barril está activo. Otro par de chaperonas, Pba1–Pba2, sujeta la superficie del anillo exterior de dos maneras ingeniosas. Un lazo flexible de Pba1 se encaja entre dos subunidades del anillo exterior como un espaciador, manteniéndolas ligeramente separadas e impidiendo el cierre prematuro. Al mismo tiempo, el extremo terminal de una subunidad del anillo exterior (α1) ayuda a posicionar segmentos vecinos de modo que, en la etapa final, las chaperonas puedan liberarse y el anillo cerrarse correctamente. Cuando los investigadores eliminaron la cola de α1, el barril se estancó en un estado tardío y casi terminado que retenía obstinadamente sus chaperonas, confirmando que esta pequeña región actúa como parte de un interruptor de liberación.
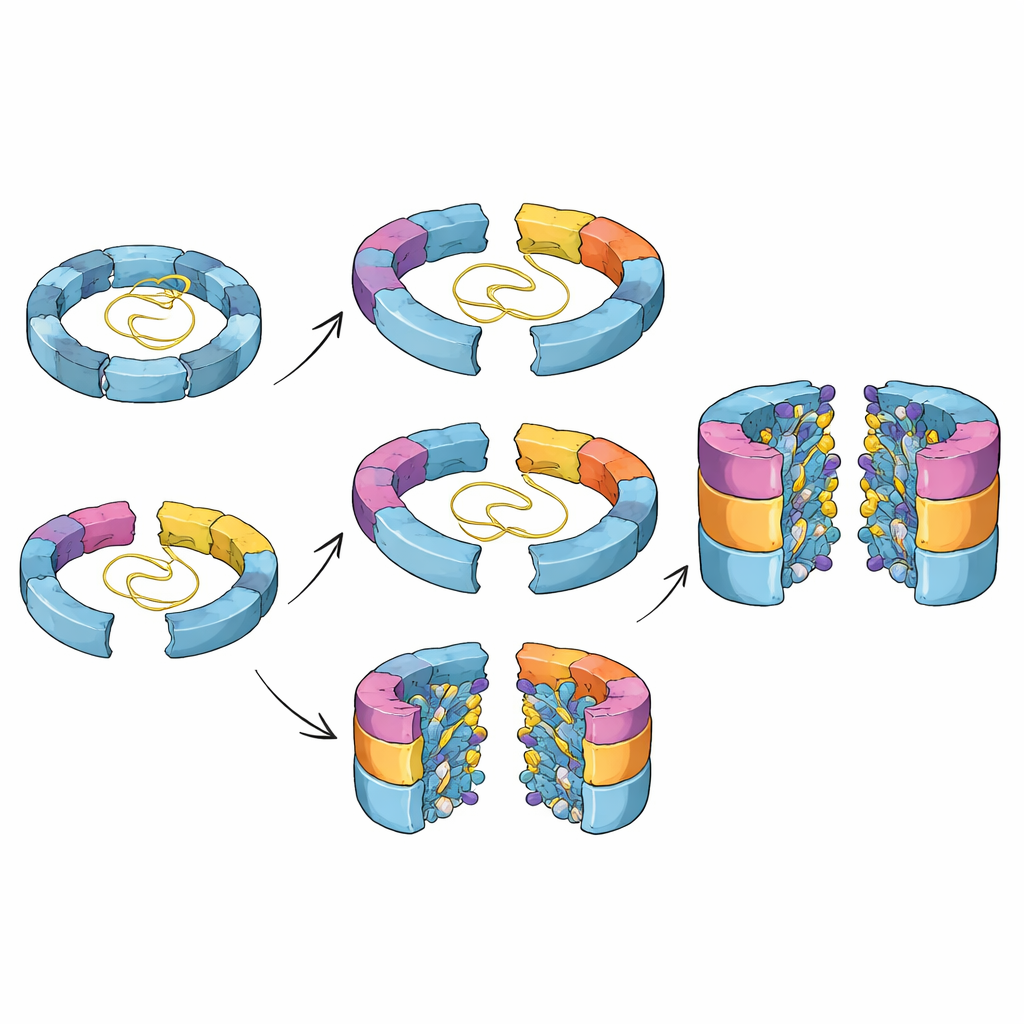
Por qué importan estos pasos ocultos
En conjunto, estos hallazgos dibujan un panorama detallado de cómo las células coreografían el ensamblaje de un triturador de proteínas peligroso pero esencial. El trabajo muestra que el núcleo del proteasoma puede construirse por más de una vía, que sus sitios activos se esculpen gradualmente en su lugar y que las proteínas auxiliares no solo estabilizan intermedios tempranos sino que también están integradas en un circuito temporal que asegura que se marchen en el momento justo. Comprender estos pasos ocultos ayuda a explicar cómo pequeños cambios genéticos en factores de ensamblaje pueden contribuir a enfermedades y puede facilitar el diseño de fármacos que ajusten finamente la actividad del proteasoma en cáncer, trastornos inmunitarios o neurodegenerativos al apuntar a su construcción en lugar de a su forma final.
Cita: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
Palabras clave: ensamblaje del proteasoma, degradación de proteínas, chaperonas moleculares, crio-microscopía electrónica, control de calidad celular