Clear Sky Science · es
Quimerismo molecular transitorio para explotar organelos xenogénicos
Paneles solares prestados en una sola célula
Solemos pensar en la vida impulsada por la energía solar en términos de plantas y algas, pero algunos depredadores unicelulares toman un atajo: roban los “paneles solares” —los cloroplastos— de sus presas. Este estudio explora cómo un microbio de ese tipo, Rapaza viridis, mantiene estas piezas robadas funcionando durante semanas, aunque proceden de una especie completamente distinta. Al desvelar cómo las proteínas del propio hospedador se filtran y sostienen estos cloroplastos foráneos, el trabajo arroja luz sobre cómo partes celulares complejas como los cloroplastos pudieron haberse originado hace mucho tiempo.
Cómo un microbio roba y usa energía verde
Rapaza viridis es un diminuto flagelado que se alimenta de una alga verde específica llamada Tetraselmis. En lugar de digerirlo todo, Rapaza conserva los cloroplastos capturados, ahora llamados “kleptoplastos”, y desecha el resto de la célula algal, incluido su núcleo. Estos kleptoplastos se trocean y se pasan a las células hijas de Rapaza. Durante unas dos semanas, el hospedador puede vivir casi por completo con la energía y el carbono producidos por estos cloroplastos prestados, pese a que ya no reciben instrucciones ni piezas de reemplazo del genoma algal original. Este modo de vida inusual ofrece una ventana en vivo sobre cómo pudieron ser los primeros pasos hacia cloroplastos permanentes.
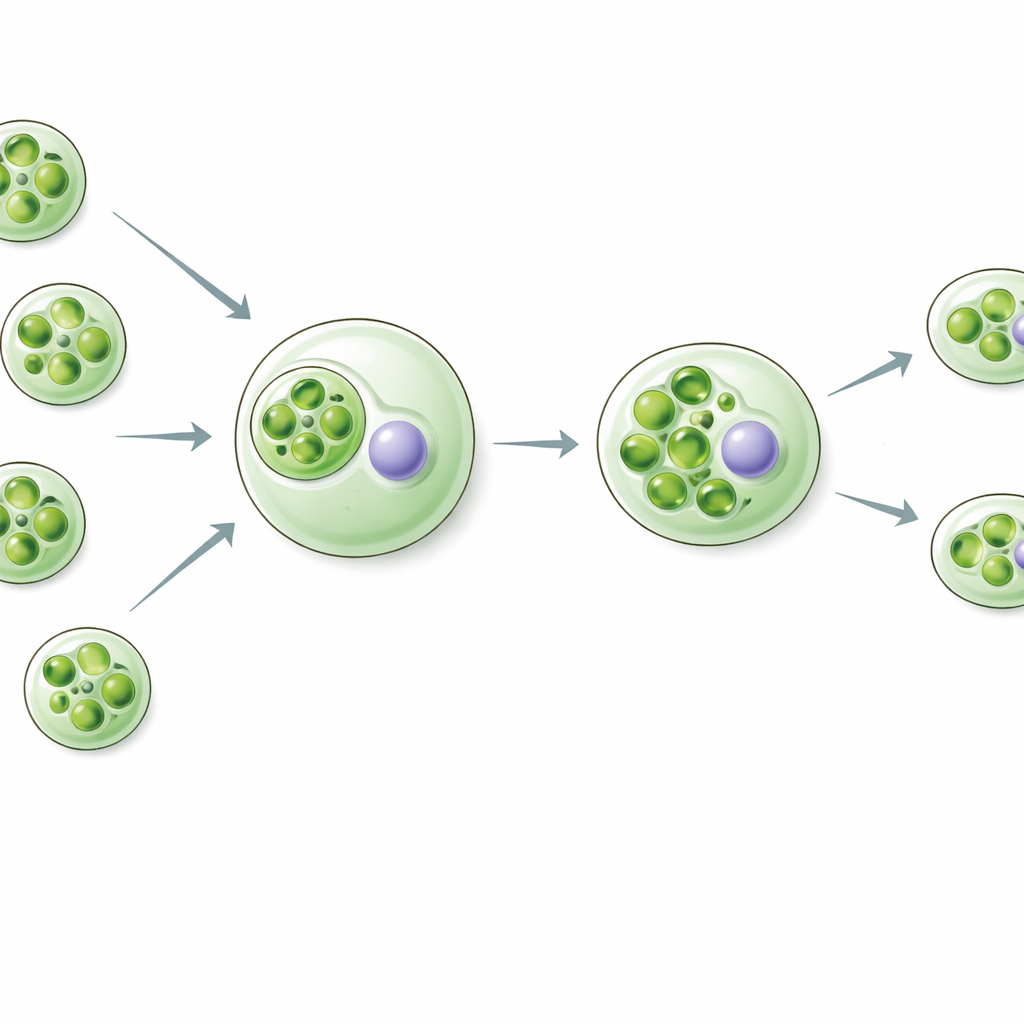
Los genes del hospedador intervienen para mantener vivas las piezas robadas
Los investigadores se plantearon una pregunta crucial: si el núcleo algal ha desaparecido, ¿quién suministra las proteínas necesarias para mantener el kleptoplasto en funcionamiento? Analizando la actividad génica a lo largo del tiempo en Rapaza, identificaron 37 genes del hospedador cuyos productos parecen actuar dentro de los cloroplastos. Muchos de estos genes se asemejan a componentes de la maquinaria fotosintética: proteínas captadoras de luz, elementos del transporte electrónico y enzimas que fijan carbono. Dos destacaron: una proteína similar a la subunidad pequeña de RuBisCO (RvRbcS-like) y una proteína similar a la activasa de RuBisCO (RvRca-like). Ambas están relacionadas con ayudantes clave de la RuBisCO, la enzima central que captura dióxido de carbono. Estos genes del hospedador se activan con fuerza después de que se ingiere la presa, justo cuando los kleptoplastos se remodelan y preparan para un uso a largo plazo.
Demostrando que las proteínas del hospedador entran en los kleptoplastos
Encontrar secuencias génicas sugerentes no basta; las proteínas deben llegar realmente al interior de los kleptoplastos. Con anticuerpos personalizados y microscopía de fluorescencia, el equipo siguió dónde se acumulan las proteínas RvRbcS-like y RvRca-like. Modificaron cepas de Rapaza con pequeñas etiquetas detectables en RvRbcS-like y mostraron que la señal se solapaba con los kleptoplastos y con la propia RuBisCO. Imágenes similares con un anticuerpo contra RvRca-like revelaron que esta proteína también se concentra dentro de los kleptoplastos. En geles proteicos, ambas proteínas aparecieron acortadas, consistente con la eliminación de un segmento frontal especial al cruzar membranas —tal como ocurre con las señales de destino que guían proteínas hacia los cloroplastos ordinarios.
Por qué importan estos ayudantes prestados
Para comprobar si estas proteínas del hospedador son verdaderamente importantes, los autores utilizaron edición génica basada en CRISPR para eliminar cada gen. Las células carentes de RvRbcS-like crecieron mal, perdieron fuerza fotosintética, produjeron muchas menos gránulos de almacenamiento ricos en energía y murieron mucho antes de lo normal. Los niveles de la subunidad grande de RuBisCO de la alga también disminuyeron, lo que sugiere que sin la subunidad pequeña sustituta del hospedador, el complejo enzimático se desarma. Eliminar RvRca-like tuvo un efecto más suave pero claro: el crecimiento temprano se mantuvo cercano a la normalidad, pero más adelante la fotosíntesis y el almacenamiento de carbono se redujeron, revelando una pérdida gradual de eficiencia. En conjunto, estos resultados muestran que Rapaza no se limita a aparcar cloroplastos robados; los mantiene y remodela activamente con su propio conjunto de proteínas.
Etiquetas de entrega personalizadas y estructuras internas reconstruidas
La mayoría de las proteínas putativamente dirigidas a kleptoplastos en Rapaza comparten largas “cabezas” de baja estructura en su extremo frontal, a menudo con segmentos predichos que atraviesan membranas. Al fusionar una de estas cabezas con una proteína reportera luciferasa, los autores mostraron que este segmento por sí solo basta para transportar una proteína cargo a los kleptoplastos. Un análisis detallado de secuencias reveló varias clases de estas regiones de direccionamiento, que se parecen estrechamente a las utilizadas por un grupo relacionado de algas para importar proteínas a sus cloroplastos permanentes de triple membrana. Una proteína del hospedador especialmente llamativa, RvRbcS-like, contiene cuatro dominios relacionados con RuBisCO y una cola flexible rica en motivos repetidos que se cree promueven la separación de fases de proteínas. Los autores proponen que esta cola ayuda a reorganizar el pirenoide —el denso núcleo fijador de carbono dentro del kleptoplasto— en múltiples gotas que puedan heredarse por las células hijas.
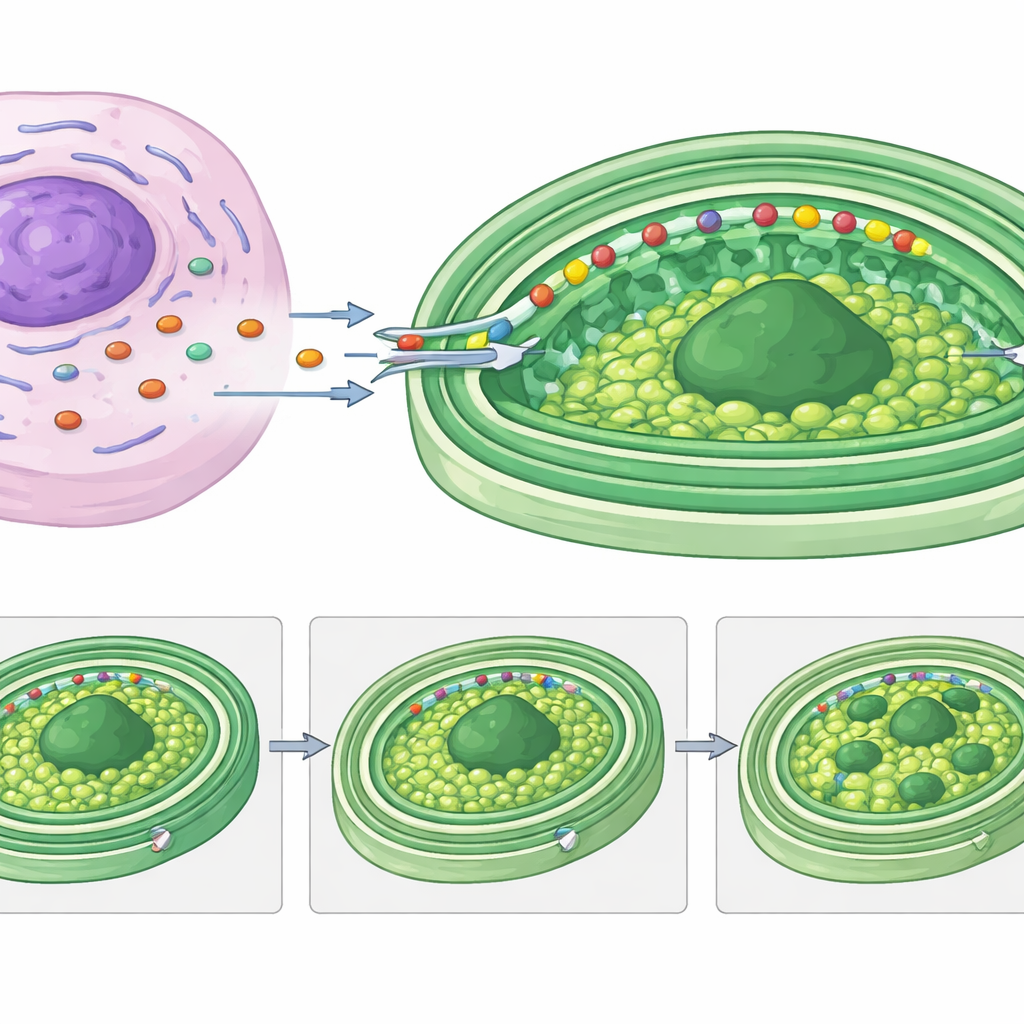
Qué significa esto para la historia de las células complejas
Para el no especialista, el mensaje clave es que Rapaza viridis muestra una versión viva y reversible de lo que pudo suceder cuando células antiguas convirtieron por primera vez bacterias libres en partes permanentes como los cloroplastos. Aquí, el hospedador construye rápidamente una asociación molecular temporal: sus propios genes suministran piezas de reemplazo cruciales e incluso remodelan la estructura interna de los cloroplastos robados, todo guiado por etiquetas de entrega especializadas. Este “quimerismo molecular transitorio” demuestra que incluso integraciones de corta duración entre especies pueden ser sofisticadas y finamente ajustadas. Estudiar este sistema ofrece a los científicos un modelo poderoso para descubrir cómo las células complejas aprendieron a controlar, alimentar y usar de forma segura fábricas de energía foráneas —y cómo nuevos orgánulos aún pueden surgir a lo largo del tiempo evolutivo.
Cita: Kashiyama, Y., Maruyama, M., Nakazawa, M. et al. Transient molecular chimerism for exploiting xenogeneic organelles. Nat Commun 17, 2371 (2026). https://doi.org/10.1038/s41467-026-70516-x
Palabras clave: kleptoplastia, evolución de los cloroplastos, Rapaza viridis, <keyword>biogénesis de orgánulos