Clear Sky Science · es
Caracterización sin etiquetas de masa y tamaño de biomoléculas de pocos kDa mediante microscopía de dispersión nanofluídica aumentada por transformadores de visión jerárquicos
Ver las moléculas más pequeñas
Muchos de los mensajeros más importantes del cuerpo —como hormonas y señales inmunitarias— son tan diminutos que han sido prácticamente invisibles para microscopios potentes a menos que se les añadan etiquetas fluorescentes. Esas etiquetas pueden alterar el comportamiento de las moléculas, un inconveniente serio para el desarrollo de fármacos y la biología básica. Este estudio presenta una forma de pesar y medir individualmente moléculas tan pequeñas como la insulina sin necesidad de etiquetas, empleando una combinación de chips nanofluidicos y una inteligencia artificial avanzada. Abre la posibilidad de observar biomoléculas clave en su estado natural, una por una.
Canales minúsculos como tubos de ensayo
En el núcleo del método está la microscopía de dispersión nanofluídica, que utiliza un chip del tamaño de una uña con canales extremadamente estrechos. Esos canales tienen solo unas decenas de nanómetros de ancho —miles de veces más finos que un cabello humano. Las moléculas disueltas en un tampón se desplazan libremente a través de esos canales en lugar de quedar adheridas a una superficie. Al iluminar el chip con luz visible, tanto las paredes del canal como cualquier molécula que pase dispersan la luz. Dado que el canal es mucho mayor que la molécula, la luz dispersada por ambos interfiere de una manera que amplifica considerablemente la señal óptica de la molécula. Al restar imágenes de un canal vacío de las imágenes tomadas cuando hay una molécula presente, los investigadores obtienen un registro similar a una película (un cinemógrafo) de su paso por el canal, que contiene información sobre su masa y la rapidez con que difunde.
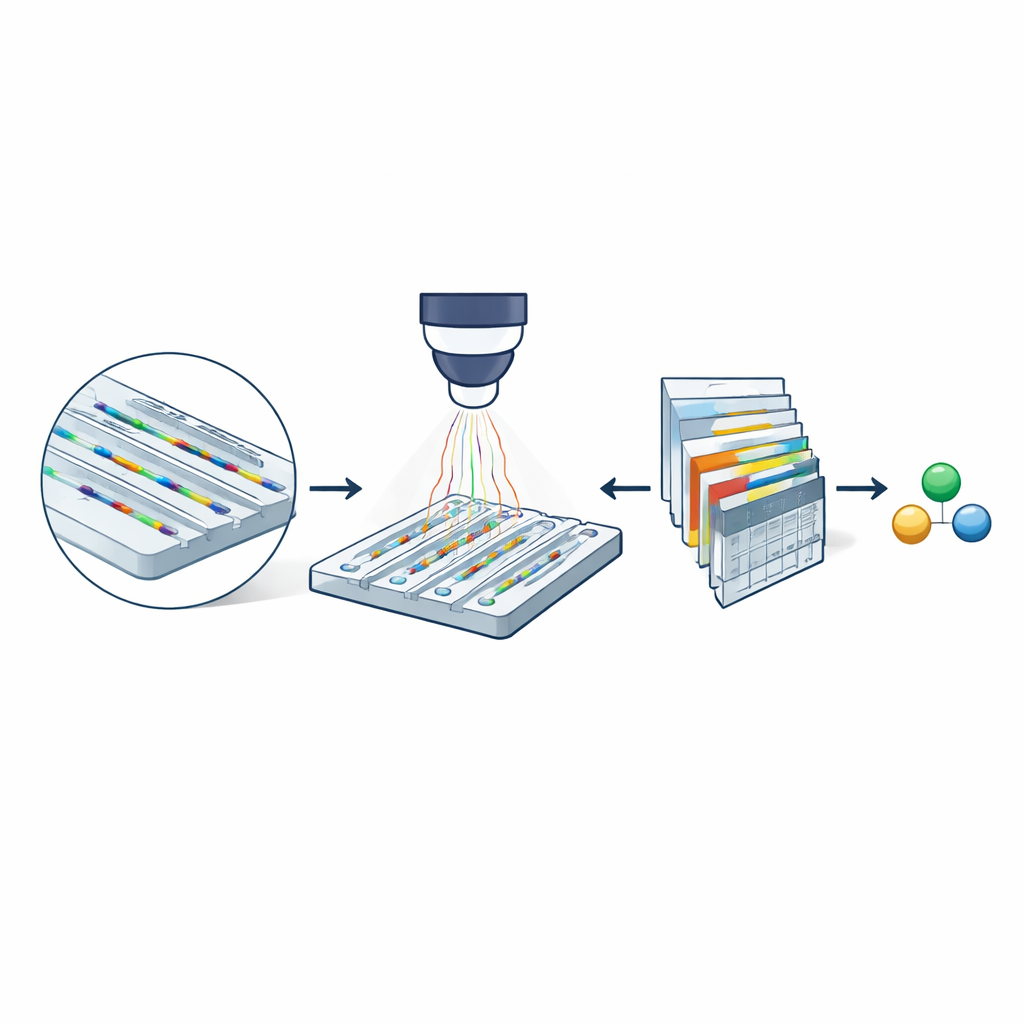
Por qué importan los canales más estrechos
Incluso con este refuerzo óptico, versiones anteriores de la técnica solo podían caracterizar moléculas más pesadas de aproximadamente 60 kilodaltons —proteínas grandes típicas— porque las señales de especies más pequeñas se perdían en el ruido. El equipo demuestra que reducir la sección transversal de los nano canales mejora dramáticamente la sensibilidad: el contraste óptico de una molécula aumenta a medida que disminuye el área del canal. Experimentos que comparan dos tamaños de canal con la proteína albúmina sérica bovina muestran que su trayectoria es claramente visible en el canal más estrecho pero casi desaparece en el más ancho. Este simple cambio geométrico sugiere que, en principio, podrían detectarse biomoléculas mucho más pequeñas si sus señales tenues pueden extraerse de forma fiable de secuencias de imagen ruidosas.
Dejar que una IA lea películas ruidosas
Para alcanzar este régimen, los investigadores desarrollaron un modelo de aprendizaje profundo especializado llamado transformador de visión jerárquico. En lugar de intentar reconstruir la trayectoria exacta de cada molécula píxel a píxel, el modelo explora el cinemógrafo a múltiples escalas y produce dos salidas: un mapa de probabilidad que marca dónde es probable que haya una molécula en cada punto del espacio y del tiempo, y un mapa de propiedades que codifica estimaciones de masa molecular y tamaño hidrodinámico. Al ponderar las estimaciones de propiedades con el mapa de probabilidad, el modelo puede ignorar regiones que son principalmente ruido. El entrenamiento se basa completamente en trayectorias simuladas superpuestas sobre ruido de fondo medido experimentalmente, lo que permite al sistema aprender cómo deben verse las señales reales incluso cuando son apenas visibles a simple vista.
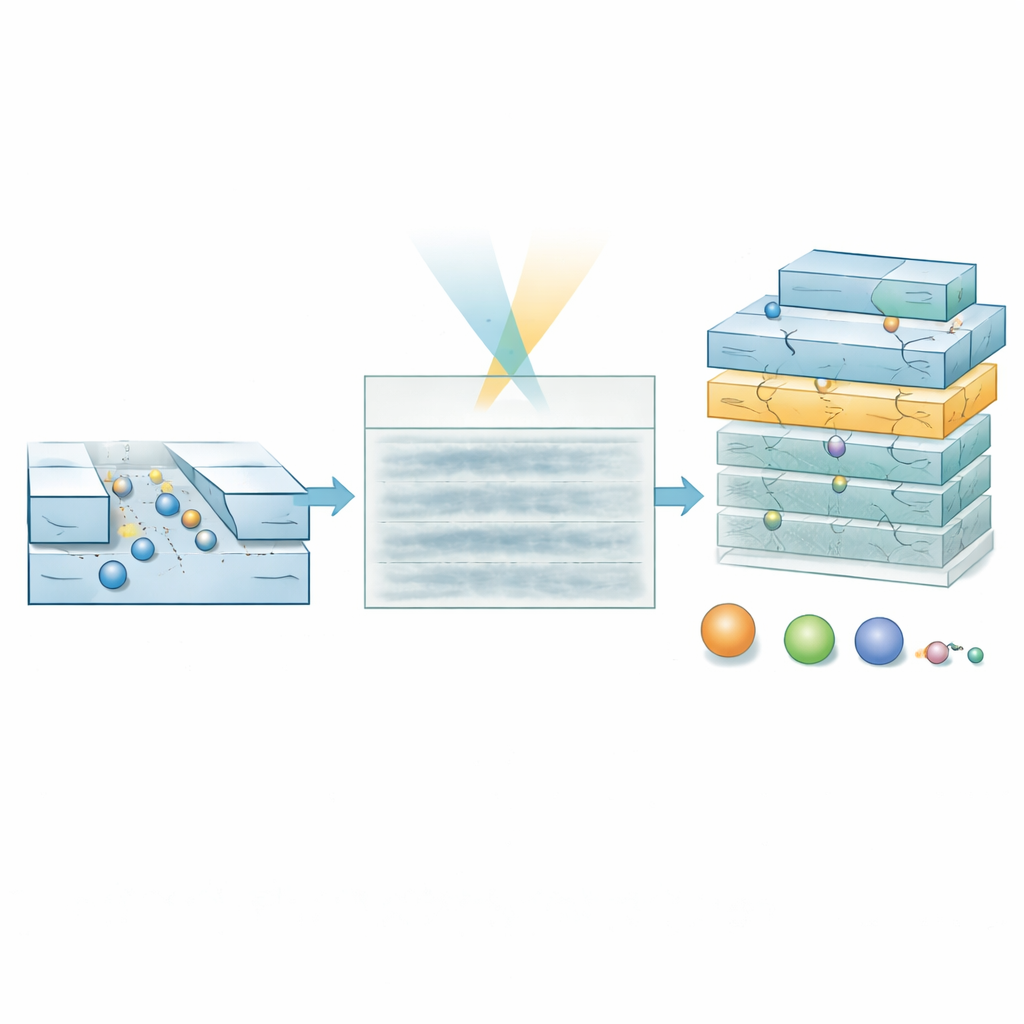
Pruebas con ADN y moléculas hormonales
Los autores validaron primero el enfoque usando una "escalera" estándar de ADN, una mezcla de fragmentos de doble hebra de longitudes y masas conocidas, en canales relativamente anchos donde todos los fragmentos están deliberadamente por debajo del límite habitual de detección. En las películas sin procesar no se aprecian trazas claras de ADN. Sin embargo, el modelo de IA produce mapas de probabilidad que destacan correctamente por dónde pasan las moléculas y predice masas que coinciden con los valores esperados una vez que se filtran los datos de baja confianza. El método también informa correctamente tamaños efectivos más pequeños para los fragmentos rígidos y en forma de varilla del ADN que su longitud física completa, reflejando cómo su forma afecta la difusión. La prueba más exigente utilizó canales ultrasmall para estudiar la hormona péptida insulina, que pesa solo alrededor de 5,8 kilodaltons y tiene unos 1,5 nanómetros de diámetro. Aquí también, los cinemógrafos parecen carentes de rasgos, pero el modelo extrae un grupo compacto de valores de masa y tamaño en excelente acuerdo con cifras de la literatura, claramente separados de los controles con solo tampón.
Empujando los límites
Para entender hasta dónde puede llegar esta estrategia, el equipo comparó la precisión del modelo con la cota inferior de Cramér–Rao, un límite estadístico que define la mejor exactitud posible para cualquier estimador insesgado dado el ruido en los datos. Usando grandes conjuntos de simulaciones, muestran que cuando el número de fotogramas que contribuyen a la trayectoria de una molécula supera aproximadamente las diez mil imágenes, las estimaciones de masa y tamaño del modelo se aproximan a este óptimo teórico incluso para una partícula de seis kilodaltons. Experimentos con insulina a diferentes concentraciones reproducen la misma tendencia: trayectorias efectivas más largas proporcionan medidas más precisas, limitadas principalmente por cuánto tiempo moléculas diminutas y de difusión rápida permanecen en campo. Los autores proponen estrategias futuras —como atrapar suavemente las moléculas en los canales o reutilizar datos mediante remuestreo (bootstrapping)— para aumentar aún más el tiempo de observación utilizable.
Qué significa esto para la biología y la medicina
En términos sencillos, este trabajo demuestra que ahora es posible pesar y medir algunas de las moléculas más pequeñas e importantes del cuerpo de forma individual, sin tocarlas con etiquetas fluorescentes ni pegarlas a una superficie. Al casar canales nanofabricados con una IA diseñada específicamente para leer películas ruidosas de dispersión de luz, el método reduce el límite de detección de masa de este enfoque de microscopía sin etiquetas en aproximadamente un factor de diez. Esto abre la puerta al estudio a nivel de una sola molécula de familias de pequeñas proteínas señalizadoras y péptidos hormonales —como citocinas, quimiocinas e insulina— y a caracterizar diminutos nanopartículas biológicas y transportadores de fármacos con sensibilidad sin precedentes. A medida que la tecnología madure, podría convertirse en una herramienta poderosa en el descubrimiento de fármacos, el diagnóstico y los estudios fundamentales sobre cómo las interacciones moleculares moldean la vida en las escalas más pequeñas.
Cita: K. Moberg, H., Yeroshenko, B., Fritzsche, J. et al. Label-free mass and size characterization of few-kDa biomolecules by hierarchical vision transformer augmented nanofluidic scattering microscopy. Nat Commun 17, 2533 (2026). https://doi.org/10.1038/s41467-026-70514-z
Palabras clave: microscopía de una sola molécula sin etiquetas, dispersión nanofluídica, transformador de visión, pequeñas biomoléculas, detección de insulina