Clear Sky Science · es
La hidrofobicidad superficial y la rigidez determinan la corona de proteínas en nanopartículas administradas por vía oral para el tratamiento de la colitis
Convertir pastillas en tratamientos más inteligentes
Las personas con enfermedades inflamatorias intestinales como la colitis suelen tomar fármacos antiinflamatorios potentes, pero gran parte de cada dosis se desperdicia o provoca efectos secundarios en otras partes del cuerpo. Este estudio explora una forma nueva de hacer que los medicamentos orales actúen más como misiles guiados: diseñando diminutas partículas portadoras de fármaco que reclutan las propias proteínas intestinales del organismo como un sistema de orientación natural, ayudando a que los fármacos lleguen a las células inmunitarias que impulsan la inflamación intestinal.
Cómo viste el intestino a las nanopartículas
Cuando una nanopartícula entra en el cuerpo, se recubre rápidamente con una fina capa de proteínas, formando lo que los científicos llaman una “corona de proteínas”. En el intestino enfermo, esta corona es muy distinta de la que se forma en tejido sano porque la mezcla proteica local cambia. Los autores observaron previamente que la colitis genera una corona intestinal especial que dirige de forma modesta las partículas hacia células inmunitarias llamadas macrófagos, que tanto alimentan como resuelven la inflamación. Aquí, se propusieron moldear deliberadamente esa corona ajustando dos características básicas de las partículas portadoras de fármaco: su repelencia al agua (hidrofobicidad) y su rigidez, para convertir un efecto leve producido por la enfermedad en una estrategia de dirigimiento potente.
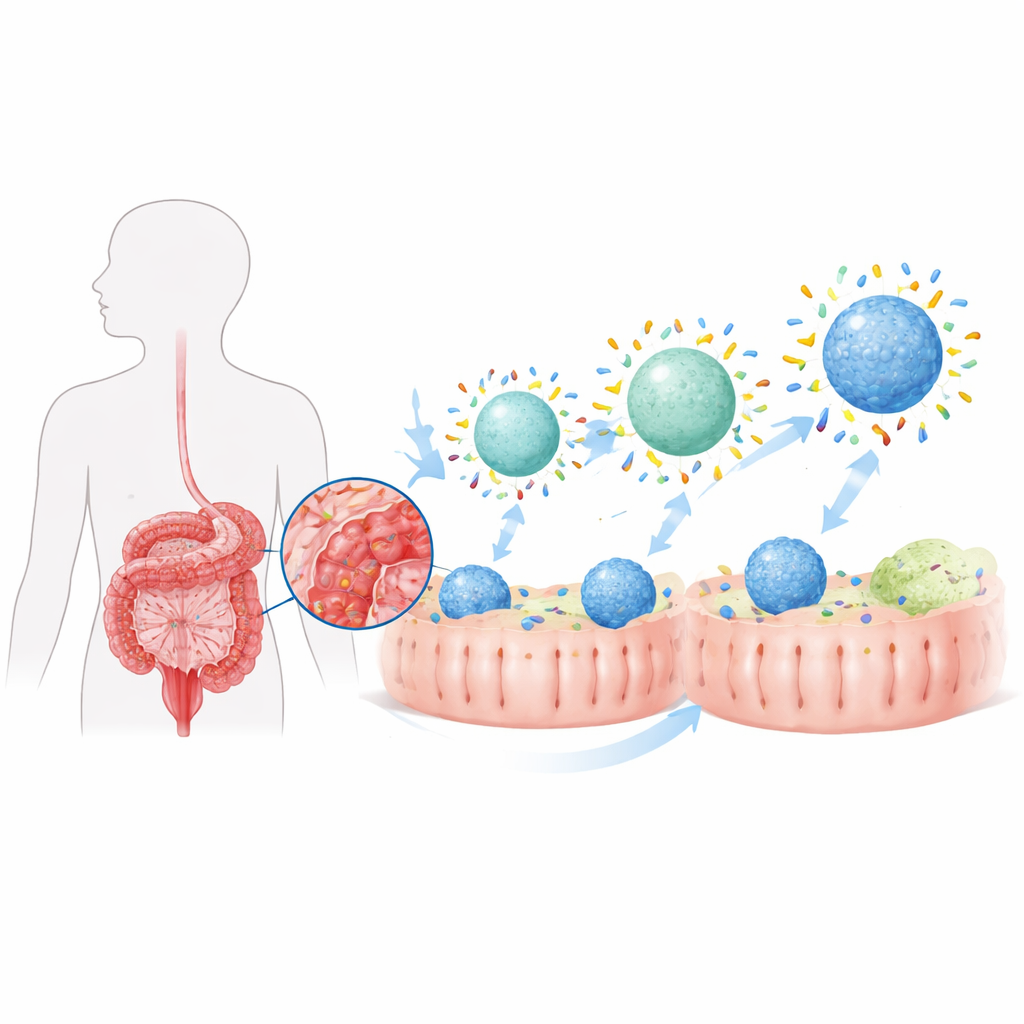
Hacer las partículas más atractivas para las proteínas
El equipo fabricó nanopartículas a base de lípidos, parecidas a pequeñas burbujas de grasa, y reguló cuánto eran atraídas o repelidas por el agua en su superficie añadiendo distintas cantidades de un polímero recubridor común. Las partículas con superficies más hidrofóbicas se unieron a muchas más proteínas intestinales cuando se expusieron a fluidos de colitis, tanto en animales como en tubos de ensayo. Cuando estas partículas “fóbicas” se cargaron con el esteroide budesonida y se administraron por vía oral a ratas con colitis, entregaron mucho más fármaco a los macrófagos del colon que las versiones más hidrofílicas. Como resultado, los animales tratados recuperaron más peso corporal, mostraron menos acortamiento y daño del colon, y presentaron niveles más bajos de moléculas inflamatorias en el intestino. Sin embargo, aunque la inflamación mejoró, no volvió por completo al estado saludable, lo que sugiere que aumentar solo la cantidad total de proteínas de la corona no bastaba.
Endurecer las partículas para elegir mejores compañeras
Para llevar el concepto más lejos, los investigadores mantuvieron las superficies hidrofóbicas pero cambiaron la estructura interna para hacer partículas blandas, intermedias o rígidas rellenando sus núcleos con esferas plásticas de distintos tamaños. Las tres seguían captando cantidades totales similares de proteína intestinal, pero la mezcla proteica cambió. Las partículas más rígidas formaron coronas especialmente ricas en proteínas que pueden unirse a receptores de macrófagos o transportar pequeños nutrientes que esas células internalizan. Una de esas proteínas, S100A8, es abundante en intestinos inflamados y puede interactuar con receptores específicos de macrófagos. Bloquear S100A8 en la corona redujo drásticamente la captación de las partículas rígidas por los macrófagos, revelándola como un componente clave de dirigimiento seleccionado por la rigidez de la partícula.
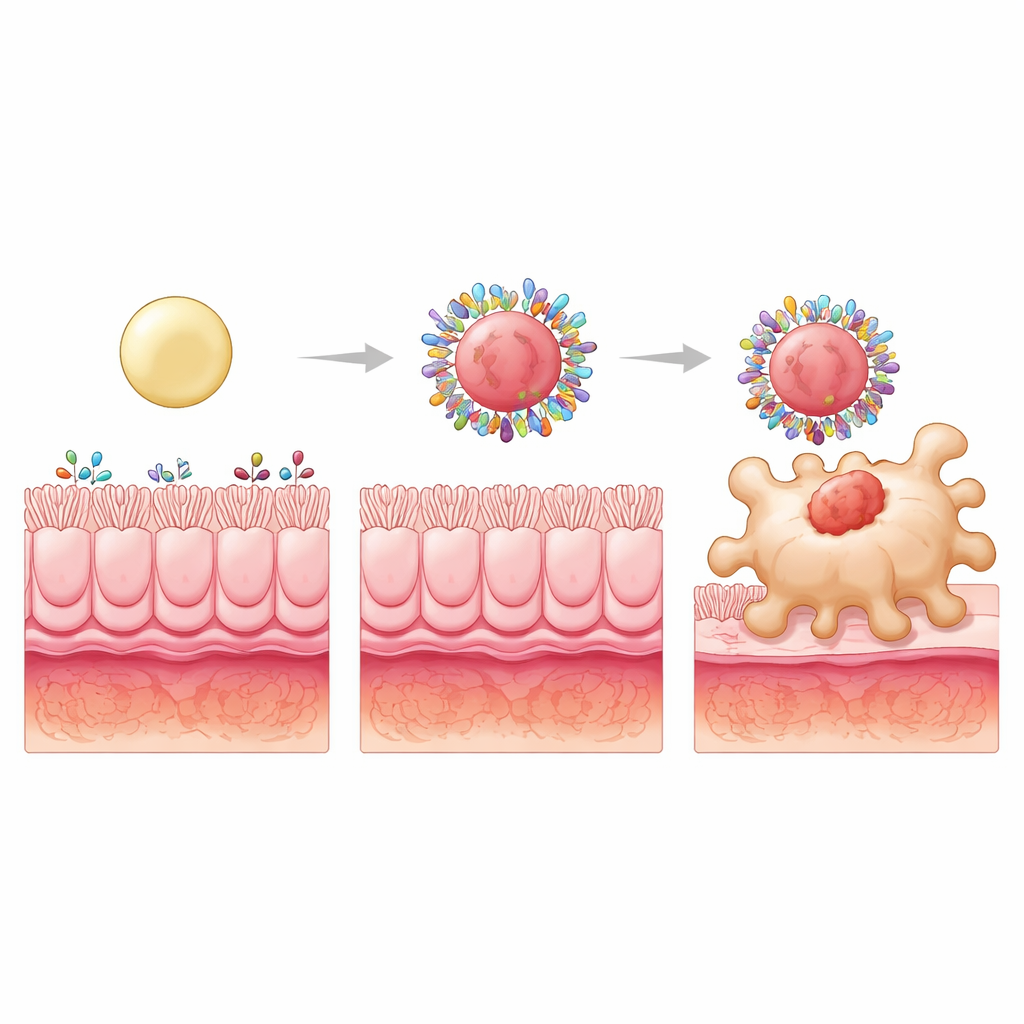
De un mejor dirigimiento a una mejor curación
Cuando la budesonida se cargó en estas partículas de alta hidrofobicidad y alta rigidez y se administró por vía oral a ratas con colitis, los beneficios fueron llamativos. La formulación rígida no solo redujo el daño intestinal y el estrés oxidativo, sino que también normalizó múltiples señales inflamatorias a niveles observados en animales sanos. Restauró un equilibrio más sano entre tipos de macrófagos “ataque” y “calma” y aumentó las células T reguladoras, que ayudan a controlar las respuestas inmunitarias. Es importante destacar que estas mejoras dependieron del entorno proteico alterado por la enfermedad en la colitis; el mismo diseño no mostró un dirigimiento especial en ratas sanas, subrayando que la corona es un aliado dinámico y específico de la enfermedad.
Por qué esto importa para futuras medicinas
Este trabajo demuestra que podemos guiar a las propias proteínas del organismo para que actúen como “etiquetas” inteligentes y autorrenovables en los portadores orales de fármacos simplemente ajustando las propiedades superficiales y mecánicas de los portadores. Primero aumentando la captura de proteínas mediante superficies hidrofóbicas y luego usando la rigidez para favorecer proteínas que reclaman macrófagos como S100A8, los investigadores crearon nanopartículas que buscan de forma natural las células inmunitarias que impulsan la colitis y entregan la terapia donde más se necesita. La misma lógica de diseño —manipular cómo se sienten y se comportan las partículas en la superficie intestinal— podría adaptarse a muchos tipos de nanomedicinas y enfermedades, ofreciendo una vía nueva y más sutil hacia el tratamiento dirigido sin añadir moléculas de dirigimiento artificiales.
Cita: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
Palabras clave: administración de fármacos con nanopartículas, enfermedad inflamatoria intestinal, corona de proteínas, nanomedicina oral, dirigido a macrófagos