Clear Sky Science · es
Un atlas de interacciones a nivel de género entre ortólogos de NS4B identifica un papel conservado de la UFMilación en la replicación de ortoflavivirus
Por qué importa este estudio sobre virus
Virus como el dengue, el Zika y el West Nile se están extendiendo a nuevas regiones y pueden causar desde fiebre hasta infecciones cerebrales y malformaciones congénitas. Sin embargo, aún carecemos de tratamientos amplios y fiables. Este trabajo explora cómo una alianza oculta entre estos virus y un sistema celular de etiquetado poco conocido, la UFMilación, ayuda a los patógenos a multiplicarse. Al cartografiar esta relación a lo largo de muchos virus emparentados, los autores descubren una vulnerabilidad compartida que podría explotarse para desarrollar futuros fármacos antivirales.
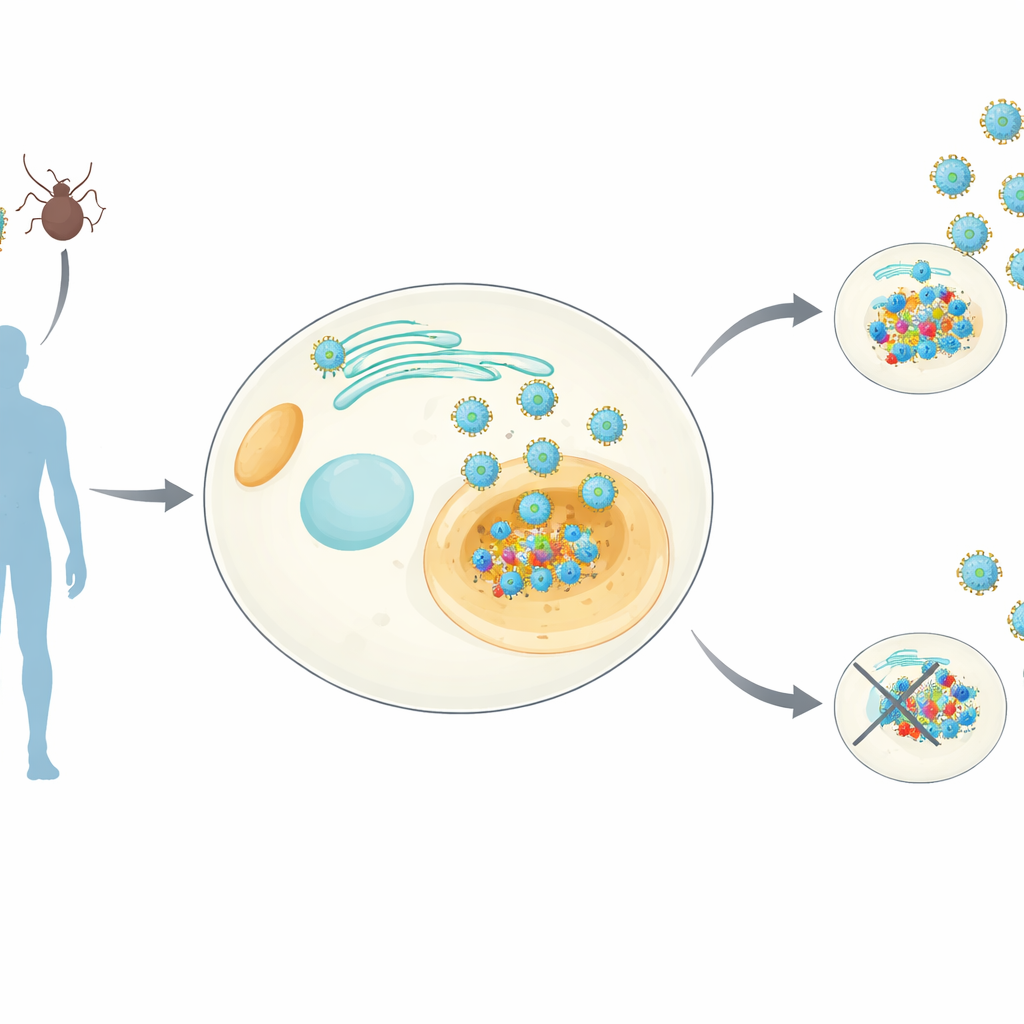
Siguiendo a un infiltrado viral clave
Los ortoflavivirus —el grupo que incluye dengue, Zika, fiebre amarilla y otros— llevan una pequeña proteína llamada NS4B que se integra en las membranas dentro de nuestras células. Se sabe que NS4B es esencial para la replicación viral, pero sus funciones exactas han permanecido poco claras. Los investigadores crearon líneas celulares humanas que producen de forma estable NS4B procedente de ocho ortoflavivirus diferentes. Luego emplearon técnicas sensibles de espectrometría de masas para captar NS4B junto con las proteínas humanas que se le adhieren y, en paralelo, midieron cómo la expresión de NS4B altera la mezcla global de proteínas en la célula. Esto produjo un “atlas de interacciones” a nivel de género —que denominan NS4Bome— mostrando dianas huésped comunes y específicas de cada virus.
Trucos compartidos y adaptaciones propias
El atlas reveló 538 proteínas humanas que interactúan con NS4B y más de 500 cuya abundancia cambia cuando NS4B está presente. Muchas de ellas se concentran en vías que gestionan la producción de energía en las mitocondrias, la conformación de membranas internas y el transporte de proteínas y lípidos recién sintetizados. Algunas interacciones fueron compartidas por la mayoría de los virus, lo que sugiere trucos conservados evolutivamente que usan todos los ortoflavivirus. Otras aparecieron solo en ciertas especies o cepas, lo que podría explicar por qué algunos virus prefieren mosquitos frente a garrapatas o provocan enfermedad cerebral en lugar de fiebre hemorrágica. Esta visión sistemática convierte un conjunto enmarañado de estudios anteriores fragmentarios en un mapa coherente de cómo estos virus reprograman la célula.
Un aliado sorprendente: el sistema de UFMilación
Entre los muchos socios con los que NS4B se vinculó, destacó uno: UBA5, la enzima iniciadora de la vía de UFMilación. La UFMilación es un sistema celular que adjunta una pequeña proteína etiqueta, UFM1, a objetivos seleccionados, influyendo en procesos como el control de calidad de proteínas y las respuestas al estrés. Mediante interferencia por ARN y deleciones génicas basadas en CRISPR, el equipo mostró que las células carentes de UBA5 o incapaces de llevar a cabo la UFMilación presentaban una replicación muy reducida del Zika y de varios virus relacionados. Reintroducir UBA5 normal restauró el crecimiento viral, mientras que formas mutantes que ya no podían impulsar la UFMilación no lo hicieron, demostrando que la propia actividad de etiquetado es crucial para la infección.
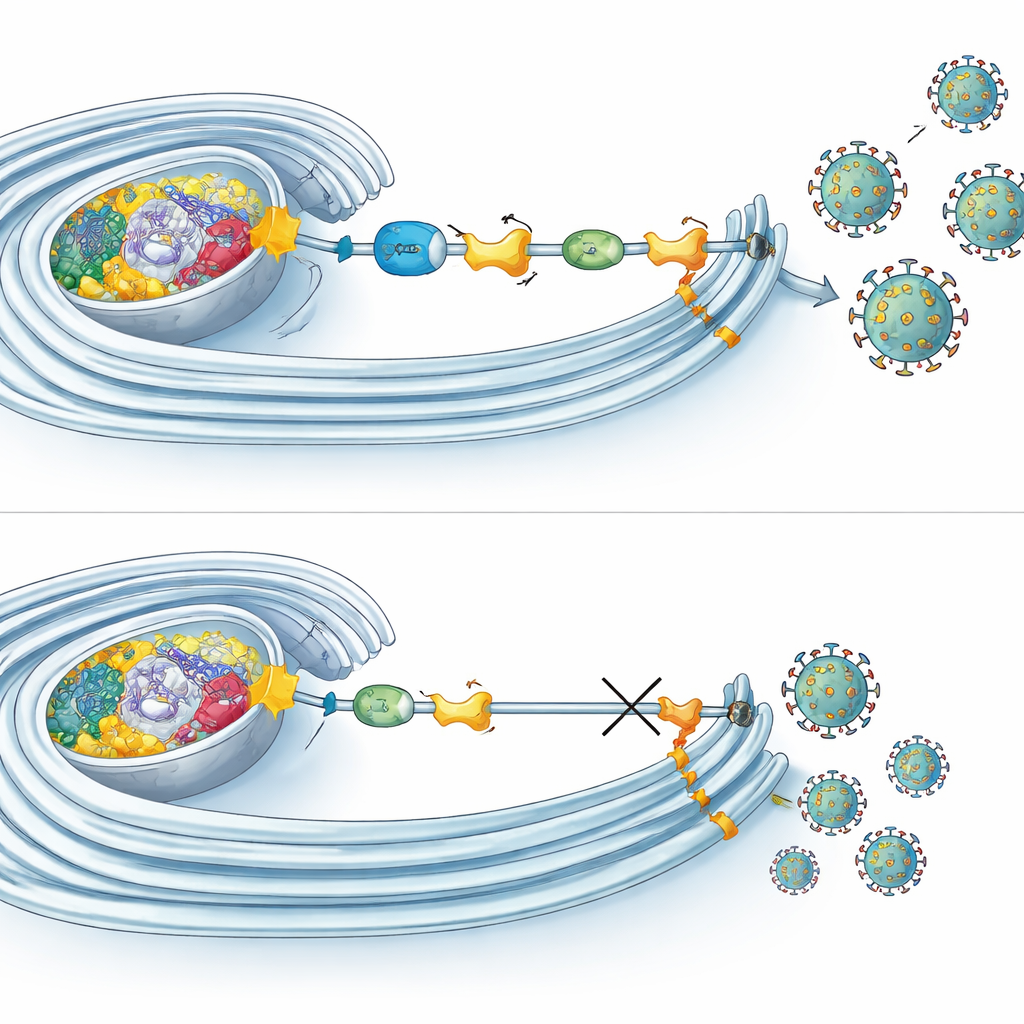
Cómo la etiqueta sostiene las fábricas virales
Experimentos de microscopía y bioquímica revelaron que múltiples componentes de la UFMilación se concentran en los mismos lugares donde el ARN viral se copia dentro de membranas remodeladas. Allí se asocian no solo con NS4B sino también con otras proteínas virales que montan la maquinaria de replicación. Curiosamente, bloquear la UFMilación no detuvo la entrada viral, la producción de ARN ni la síntesis proteica. En su lugar, afectó principalmente las etapas tardías del ciclo, como el ensamblaje o la liberación de partículas infecciosas. Al mismo tiempo, la UFMilación resultó influir en la respiración mitocondrial: cuando la vía se desactivó, las células mostraron un consumo de oxígeno reducido y formas mitocondriales alteradas. En contraste, al inicio de la infección por Zika, la respiración mitocondrial se intensificó, lo que sugiere que los virus pueden aprovechar la UFMilación para aumentar la producción de energía celular justo cuando más la necesitan.
Probando un fármaco en células y peces diminutos
Los autores recurrieron luego a un compuesto de pequeña molécula, DKM 2‑93, que bloquea el sitio activo de UBA5. En células humanas cultivadas, este inhibidor redujo la producción del virus Zika aproximadamente diez veces a dosis que mantenían, en gran medida, la salud celular, y mostró actividad en varios tipos celulares. Para evaluar si esta estrategia funcionaría en un organismo vivo, usaron un modelo de infección por Zika en pez cebra, que reproduce características clave de la enfermedad en el cerebro en desarrollo. Tratar embriones infectados con DKM 2‑93 durante el desarrollo cerebral temprano disminuyó de forma significativa los niveles de ARN viral y redujo la proporción de peces con malformaciones graves, indicando un beneficio antiviral real in vivo.
Qué significa esto para futuros tratamientos
Al construir un mapa exhaustivo de cómo NS4B de muchos ortoflavivirus interactúa con proteínas humanas, este estudio destaca la UFMilación como una vía auxiliar conservada de la que estos virus dependen para producir partículas infecciosas. Dado que el mismo sistema huésped parece apoyar al dengue, Zika, West Nile y otros, los fármacos que atenúen selectivamente la UFMilación podrían actuar como antivirales de amplio espectro, en lugar de dirigirse a un solo virus. Aunque se necesita más trabajo para identificar exactamente qué proteínas son etiquetadas y para garantizar la seguridad, los hallazgos señalan una diana prometedora basada en el huésped que podría, algún día, ayudar a mitigar brotes de múltiples enfermedades transmitidas por mosquitos y garrapatas con un único enfoque terapéutico.
Cita: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
Palabras clave: virus Zika, dengue, interacciones huésped‑virus, UFMilación, antivirales de amplio espectro