Clear Sky Science · es
Control de la función lisosomal por la proteína activadora de GTPasa TBC1D9B y su compañera de unión TMEM55B
Cómo los centros de reciclaje celulares mantienen el equilibrio
Dentro de cada una de nuestras células hay pequeñas vesículas llamadas lisosomas que funcionan como centros de reciclaje y nodos de control del crecimiento. Cuando funcionan bien, las piezas desgastadas se degradan y sus componentes se reutilizan; cuando fallan, los desechos se acumulan y pueden surgir enfermedades, entre ellas la neurodegeneración y el cáncer. Este estudio revela cómo dos proteínas poco conocidas ayudan a cambiar los lisosomas entre un estado móvil, favorable al crecimiento, y un modo agrupado, orientado a la limpieza de residuos, arrojando luz sobre cómo las células se adaptan a la abundancia y la escasez.
Mover los centros de reciclaje por la célula
Los lisosomas no están fijos. Viajan a lo largo de vías internas, empujados hacia fuera por un conjunto de motores moleculares y atraídos hacia el interior por otro. Su localización en la célula importa: cuando los nutrientes son abundantes, los lisosomas se despliegan hacia las regiones periféricas y ayudan a sostener las señales de crecimiento; cuando falta alimento, retroceden hacia el centro, se acidifican y aumentan la degradación de material celular. Se sabe que una pequeña proteína con comportamiento de interruptor llamada ARL8 impulsa a los lisosomas hacia afuera, pero hasta ahora nadie había identificado un sistema de frenado dedicado para contenerla. Los autores sospechaban que tal freno sería crucial para permitir que las células cambien rápidamente a un modo de conservación durante el ayuno.
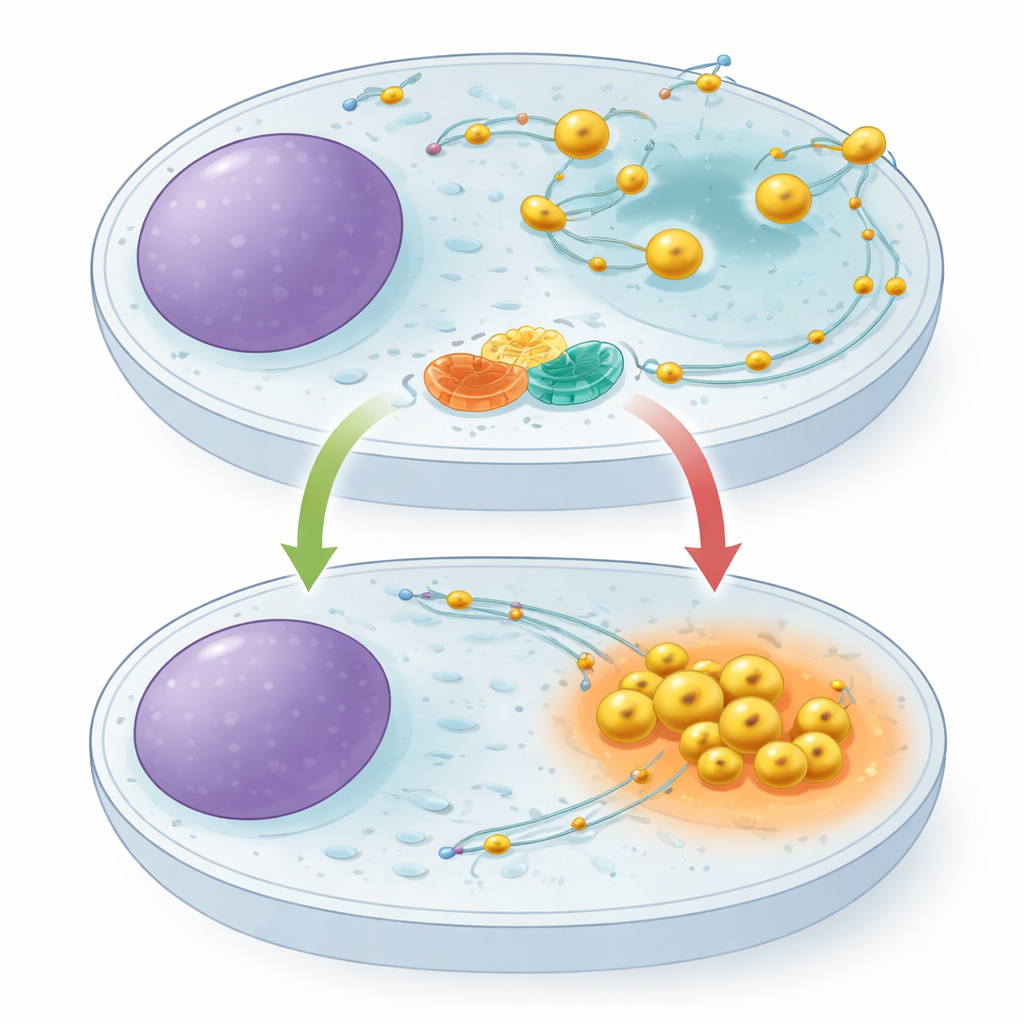
Una asociación molecular en la superficie lisosomal
Usando técnicas de pesca de proteínas y espectrometría de masas, los investigadores descubrieron que una proteína llamada TBC1D9B se une a una proteína de la membrana lisosomal llamada TMEM55B. TMEM55B se sitúa a través de la envoltura externa del lisosoma, mientras que TBC1D9B es en gran parte soluble y puede acoplarse a la membrana. El equipo mostró que estas dos forman un complejo directo: TBC1D9B purificada se adhiere a la porción expuesta de TMEM55B en tubos de ensayo, y versiones etiquetadas de las proteínas se co‑precipitan a partir de extractos celulares. Un mapeo cuidadoso de los segmentos proteicos reveló que varias regiones de TBC1D9B contactan con TMEM55B, posicionando a TBC1D9B en la superficie lisosomal sin bloquear la parte de la proteína responsable de su actividad catalítica.
Cuando falla el freno, los lisosomas se descontrolan
Para averiguar qué hace esta asociación, los autores usaron edición CRISPR para eliminar TMEM55B o TBC1D9B de células humanas. En ambos casos, los lisosomas dejaron de agruparse cerca del núcleo y en su lugar se dispersaron hacia el borde celular y se movieron más rápido a lo largo de sus vías, imitando a células en un estado de alimentación constante. Reintroducir TBC1D9B normal restauró la posición adecuada, pero una versión carente de poder catalítico no lo hizo, lo que indica que su actividad enzimática es esencial. Cuando las células fueron sometidas a inanición, las células control retiraron sus lisosomas hacia el interior y aumentaron su capacidad digestiva, como mostró la mayor actividad de enzimas clave y la intensificación de la degradación de cargas experimentales. Las células sin TMEM55B o TBC1D9B no pudieron hacer esto: sus lisosomas permanecieron periféricos y su respuesta degradativa al ayuno se vio atenuada. La autofagia, el proceso por el cual las células se comen componentes dañados, también quedó afectada, con un procesamiento menos eficiente de un informe de autofagia y acumulación de la proteína adaptadora p62.
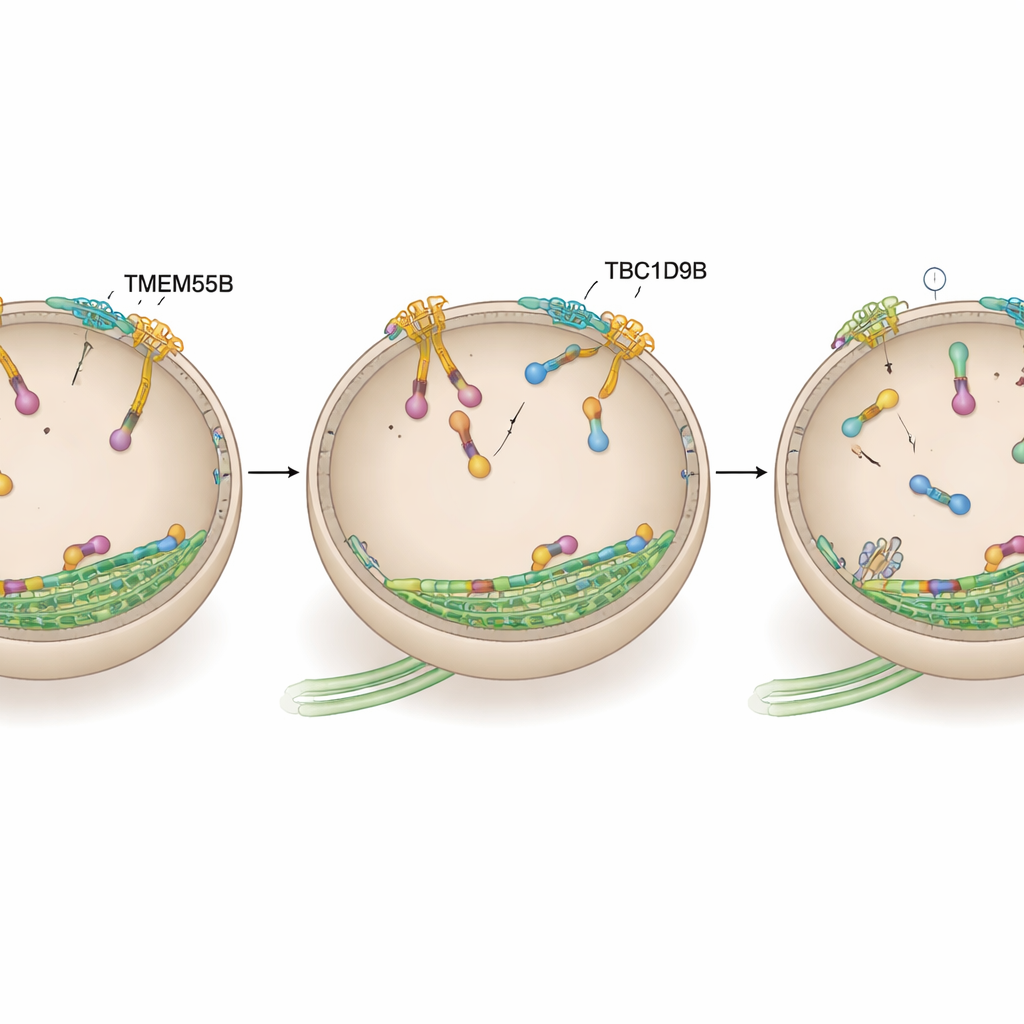
Apagar el motor lisosomal
El equipo preguntó luego si TBC1D9B ejerce sus efectos actuando directamente sobre ARL8, el interruptor motor que impulsa hacia afuera. Usando etiquetado por proximidad en neuronas humanas y pruebas de unión en líneas celulares y con proteínas purificadas, mostraron que TBC1D9B se une selectivamente a la forma activa cargada con GTP de la variante ARL8B, pero no a su forma inactiva ni a la ARL8A estrechamente relacionada. Modelos estructurales predijeron que residuos clave en TBC1D9B contactan el bolsillo de GTP de ARL8B. En ensayos bioquímicos, TBC1D9B aceleró la hidrólisis del GTP unido a ARL8B, convirtiendo efectivamente la proteína de su estado “activado” a su estado “desactivado”; una versión mutante de TBC1D9B que carecía de estos residuos ya no pudo hacerlo. En consonancia con esto, las células carentes de TMEM55B o TBC1D9B mostraron aumento de ARL8B en los lisosomas, mientras que la sobreexpresión de TBC1D9B atrajo los lisosomas de nuevo hacia el centro, de manera similar a reducir la actividad de ARL8B.
Una nueva perilla de control para el mantenimiento celular
Finalmente, los autores evaluaron si este freno sobre ARL8B explica los cambios celulares observados cuando falta TBC1D9B. Cuando ARL8B fue eliminado, los lisosomas permanecieron agrupados cerca del núcleo independientemente de la presencia de TMEM55B o TBC1D9B, y los defectos en la autofagia causados por la pérdida de TBC1D9B se superaron en gran medida. En conjunto, los datos apoyan un modelo en el que TMEM55B recluta a TBC1D9B a los lisosomas, donde inactiva ARL8B y permite que los lisosomas pasen de un estado disperso, que favorece el crecimiento, a otro centralizado y centrado en la digestión. Para los no especialistas, esto significa que el estudio ha descubierto un dial importante que las células usan para decidir cuándo reciclar con más intensidad, un proceso con implicaciones para trastornos de acumulación de desechos en el cerebro, el metabolismo y el cáncer.
Cita: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
Palabras clave: lisosomas, autofagia, señalización celular, transporte de orgánulos, neurodegeneración